Materjalide keemia III kordamisküsimused 1/2
Lisamise aeg:
2015-02-01 13:27:34Vaatamiste arv:
23730Tagasiside:
0 0Kordamisküsimused - Materjalide keemia III 2014/2015
Loeng 1. Sissejuhatus
1. Milleks on energiasalvestus vajalik? Millised on põhilised takistused võimalike tehnoloogiate rakendamisel?
Vajalikkus
Traditsioonilised energiaallikad nagu soojusjaamad ja soojuselektrijaamad kasutavad toorainena valdavalt taastumatuid maavarasid – kivisütt (meil põlevkivi), kütteõli ja maagaasi. Suurem osa liiklusvahenditest sisepõlemismootoriga – taastumatu tooraine nafta.
Varem või hiljem seisab ühiskond vajaduse ees võtta laialdaselt kasutusele taastuvtoorained (nn biokütused). Suhteliselt madala kasuteguriga Carnot termodünaamilisel tsüklil (soojuseülekanne soojemalt kehalt külmemale) põhinevates süsteemides energiaressursside raiskamine.
Üheks võtmeküsimuseks
ebaefektiivse ja keskkonnavaenuliku põlevkivienergeetika ümberkujundamine taastuvenergeetikaks: tuule-, hüdro-, päikse-, maasoojusenergia.
Taastuvenergeetika kaasamiseks piisaval mahul on vajalik kaasata muutlikku energiavaru tasakaalustavad võimsused, millest üheks sobivaimaks variandiks on efektiivsete ning odavate energiasalvestus-süsteemide kasutuselevõtt.
Lüli energia allika ning tegeliku kasutuse vahel:
Painduvus energia kättesaadavuse ning nõudlusprofiili sobitamisel, olenevalt elektrienergia vajaduse ajast, kohast ning hulgast
Kaasaegne (elektrivarustussüsteemide) võrgustik on paljude ühendustega keeruline süsteem – tekivad energia ja võimsuse probleemid usaldusväärse/kvaliteetse elektrienergia tarnel. Täielikud süsteemitõrked on tihti tingitud liiga suureks venitatud võrgustikest või võrgustiku ühe võtmelüli tõrkest, mis põhjustab rikete joa.
Seega, on uuenenud huvi salvestatud energia kaasamiseks süsteemi selliste probleemide lahendamiseks/vältimiseks.
Piirangud
Vee pumpelektrijaam ning suruõhk-salvestus on asukoha spetsiifilised ning ei võimalda energia vabastamist hetkeliselt.
Hooratta rakendamine on veel testprogrammide faasis, võrreldes hüdro- ja suruõhk-energigaga on salvestusmaht väiksem.
Ülijuhtmagnet-energisalvestus on kallis ning alles uurimis- ja arendustegevuse faasis.
Superkondensaatorid sobivad eelkõige suure hetkevõimsuse rakenduseks ning elektrienergia kvaliteedi kontrolliks, sest energia hulk on väiksem.
Kõike laialdasemalt on kasutusel aku-energiasalvestus (erinevad piirangud olenevalt tüübist – jahutuse/kuumutamise nõue, ohutusprobleemid, kõrge hind jne). Samas liiga kallis valik energisalvestuseks aastas ühekordseks laadimise/tühjenemise tsükliks.
2. Mida kujutab endast hajutatud energiatootmine? Mis on selle eelised?
Tuleviku elektriettevõte saab olema hübriidvõrgustik:
traditsioonilisest täiustatud elektrikeskjaamast ja
hajutatud elektritootmisest – laialipaigutatud üksused (tuulegeneraatorid, päikesepaneelid koos energiasalvestussüsteemidega nagu akud, superkondensaatorid, elektrolüüserid/kütuseelemendid.
Hajutatud elektrisüsteemi positiivsed mõjud:
paraneb tarbijate teenindus,
vähenevad kulud (efektiivsus kasvab – vähenevad pikkade ülekandeliinide võimsuskaod),
saavutatakse keskkonda säästvam elektritootmine,
elektriettevõtted suudavad vastu pidada kasvavas konkurentsis.
3. Miks ei ole endiselt taastuvate energiaallikate osakaal elektrienergia tootmises suur?
Enamikku taastuvenergiast ei ole võimalik säilitada ega transportida seda eelnevalt elektrienergiaks muundamata (põletatav biomass – säilitatav ning transporditav, hüdroenergia – säilitatav). Taastuvenergia hetkelise kättesaadavuse ning energiatarbe omavaheline sobitamine on probleemne – eriti üldiselt elektrivõrgust eraldiasetsevatel aladel. See innustab efektiivsete energiasalvestussüsteemide arendamist ning rakendamist lokaalsel tasemel. Kuid tuule tugevus on kõikuv ning päikeseenergia on kättesaadav vaid teatud osa päevast – vaja salvestada.
Taastuvenergia pole reeglina säilitatav ega transporditav (nt tuuleenergia), ühtlasi on see hooajaline ning üldjuhul ei kattu energia tootmise tippvõimsus selle kasutuse tippvõimsusega. See teeb vajalikuks taastuvenergia salvestamise, kuid energia salvestamine on kallis ja vähelevinud tegevus.
Loengud 2 ja 3. Kütuseelemendid (KE)
1. KE kui energiasalvestussüsteemi üldine kirjeldus (s.h. elektroodi-protsessid, eelised-puudused)
Kütuseelement (KE) on elektrokeemiline seade, mis muundab kütuse (vesinik, metaan, butaan, bensiin, diisel, jne) keemilist energiat otse elektrienergiaks
Efektiivne ja minimaalse keskkonna-mõjuga süsteem
Puudub soojusmootoritele omane termodünaamiline piirang (Carnot tsükkel)
Reaktsiooni kontrollitud suunamisel läbi seadme on võimalik reaktsioonienergiat kasutada efektiivselt elektrienergia tootmiseks
„Elektrokeemiline kütuse põlemine“
4 funktsionaalset koostiselementi:
Katood (O2 redutseerumine)
Anood (kütuse oksüdeerumine)
Elektrolüüt
Voolukollektor/moodulühenduse vahelüli (interconnect) gaasivoolu kanalitega
Individuaalsed ühikrakud saab elektriliste kontaktide abil ühendada soovitud väljundmahtuvusega (energiaga) mooduliks.
KE elektroodiprotsessid
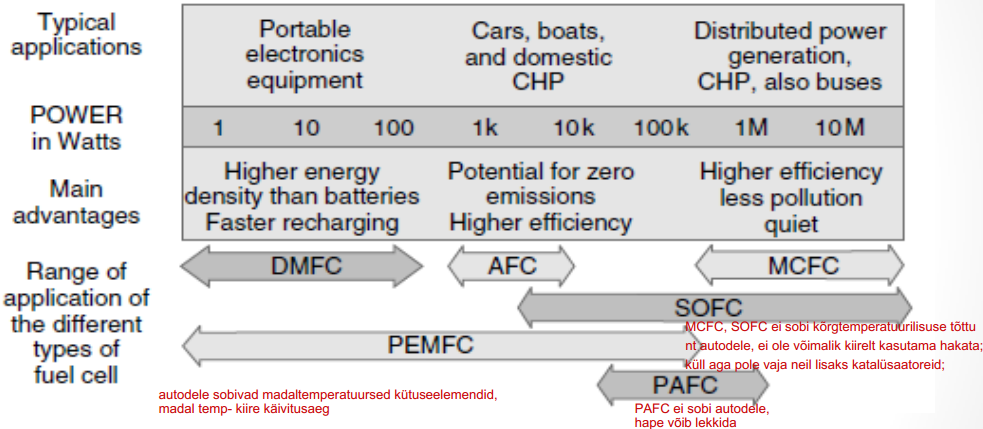
Vesinikul ja õhul (hapnikul) töötava pöörduva KE elektroodireaktsioonid:
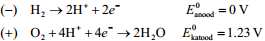
Elektrokeemilisel oksüdeerimisel tekitatud H+ transporditakse (–) elektroodilt (+) elektroodile läbi ioonjuhtiva (kuid elektroonselt isoleeriva) membraani
On olemas ka O2– ioonjuhid
Vabastatud elektronid transporditakse läbi välise vooluahela katoodile, kus kasutatakse O2 redutseerimiseks, et moodustada koos prootonitega vesi.
Summaarne reaktsioon:
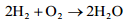
Ideaalselt peaks pöörduva raku potentsiaal olema E0= 1.23 V (1.18 V kui gaasiline vesi reaktsiooni produkt – töötemperatuur kõrgem).
Faraday seadus:
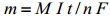
m ja M - reageeriva ühendi mass ja molaarmass I - süsteemi läbiv vooluhulk (A) t - reaktsioonikestus (s) n - üleminevate elektronide arv
Seega, kütuseelemendist kättesaadav vool on otseselt seotud H2 ja O2 reageerimise kiirustega vastavatel elektroodidel.
Praktiliselt pole ideaalne rakupinge 1.23 V KE töötamisel kättesaadav.
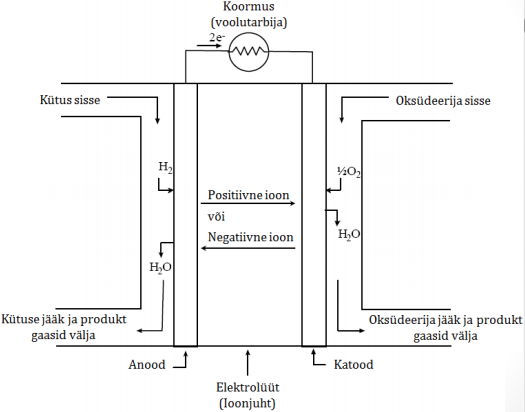 KE eelised elektrienergia genereerimiseks
KE eelised elektrienergia genereerimiseks
Kõrge termodünaamiline efektiivsus (vs. Carnot tsükkel mehaanilises mootoris).
KE korral muundatakse keemiline energia otse elektrienergiaks. Ideaalsel juhul on reaktsiooni Gibbs’i energia muut kättesaadav kasuliku energiana, ehk:
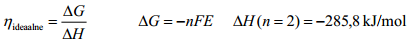
H2 ja O2 reageerimisel ideaalselt 83% (tegelikult tuleb arvestada reaalse rakupingega).
Head tööomadused madalal koormusel (vs. sisepõlemismootor)
Seismise hetkel (ka konstantse kiirusega sõites) energia tarbimise efektiivsus tunduvalt kõrgem kui sisepõlemismootoril. KEga elektrimootor jääb seisma, kui koha peal ollakse, sisepõlemismootoril aga vaja hoida pidevalt ~1200 pööret
Puhas, usaldusväärne ja praktiliselt saastevaba süsteem
Ainult juhul kui kütus on H2
Liikuvate detailide puudumise tõttu vaikne elektrienergia tootmine
Konstantne töötemperatuur , elektrokeemilise reaktsiooni soojus koostootmise rakenduseks
Lihtne ülesehitus
Moodulehitus, mis lihtsustab suuremahuliste süsteemide rakendamist
Tööomadused ja hind vähem suurusest sõltuvad kui teistel tehnoloogiatel
Väiksemahulised KEd töötavad praktiliselt sama efektiivsusega kui suured, võrdselt väikese saastehulga ning võrreldava hinnaga
Probleemid KE kasutamisega
Kütus (maagaas, õli, süsi) tuleb reformida vesinikuks – puuduvad piisavalt efektiivsed reformerid
Metanooli ja maagaasi jaoks olemas head reformerid
bensiini ja diisli reformereid arendatakse
Vaja ühildada reformer ja KE
Kineetiliste ja termiliste parameetrite ühildamine hea massi- ning soojusülekande saavutamiseks
Nii reformeri kui KE katalüsaatori mürgistus kütuse lisandite poolt (eriti väävel)
Vee regulatsioon – rakk ei tohi küllastuda ega kuivada
Ebapiisav eluiga ning usaldusväärsus
Vastuvõetamatu hind
Turu harjumatus KE tehnoloogiaga
Ioonjuhtivus KEdes
KEsid klassifitseeritakse elektrolüüdi ja kütuse alusel:
Erinevad elektroodi reaktsioonid
Erinev ioonide liik kannab laengut läbi elektrolüüdi – H+, O2–,OH–or CO3 2–
Kui elektrolüüdil/separaatoril H+ juhtivus, siis moodustub H2O vastavalt oksüdeerija poolel, kui anioon-juhtivus, siis kütuse elektroodil
Sarnaselt akudele toimub KEs keemilise energia muundamine elektriliseks
Erinevalt akudest on reageerivad ühendid (enamasti) gaasilised ning hoitakse ühikrakust väljaspool
Seadme energiahulk limiteeritud kättesaadava kütuse ja hapniku hulga mitte seadme ehituse poolt
KEsid hinnatakse pigem väljundvõimsuse (kW) kui energia (kWh) alusel
Kolme faasi piirpind
Mikroskoopiline piirkond KEs, kus tegelik elektrokeemiline reaktsioon aset leiab
Reaktsiooniks aktiivne punkt peab olema:
Reageerivale gaasile ligipääsetav
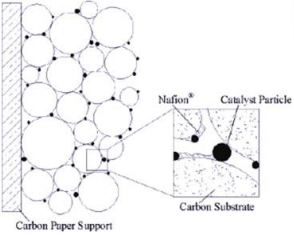 Elektrilises kontaktis elektroodiga
Elektrilises kontaktis elektroodiga
Ioonses kontaktis elektrolüüdiga
Kontaktis piisava koguse elektrokatalüsaatoriga, et reaktsioon toimuks kiiremini
Piirpindade tihedusel ja omadustel on kriitiline roll KEde toimimisel:
Vedel-elektrolüüt KEdes õhuke elektrolüüdi kiht märgab osaliselt poorset elektroodi. Liigse elektrolüüdi korral on reageerivate gaaside difusioon takistatud.
Tahke-elektrolüüt KEdes on keerulise disainiga süsteem, kus on palju katalüütilisi tsentreid ühenduses elektroodi ja elektrolüüdiga, lubades samas gaasi ligipääsu
2. KE elektroodide ja elektrolüüdi vajalikud omadused
KE elektroodid
Poorsete elektroodide ülesanded:
Pind elektrokeemiliste reaktsioonide toimumiseks
Katalüsaatori nanoosakeste kandja (kui vaja katalüsaatorit)
Keemilises reaktsiooniga seotud elektronide juhtimine 3 faasi piirpinnalt/-pinnale (hea elektronjuht-materjal)
Voolu kogumine ning elektriline ühendust teise ühikraku või koormusega
Reageerivate gaaside ühtlane jaotamine
Reaktsiooniproduktide efektiivne väljajuhtimine
Madal-T KEd: vaid mõned haruldased ja kallid materjalid omavad piisavat katalüütilist aktiivsust – sadestatakse piirpinnale nanoklastritena
Kõrg-T KEd: elektroodi materjali aktiivsus piisav
Elektroodi funktsioon – kanda reageeriv kütus/hapnik – transport. Elektronide juhtivus. Peab olema hea juhtivusega materjal. Poorne struktuur peab olema, et oleks võimalikult palju piirpindasid tekitada. Kontakt elektrolüüdiga. Oleneb millist liiki kütuseelement on.
KE elektrolüüt
Võimalikult õhuke kiht ja hea ioonjuht süsteemi sisetakistuse vähendamiseks
Vedela elektrolüüdiga KEd – elektrolüüt jaotunud maatriksis, mis katab kogu elektroodide pinda
PAFC (H3PO4), AFC (KOH), MCFC (sula Li ja K karbonaadid)
Maatriksis elektrolüüt tagab reageerivate gaaside teineteisest eraldatuse
PEMFC ja DMFC – õhuke polümeermembraan kõrge H+ juhtivusega
MCFC – keraamiline LiAlO2
SOFC – õhuke keraamiline mittepoorne membraan O2- või H+ juhtivusega kõrgel temperatuuril
Veebaasil elektrolüütidega süsteem limiteeritud <100 °C suure aururõhu ja kiire degradeerumise tõttu
Elektrolüüt: Võimalikult õhuke süsteemi sisetakistuse vähendamiseks. Mida suurem sisetakistus, seda väiksem võimsus. Ioonjuhtiv, mitte elektronjuhtiv. Kindlus, et kütuse ja hapniku transporti ei toimuks läbi elektrolüüdi faasi.
3. Kasutatavad kütused (sobivus eri liiki KE-dele, väline ja sisemine reformimine)
Üldiselt kasutatavad kütused: H2, metaan, butaan, CO
KE tüübid:
Madaltemperatuursed (50–150 °C):
Leelis KE (AFC) – puhas vesinik
Polümeer-elektrolüüt-membraan / prootonvahetus-membraan KE (PEMFC) - puhas vesinik
Otsene metanool KE (DMFC) - metanool
Kesktemperatuursed (~200 °C):
Fosforhappe KE (PAFC) - vesinik
Kõrgtemperatuursed (600–1000 °C):
Tahke-oksiid KE (SOFC) – vesinik, CO, metaan, valik süsivesinikkütuseid
Sulakarbonaat KE (MCFC) – vesinik, CO, valik süsivesinikkütuseid
KEde massiline rakendamine nõuaks laiaulatuslikku H2 võrgustikku
Kütuse reformimine
H2 tootmisprotsess (erinevate vesinikku sisaldavate kütuste lagundamine sisuliselt), millega kaasneb CO2 eraldumine.
Temp u 500 oC, Ni – katalüsaator
CnHm + nH2O = nCO + (m/2 + n)H2
CH4 + H2O = CO + 3H2
CO + H2O = CO2 + H2
CH3OH + H2O = 3H2 + CO2
Temp u 250 oC, Ni – katalüsaator
CH3OH + H2O = 3H2 + CO2
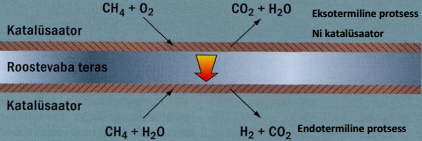
Kõrg-T KEdes sisemine reformija – termiline regulatsioon lihtsam välimisega
Madal-T KEdes ainult välimine reformija, kus töötemp. säilitamiseks osa kütusest tarbitakse, kütuse lahjenemine viib KE efektiivsuse alla
AFC ei saa töötada reformitud kütusel, sest sisaldab elektrolüüdi mürki CO2
Reformimine toimub veeauruga katalüsaatori (Ni) juuresolekul . Madaltemperatuurilistel nt maagaasil töötavatel KEdel on sellepärast vajalik eraldi seade (aurugeneraator) veeauru tootmiseks.
Madalametl temperatuuridel töötavad KE-d vajavad välist kütuse reformimist – kasutatavat kütust (maagaas vmt) kuumutatakse eelnevalt ning lastakse katalüsaatori juuresolekul (Ni) veeauruga reageerida u 800 kraadi juures.
Sisemine reformimine on võimalik eelkõige kõrgtemeratuursetes KEdes tänu nende kõrgele soojusegenereerimsiele (st kõrge töötemp). MCFC puhul on vajalik Ni-katalüsaatori olemasolu, kuna töötemperatuur on 650 kraadi juures. SOFCi puhul aga piisab ainult töötemperatuurist 1000 kraadi ning katalüsaatorit pole vaja. Reformimine toimubki põhimõtteliselt anoodil.
4. KE tegelik tööpinge vs. termodünaamiline rakupinge (polarisatsioonikõver, erinevad ülepinge
põhjused)
Tüüpiline polarisatsioonikõver ülepinge allikatega
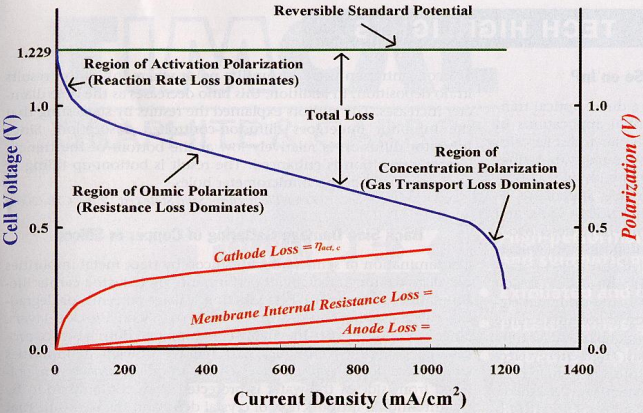
Ülepinge põhjused
Ülepinge – antud voolutihedusel toimuva reaktsiooni tegeliku rakupinge ja pöörduva termodünaamilise rakupinge erinevus
Potentsiaali muutused elektroodidel parasiitreaktsioonide tõttu
Reaktantide membraanist läbitungimine
Aktivatsiooni ülepinge
Aeglane reaktsiooni kineetika – eriti O2 redutseerumine
Sõltub katalüsaatori valikust ja mikrostruktuurist
Eriti märgatav voolutihedustel <100 mA/cm2
Oomiline pingelangus
Ioon-takistus elektrolüüdis (ja elektroodides)
Elektron-takistus elektroodides, voolukollektorites ja vahelülides
Kontakttakistused
Voolutihedusega proportsionaalneS
Sõltub materjalide valikust ja raku ülesehitusest ning temperatuurist
Kõige märgatavam efekt keskmistel voolutihedustel 100-500 mA/cm2
Kontsentratsiooni (massiülekande) ülepinge
Piiratud reaktantide massiülekanne elektroodi struktuuris
Sõltub voolutihedusest, reaktantide aktiivsusest ja elektroodi struktuurist
Kõige märgatavam efekt kõrgetel voolutihedustel > 500 mA/cm2
Ülepinge allikate kombinatsioon põhjustab süsteemi väljundpinge languse voolutiheduse kasvades. Väljundvõimsus (mW/cm2) sõltub rakupingest ja voolutugevusest – polarisatsioonikõver peab olema nii lame kui võimalik!
5. Millisteks rakendusteks ja millised KEd sobida võiksid? Milliseid takistusi esineb laialdasele rakendamisele/tootmisele?
| KE tüüp |
Tüüpiline elektrolüüt |
Rakendused |
Eelised |
Puudused |
| Polümeerelektrolüüt- Membraan (PEM) |
Perfluorosulfoon- Hape |
Väikese võimsusega elektro tootmine, Kaasaskantav energia, tagavara energiaallikas, Hajutatud tootmine, Transport, eritranspordivahendid |
Tahke elektrolüüt vähendab korrosiooni ja probleeme käsitlemiselm, madal T, quick start-up |
Kallis katalüsaator, Tundlik kütuse ebapuhtuste suhtes, low temp waste heat |
| Aluseline (AFC) |
KOH vesilahus soaked in matrix |
Sõjaväetehnikas Kosmoses |
Katoodne reaktsioon aluselises kk-s kiirem > suur jõudlus, Odavamad komponendid |
Kütuses ja õhus leiduva CO2 suhtes tundlik, elektrolüüdi käsitlemine |
| Fosforhape (PAFC) |
Fosforhape soaked in matrix |
Hajutatud tootmine, Elektri ja soojuse koostootmine |
Kõrgem T võimaldab CHP’d, suurem tolerants kütuse ebapuhtuse osas |
Pt katalüsaator, Pikk stardiaeg?, Madal vool ja võimsu, |
| Sulakarbonaat (MCFC) |
Li/Na/K-karbonaadid soaked in matrix |
Electric utility, Hajutatud tootmine, Elektri ja soojuse koostootmine |
Kõrge efektiivsus, Fuel flexibility, Katalüsaatoreid võib varieerida, Sobib CHP’le |
Kõrgetemperatuuriline korrosioon ja raku komponentide lagunemine, pikk stardiaeg, madal energiatihedus |
| TOKE |
Ütriumoksiidiga stabiliseeritud strontsiumoksiid (Y2O3-ZrO2) |
Electric utility, Hajutatud tootmine, Auxiliary power Elektri ja soojus koostootmine |
Kõrge efektiivsus, Fuel flexibility, Katalüsaatoreid võib varieerida, Tahke elektrolüüt, Sobib CHPle ja CHHPle, hübriid/GT tsükkel |
Kõrgetemperatuuriline korrosioon ja raku komponentide lagunemine, kõrge temperatuur vajab pikka stardiaega |
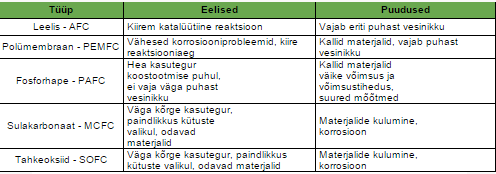
KEde rakendused
Statsionaarsed elektrijaamad (koostootmisjaamad)
Väiksemamahulised (300 kW kuni 2 MW) individuaalseks kasutuseks
Suurema mahuga (1-10 MW) hajutatud elektrienergia tootmise süsteemis
Eelkõige sõltumatu energiavaru olemasoluks nt haiglates, tööstuses, ettevõtetes, jne
Kütuseks maagaas või süsi (gaasistatud) või vesinik
Hinna optimeerimisel ning laiadasel kommertsialiseerimisel võiks KEsid rakendada ka baasvõimsuse tootmiseks nende suure efektiivsuse tõttu
Elektrisõidukite liikumapanev jõud (kütus)
Null-emissiooniga sõidukid H2 kütuse korral
Pardapealne elektrienergia kosmosesõidukitele, allveelaevadele jt suletud süsteemidele
Juba 1960ndatel demonstreeriti PEMFC ja AFC kasutamist kosmoseprogrammis
Portatiivsete elektrooniliste seadmete energiaallikas
6. Polümeer-elektrolüüt-membraan KE (põhimõte ning materjalid, eelised-puudused, rakendused)
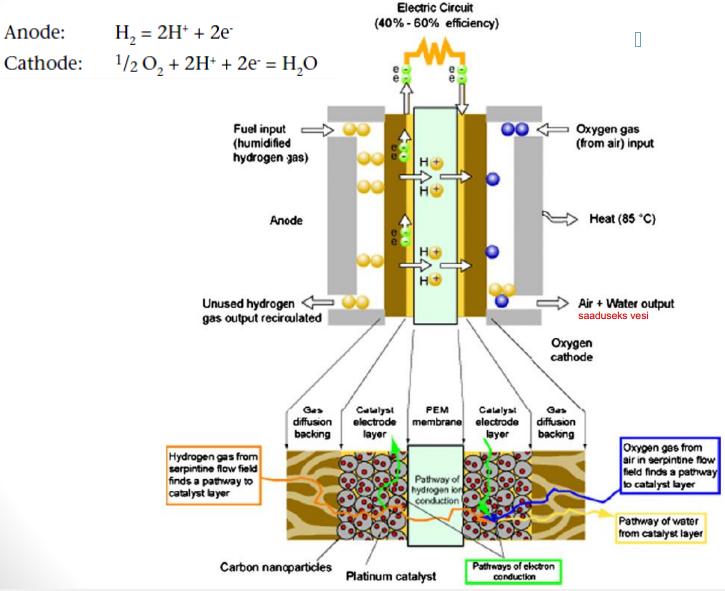
Loengus: Prootonite liikumine anoodilt katoodile; kui kasutatakse katalüsaatoreid, siis reaktsioon toimub katalüsaatori säästmiseks poorse struktuuri lähikihis; ka katoodil käib reaktsioon aktiivkihis, mis võimalikult elektrolüüdi lähedal; elektrolüüdi materjaliks on poorne membraan.
PEMFC koostisosad
Polümeer-membraan prootonjuhina (ionomeer)
Polymer electrolyte membrane / proton exchange membrane
Fluoreeritud sulfoonhappe polümeer või muu sarnane polümeer (Nafion®)
–SO3H rühmad võimaldavad H+ liikumist läbi materjali
Max juhtivuseks peab polümeer olema niisutatud (aga ei tohi olla ka liiga niiske), samas elektroodi pinna läheduses peab olema piisavalt kuiv gaaside takistuseta transpordiks
Minimaalne gaaside läbilaskvus
Loengus: H ei tohi sattud katoodiruumi, O ei tohi sattuda anoodiruumi > muidu kogu süsteemi efektiivsus väheneb
Anood ja katood – suure eripinnaga (et oleks võimalikult palju reaktsioonitsentreid) süsinik-materjal katalüsaatori (Pt – sellepärast kallis) nanoklastritega
Ionomeeri lisand sideainena ja H+juhtivuseks
Süsinikkandja – “ gaasi difusiooni kiht ”
Voolukollektor/vahelüli
Grafiidist või metallist
Gaasivoolu kanalitega
Reaktantide jäägi ja vee ärajuhtimine
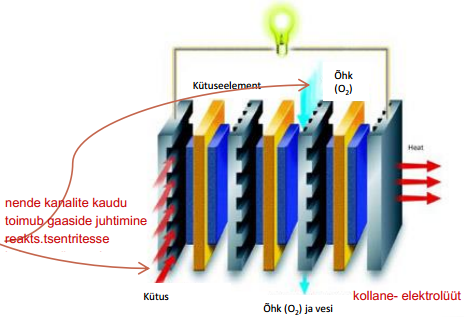
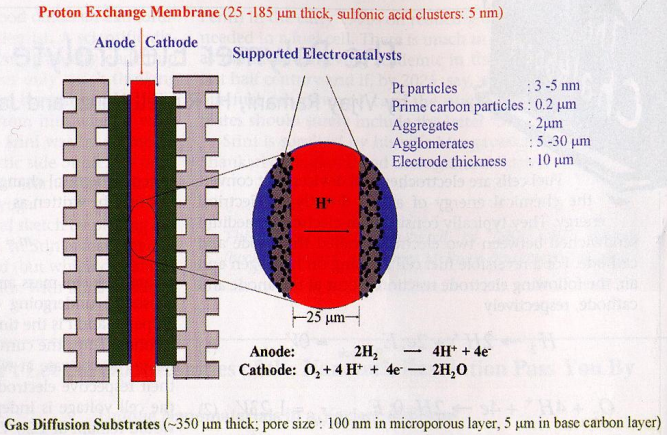
Loengus: Mida paksem membraan, seda suurem sisetakistus > soovitatakse võimalikult õhukest membraani
Eelised/puudused
Eelised:
Madal töötemp. – kiire käivitamine (start-up)
Tahke membraan-elektrolüüt – hea takistus gaasi ülekandele
Korrosiooni probleem väike (vesi ainuke vedelik)
Suur võimsus (mitme ühikraku kokkupanek võimalik > võimalik võimsust varieerida)
Lihtne skaleerida (ühikrakkude ühendamine, elektroodide mõõtmete muutmine)
Puudused:
Madal ja kitsas töötemp. vahemik – keeruline termiline regulatsioon (eriti kõrgel voolutihedusel) ja jääksoojuse kasutamine
Vee regulatsioon – membraani niisutamine vs. Üleujutamine
Aktiivse katalüsaatori (Pt) vajadus vs. kõrg-temp KE
Aeglane O2 redutseerumise reaktsioon
Kallis membraan
Väga tundlik kütuse lisandite suhtes (CO, S jne)
PEMFC kommertsialiseerimise takistused
Vastupidavus
Keemiline rünnak membraanile – katoodireaktsiooni kõrvalprodukt H2O2 põhjustab õhenemist, gaasi lekkimist läbi membraani, lühistumist
Katalüsaatori mahapudenemine elektroodilt
Katalüsaatori tundlikkus (CO <10 ppm)
Adsorbeerunud CO eemaldamine – kiirust limiteeriv
Lihtsustatud CO oksüdeerimine adsorbeerunud OH abil (Ru katalüsaatoril madal potentsiaal OH-ads moodustumiseks)
Hind
Katalüsaatori osakeste suuruse vähendamine ja homogeensem jaotamine
Uued katalüsaatorid – nt Pt-sulamid, mitte-väärismetallid
Uued sulfoneeritud süsivesinikud ja happega dopeeritud polümeerid
Soojenemine ebaefektiivsuste tõttu – peamiselt aeglane O2 redutseerumine
PEMFC membraan
Membraani omadused optimeerimiseks:
Prootonjuhtivus – sõltub sulfoneerimise ulatusest ja membraani paksusest
Mehaaniline, keemiline ja termiline vastupidavus (sobiva süsinik-peaahela valimine)
Tugevdavad lisandid
Gaasi läbilaskvus – sõltub materjalist endast ning membraani paksusest
Sisetakistus minimaalne õhukese kihi korral
NafionTM
Kallis (~780 $/m2)
Kõrge O2 läbilaskvus
Limiteeritud töötemp (T < 80 oC)
CH3OH, CH4 läbilaskvus (sõltub T)
Polüstüreen ja divinüülbenseen sulfoon-gruppidega
H3PO4-ga modifitseeritud polümeerid
H-soolasid (CsHSO4, NaH2PO4) sisaldavad polümeerid
Rakendused:
Back-up energia
Kaasaskantav energia
Elektri hajutatud genereerimisel
Sõidukites
7. Otsene metanool-KE (DMFC) (põhimõte ning materjalid, eelised-puudused, võimalikud rakendused)
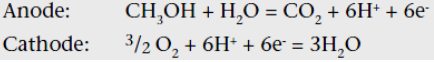
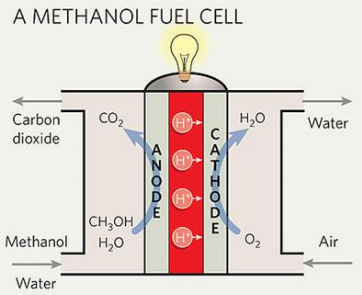
Loengus: samamoodi toimub prootonite juhtimine, aga anoodi suunas toimub metanooli liikumine
Modifitseeritud PEMFC, mis kasutab kütusena metanooli
Vedel kütus vs gaasiline – MeOH oluliselt lihtsam transport ja hoiustamine
Väike MeOH molekul käitub H2O-le sarnaselt – tungib läbi kasutatavate membraani materjalide
Kütuse kadu
Madal rakupinge (0.25-0.4 V):
Pingekadu segapotentsiaali tõttu O2-elektroodil (toimub ka kütuse redutseerimine)
MeOH laguproduktide (nt CO) adsorptsioon elektroodidel
CO-taluva katalüsaatori vajadus veel suurem vs PEMFC (katalüsaator ei tohi Coga reageerida)
Pt katalüsaatorit vaja 10x rohkem (3-5 mg/cm2) vs PEMFC
Sihtmärk parema T-taluvusega membraan:
Kõrgemal töötemp. CO tundlikkus väheneb
>100 °C – H+ juhtivuse parandamises ei saa vesi osaledaM
MeOH ülekande vähendamiseks vajalik madala elektro-osmootse ülekandekoefitsiendiga materjal
Materjalid on üldiselt samad, mis PEMFC-l:
Elektroodid: katalüütiline kiht koosneb süsiniku nanoosakestest, katalüsaatorist (Pt) ionomeerist, et oleks nii elektron- kui ka ioonjuhtivus; gaasi difusioonikiht koosneb süsinikust ja teflonist üldiselt, peab olema hüdrofoobne materjali O2 ja CO2 ärastamiseks elektroodidelt (vastavalt katoodilt ja anoodilt)
Membraan: nt perfluorosulfoonhappe polümeer.
Eelised: Pole vaja kütuse reformimist, hea energia ja võimsustihedus
Puudused: MeOH toksilisus, Madal efektiivsus
Rakendused mikrokütuseelementidena elektroonilistes seadmetes (nt mobiiltelefonid)
8. Leelis- KE (AFC) (põhimõte ning materjalid, eelised-puudused, rakendused)
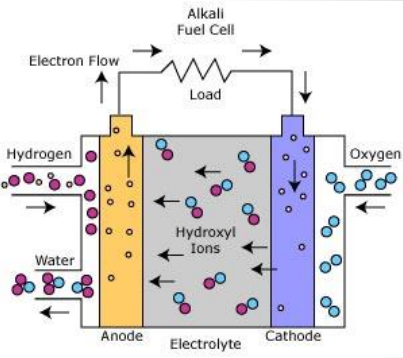

Elektrolüüt: Konts. KOH (85 %) töötemp. ~250 °C
Elektrolüüt paikneb tahkes maatriksis (asbest)
KOH – kõrgeima juhtivusega leelistest
Anoodil olevad katalüsaatorid: Ni, teras, Pt-Pd
Katoodil olevad katalüsaatorid: NiO, Ag, Au-Pt
Kütus: puhas H2
CO endiselt katalüsaatori mürk
CO2 reageerib KOH-ga, moodustades K2CO3
Vähenenud OH konts. – mõjutab kineetikat
Elektrolüüdi viskoossus kasvab (difusioon ja juhtivus)
Sadenemine poorses elektroodis – vähenenud massitransport
Väheneb O2 lahustuvus
Eelised/puudused:
Eelised:
Kiirem O2 redutseerumine aluselises keskkonnas
Kõrgema töötemp tõttu laiem katalüsaatorite valik (Ni, Ag, metalloksiidid ja väärismetallid)
Puudused:
CO2 tundlikkuse tõttu vajalik ülipuhas H2
Väga efektiivse CO ja CO2 eemaldamise süsteemiga reformer või elektrolüüsitud H2
Õhu kasutamisel oksüdeerijana, tuleb ka sealt CO2 eemaldada
Tehniliselt lihtne – aga süsteemi suurus/hind
Edukalt kasutatud kosmoserakendustes
9. Fosforhappe- KE (PAFC) (põhimõte ning materjalid, eelised-puudused, rakendused)
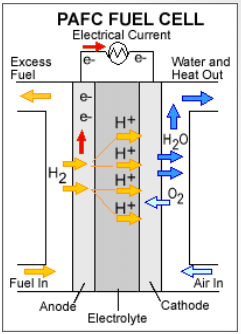
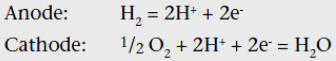
Põhimõte: elektrolüüdiks 100% fosforhape, elektrolüüt fikseeritud ränikarbiidi maatriksis. töötemperatuur 150-220C, katalüsaatoriks Pt, kütuseks H2 (võib olla madal S, CO sisaldus, tolerantne CO2 suhtes).
Esimene KE, mis oli kättesaadav tavakasutajale
100% H3PO4 elektrolüüt > lekke-probleem, selle vastu aitab SiC
Elektrolüüt enamasti fikseeritud ränikarbiidist (SiC) maatriksis
Elektroodideks Tefloniga seotud Pt katalüsaatoriga süsinik
Töötemp. ~150-220 °C (keskmise T-ga KE)
H3PO4 hea ioonjuhtivus
Pt-katalüsaatori CO-tundlikkus väiksem
Eelised/puudused:
Eelised:Pikaajaline stabiilsus
Konts. H3PO4 (100%) – kõrgem töötemp.
Elektrolüüdi madal lenduvus
Vee regulatsioon lihtsam
CO-taluvus < 1 wt% (vs. PEM)
Laiem kütuste valik
Lihtsam termiline regulatsioon
Jääksoojus koostootmiseks
Puudused:
H3PO4 – korrosioon
O2 aeglane kineetika vs. AFC (vaja Pt)
Kütuse puhastamine
Vesinikku toodetakse maagaasist või metanoolist väljaspool kütuseelementi asetsevas reformeris. Oksüdeerijaks on õhk. Kõige enam arendatud tehnoloogia statsionaarsete seadmete kasutamise jaoks (praegusel ajal). Kuni 200 kraadise töötemp-i tõttu sobilik kasutada elektrienergia ja soojuse koostootmiseks.
10. Sulakarbonaat- KE (MCFC) (põhimõte ning materjalid, eelised-puudused, rakendused)
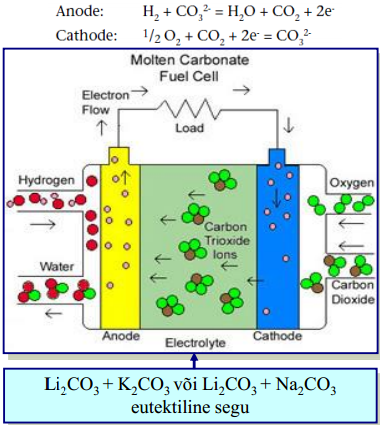
Töötemp 600-700 °C
Elektrolüüt – sulakarbonaadid keraamilises LiAlO2 maatriksis
Korrosiooni probleemid (võivad lekkida)
Ni-Cr või Ni-Al anood, NiO (Li-dopeeritud) katood
Jahutamine inertgaasi atmosfääris, et vältida anoodi oksüdeerumist
Kiletõmbamise (tape-casting) meetod võimaldab valmistada elektrolüüdi maatriksit mõõtmetes kuni 1 m2
Suhteliselt madal võimsustihedus nõuab suurt pindala
Fookus suuremahulistel statsionaarsetel ning merelaevastiku rakendustel, kus süsteemi kaal ning aeglane käivitumine pole niivõrd olulised
Eelised/puudused
Eelised:
Elektroodide materjal piisava aktiivsusega oks-red reaktsioonide kulgemiseks
CO ja süsivesinikud on kütus
Raku sees reaktsioon H2-ks
Jääksoojusest koostootmine
Puudused:
Agressiivne Li2/Na2/K2CO3 elektrolüüt (lekkimisprobleemid)
Kallid ümbris/vahelüli materjalid (Ni ja kõrgkvaliteetne roostevaba teras)
CO2 regulatsioon
Tekib anoodil ja tarbitakse katoodil
Elektrolüüdi maatriks peab vastu 3-5 jahutamise tsüklit
T tuleb hoida üle tahkumise temp. ka stand-by seisus
Kütuseks gaaside H2, CO ja CO2 segu, mis saadakse maagaasi või ka kivisöe reformimisel. Sobib elektri ja soojuse koostootmiseks.
11. Tahkeoksiid- KE (SOFC) (põhimõte ning materjalid, eelised-puudused, rakendused)
Kuna siin on materjalide poolest tegu keraamikaga, siis purunemisohu tõttu sõidukitele ei sobi.
KE liik, milles kõik funktsionaalsed elemendid on tahkes faasis
Elektroodid on poorsed kompleksoksiidid ning elektrolüüt tihe oksiidne kiht
KE summaarne elektroodide protsess eksotermiline – soojust ära juhtida
Suure koormusega ülekuumenemine
Sisetakistuse ja voolu mõjul
Kütuse reformimine endotermiline – KEst saadava soojuse abil
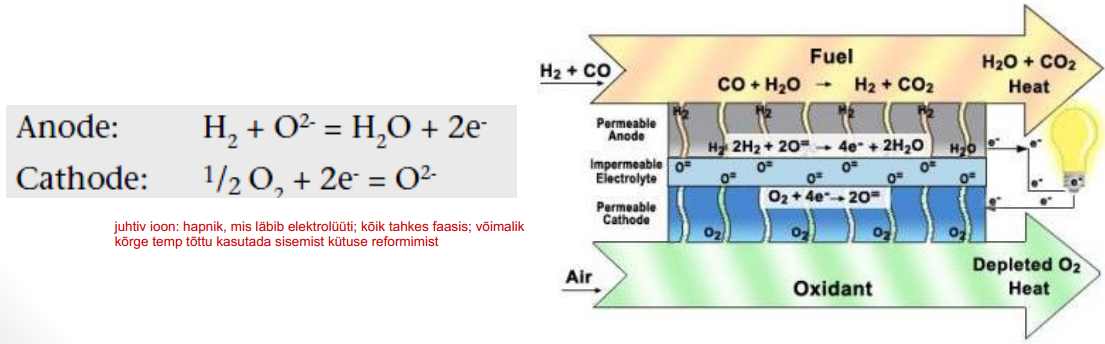
SOFC elektrolüüt
Tahke mittepoorne metalloksiid
O2-(või H+) juhtiv kompleksoksiid (hapnikjuhtivaid väga vähe)
Tihe materjal (gaaside ülekandeta)
Võimalikult õhuke (sisetakistus)
Õhuke (~40 μm) tihe kiht sünteesitakse otse poorsele elektroodile
Parim meetod elektrokeemiline aursadestus (EVD) – saadakse puhas ning väga tihe kiht (kasutatakse ka sukeldamist, pihustamist ja lamineerimist-paagutamist (kilega)
Alternatiivideks:
Pihustuskatmine
Sukelduskatmine
Lamineerimine järgneva paagutamisega
Nanoosakeste (5-10 nm) suspensiooniga kaetakse õhukeste (20 μm) kihtidena
Osakeste suuruste jaotus ja dispergeerumine pastas olulised faktorid
Levinuim ütrium-stabiliseeritud tsirkooniumoksiid (YSZ)
Y2O3 lisand stabiliseerib ZrO2 kuubilise struktuuri kõrgel töötemperatuuril ning tekitab O-vakantse
Tüüpiliselt 10 mol% Y2O3
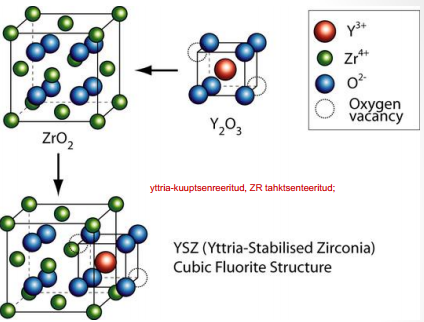
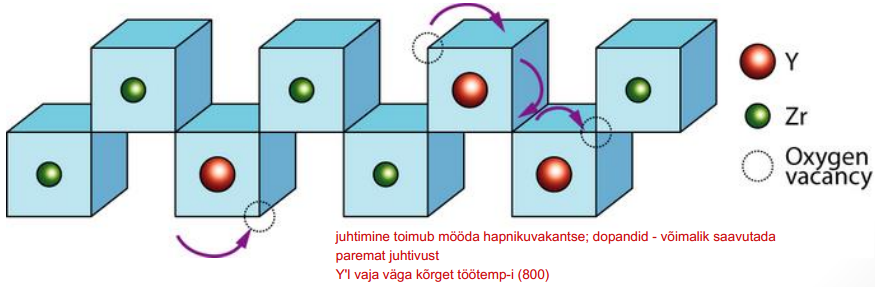
CeO2 samuti uuritud elektrolüüt (dopeeritud nt Gd-ga) (kõrgematel T-del suuremad juhtivused)
Eelised:
Kõrge ioonjuhtivus
Efektiivne madalamal T (<700 °C)
Laiem valik (odavamaid) materjale teiste komponentide jaoks
Puudused:
Kipub redutseeruma kütuse poolel
Madalamal töötemp. (500-700 °C) suur osakeste piirpinna takistus ioonjuhtivusele
SOFC elektroodid
Anood: Ni/kompleksoksiid (uuritud ka Co, Fe, grafiit)
Hea elektrijuhtivuse tõttu on metallid atraktiivsed anoodi materjalid
Ni kasutamise probleemid:
Soojuspaisumine liiga kõrge, et kombineerida elektrolüüdiga
-> Ni-YSZ komposiitanood (või muu oksiidiga)
Kipub töötemp.-l agregeeruma ja sulgema poorsust
Katalüüsib grafiidi moodustumist süsivesinikest
Sadenenud grafiit vähendab elektroodi efektiivsust
Kaob SOFCi põhiline eelis – lai kütuste valik
Katood: LaMnO3 või LaCoO3 (perovskiit tüüpi*) dopeeritud haruldase muldmetalliga (nt Sr, Ce, Pr) juhtivuse parandamiseks
Keemiline vastupidavus oksüdeerivas keskkonnas
Eelised/puudused
Eelised:
Tahke elektrolüüdiga täpsem kolme faasi piirpinna kontroll
Elektrolüüt ei ujuta elektroode
Kiire kineetika
Pole ülikalleid katalüsaatoreid
CO on kütus
Puudused:
Paisumiskoefitsientide ühildamine
Piiratud materjalide valik kõrgel T töötamiseks
Raske saada kõiki kihte õhukesi – takistus!
Detailide valmistamise keerukus
12. Kõrg-temperatuursete KE-de eelised-puudused vs. madal-temperatuursed KE-d
Madaltemperatuursed (50–150 °C):
Leelis KE (AFC)
Polümeer-elektrolüüt-membraan prootonvahetus - membraan KE (PEMFC)
Otsene metanool KE (DMFC)
Kesktemperatuursed (~200 °C):
Phosphoric acid (PAFC)
Madal- ja kesktemperatuursetel on tarvilik kütuse välise reformeri olemasolu.
Tundlikud kütuse ebapuhtuse suhtes.
Kiire käivitusaeg
Kõrgtemperatuursed (600–1000 °C):
Tahke-oksiid KE (SOFC)
Sulakarbonaat KE (MCFC).
Aktivatsiooni ülepinge probleem väiksem.
Massiülekande pingekaod olulisemad ja märgatavad juba madalamatel voolutihedustel. Pingekaod suurenevad.
Kütuse lisandite mõju väiksem.
Summaarne energeetiline efektiivsus kasvab, kui jääksoojus ära kasutada.
KE töötab kombineeritud elektri-soojus tootjana.
Eelised: lai kütuste valik. Ei vaja kallist katalüsaatorit. Lihtsam aktivatsioon. Efektiivsus kõrgem. Soojus-elektri koostootmine.
Puudused: materjalide vastupidavus. Töötavad detailide vastupidavus. Keraamiline materjal võib praguneda ja hävineda. Aeglane käivitumine. Aeglasem reageerimine koormusemuudatusele. Kõrgtemperatuursuse tõttu ei sobi sõidukitele
Kokkuvõtvalt:
PEMFC – polümeer-elektrolüüt-membraan KE

DMFC – otsene metanool-KE

AFC – leelis-KE

PAFC – fosforhappe KE

MCFC – sula-karbonaat KE

SOFC – tahke-oksiid KE

Loeng 4. Polümeermaterjalid
1. Polümeeri nanofiibrite valmistamise meetodid (tõmbamine, maatriks-süntees, faasi-eraldus, isekorrastumine)
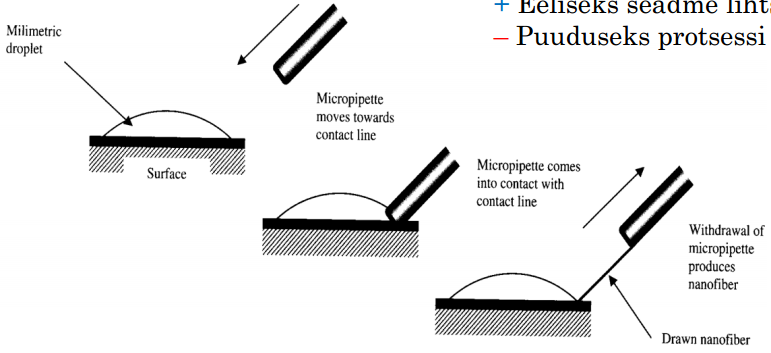
NANOFIIBRI TÕMBAMINE
Fiiber tõmmatakse polümeerilahuse tilgast
Mõne μm diameetriga mikropipett kastetakse tilga sisse aluspinnaga kontaktpunkti läheduses
Pipett eemaldatakse tilgast ~0,1 mm/s kiirusega, tõmmatakse nanofiiber
Vajalik viskoelastne materjal, milles on tugev kohesioon, et pidada vastu tugevale deformatsioonile
Lahuse viskoossus on väga oluline parameeter (kui on liga viskoosne: fiiber katkeb tõmbamisprotsessi käigus)
Eelis: seadme lihtsus
Puudus: protsessi mittepidevus
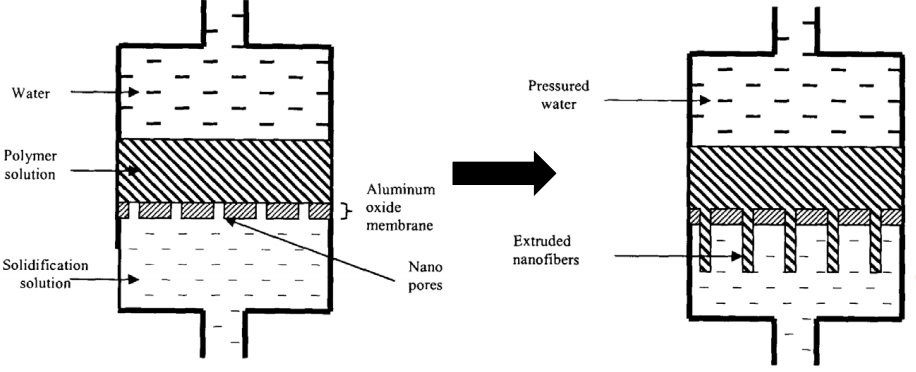
MAATRIKS-SÜNTEES
Kindla mõõtmega nanofiibrite saamiseks kasutatakse maatriks-struktuuri
Nanopoorne membraan (nt Al2O3)
Polümeeri lahus (nt polüakrülonitriil (PAN) dimetüülformamiidis) surutakse rõhuga membraanist läbi
Fiibrid sisenevad tahkendavasse lahusesse teisel pool
Keskkond, kus vastav polümeer ei ole lahustuv
Fiibri diameeter määratud membraani pooride suurusega
d lihtne varieerida (vahetame Al-membraane; pooride suurus mõjutab lõpliku diameetrit)
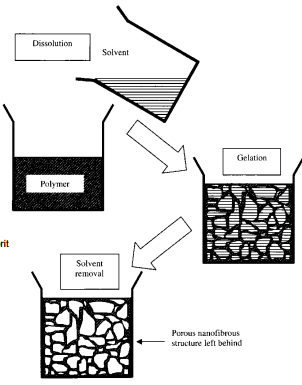 FAASI-ERALDUS MEETOD
FAASI-ERALDUS MEETOD
Mehhanism – faaside eraldumine füüsikalise sobimatuse abil
Polümeer segatakse solvendiga kõrgel T (nt polüpiimhape* tetrahüdrofuraanis)
Jahutatakse geeli moodustumise T-ni (faasid eralduvad) – oleneb polümeeri konts.-st
Solvendi vahetus ja eemaldamine
Polümeeri faas külm-kuivatatakse**
Eelised:
Minimaalne seadmestik
Saadakse otse nanofiibrite maatriks (enam ei saa üksikut fiibrit)
Suhteliselt hea reprodutseeritavus
Mehaaniliste omaduste kontroll läbi polümeeri konts.-ni
Puudused:
Teostatav valitud polümeeridega
* Ehk 2-hüdroksüpropaanhape on biodegradeeruv polümeer – looduslikult lagunevad kilekotid
** Külm-kuivatamine (freeze-drying) – materjal külmutatakse, alandatakse ümbritsevat rõhku, et külmunud solvent sublimeeruks
ISEKORRASTUMISE MEHHANISM
Toimub nanofiibrite spontaanne moodustumine väiksematest molekulidest
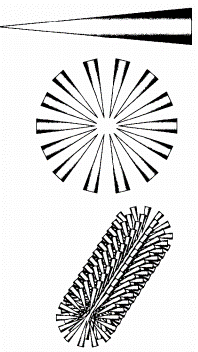 Molekulid korrastuvad kontsentriliselt (ühe keskpunktiga) molekulidevaheliste jõudude abil (van der Waals, elektrostaatiline, hüdrofoobsed interaktsioonid, vesiniksidemed, jne)
Molekulid korrastuvad kontsentriliselt (ühe keskpunktiga) molekulidevaheliste jõudude abil (van der Waals, elektrostaatiline, hüdrofoobsed interaktsioonid, vesiniksidemed, jne)
Pikitelg moodustub fiibri kasvamisel pinnanormaali suunas
Koostismolekulide kuju määrab fiibri kujuE
Eelised:
Hea meetod väikeste fiibrite saamiseks
Puudused:
Keeruline protsess
Raskesti reprodutseeritav (ei saa tootmist väga mõjutada)
2. Elektrospinning polümeeri nanofiibrite valmistamiseks (meetodi kirjeldus, süsteemi arameetrite mõju fiibri omadustele)
Meetodi kirjeldus:
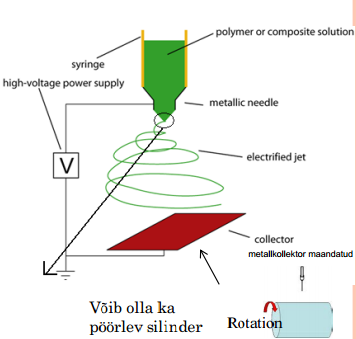 Kasutatakse elektrilist välja polümeeri lahuse pindpinevuse ületamiseks
Kasutatakse elektrilist välja polümeeri lahuse pindpinevuse ületamiseks
3 komponenti:
Pingeallikas
Nõelaga kapillaartoru
Metall kollektorplaat
Rakendatud pinge tekitab polümeerilahuse (või sula polümeeri) laetud joa väljumise nõelast
Üks elektrood polümeeri lahuses (või kinnitatud metallkapillaari/nõela külge) ja teine ühendatud kollektoriga (kollektor võib olla metall plaat, pöörlev trummel, peenikestest traatidest koosnev võrgustik > sõltub sellest, milliseid nanofiibreid tahame saada
Kui lahuses laenguhulk ületab kriitilise piiri, väljub polümeeri juga nõela otsast ja moodustub nn „Taylor’i koonus“, millest tekib polümeeri niit
Solvent aurustub enne kollektorini jõudmist ja tekib tahke fiibri võrgustik
Olulised parameetrid:
Sobiv solvent – peab lahustama täielikult polümeeri
Solvendi aururõhk – piisavalt kiire aurustumine fiibri kuju säilitamiseks kollektorile jõudes, samas mitte liiga kiire, et tahkuks liiga paks fiiber (kui aurustub liiga kiirelt, siis ei anna talle võimalust peenemaks muutuda
Solvendi viskoossus ja pindpinevus – liiga suure korral polümeerijoa moodustumine takistatud, liiga väikse korral lahus tilgub
Pindpinevus võib põhjustada tilkade tekkimist piki fiibrit (pindpinevus võib põhjustada sõlmede teket piki fiibrit (üritab polümeeri kokku tõmmata))
Polümeeri konts. suurendamine põhjustab viskoossuse suurenemist ja pindpinevuse vähenemist
Pindaktiivsete ühendite lisamisel saab tilga-vabasid nanofiibreid
Rakendatav pinge – sobiv viskoossuse ja pindpinevuse ületamiseks ning pideva joa säilitamiseks
Pipeti ja kollektori vahekaugus – mitte nii väike, et tekiks säde elektroodide vahel, kuid piisav solvendi aurustumiseks; mõjutab kaua fiibrit venitatakse ja kaua on solvendil aega aurustuda enne kollektorini jõdmist
Mida kõrgev spinnitava lahuse kontsentratsioon, seda kõrgem fiibri diameeter
Kui lahuse kontsentratsioon liiga madal, siis ei teki fiibreid > viskoossus liiga madal polümeerid ei sõlmu, vaid katkevad > tilgad
Nõela sisediameeter – määrab, kui suur on juga, mis tekib ja seega, kui suure diameetriga fiibrid saame
Erinevad liigid:
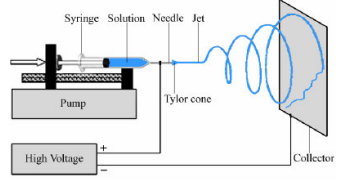 Horisontaalne elektroforeerimine
Horisontaalne elektroforeerimine
Polümeeritilgad võivad joaga väljuda, aga gravitatsiooni mõjul ei jõua enamasti kollektorini
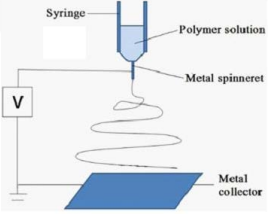 Vertikaalne elektroforeerimine
Vertikaalne elektroforeerimine
Suht sama horisontaalsega
Kui teeme vertikaalset ja peaks olema olukord, kus koonus ja juga pole väga stabiilne, siis võib ka vahepeal tulla polümeeritilku ja need võivad jõuda ka kollektorini ja proovini; siin paremini proov jaotunud, kui horison-l
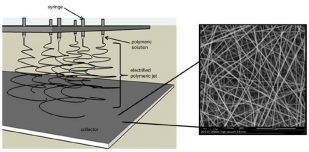 Mitme nõelaga elektroforeerimine
Mitme nõelaga elektroforeerimine
Tootlikkus suurem > paralleelprotsesse rohkem
 Nõelavaba elektroforeerimine
Nõelavaba elektroforeerimine
pole nõela, on silinder/ketas, mis kastetud polümeerlahuse vanni, mis keerleb, kettal pidevalt õhuke polõmeerikiht; fiibreid ja jugasid hakkab ülespoole nihkuma; parem kui nõelaga, sest nõelal 1 juga, mis pidevalt ketrab, siin paral mitmed joad - tootlikkus suurem
SULA ELEKTROFORMEERIMINE
Sula elektroformeerimisel kasutatakse sulatatud polümeeri mitte polümeerilahust
Parameetrid, mis mõjutavad protsessi on samad kui polümeeri lahuse elektroformeerimise korral
Polümeeri viskoossus sõltub otseselt temperatuurist
Vajalik pidev polümeeri anuma kuumutamine, et hoida polümeer vedelal kujul
Nõela ja kollektori vahekaugus on märksa väiksem (2cm)
Kokkuvõttev tabel
| Meetod |
Tehnoloogia areng |
Reprodutseeritavus |
Lihtne läbi viia? |
Fiibri mõõtmete kontroll |
| Tõmbamine |
Laboratoorne |
Jah |
Jah |
ei |
| Maatriks |
Laboratoorne |
Jah |
Jah |
Jah |
| Faasieraldus |
Laboratoorne |
Jah |
Jah |
Ei |
| Isekorrastumine |
Laboratoorne |
Jah |
Ei |
Ei |
| Elektroforeerimine |
Laboratoorne/ tööstuslik |
Jah |
Jah |
Jah |
3. Ioonjuhtivate membraanide valmistamine dopeerimise teel
Keemiline dopeerimine
Töödeldakse polümeeri kas oksüdeerija või redutseerijaga. Oksüdeerijaks sobib I2 või Br2. Redutseerijaks mingi leelismetalli katioon.
p-dopeerimine - oksüdeerija võtab elektroni konjugeeritud süsinik ahelalt ära. (Tekib elektronstruktuuris auk, kuhu on teistel elektronidel hea hüpata)
n-dopeerimine – redutseerija annab elektroni konjugeeritud süsinik ahelale juurde (tavaliselt seda ei kasutada, sest hapnik õhust reageerib n-dopeeritud materjaliga võttes selle elektroni uuesti ära).
Keemilise dopeerimise negatiivsed aspektid:
Keeruline kontrollide dopeerimise ulatust
Ajaline elektrijuhtivuse vähenemine (vastasiooni keemiline reaktsioon polümeeri ahelaga)
Elektrokeemiline dopeerimine
Tööelektroodi peale on kantud polümeer. Kui sukeldada see lahusesse ja tekitada potentsiaalide erinevus tööelektroodi ning teiste elektroodide vahel, siis hakkavad teatud ioonid (olenevalt elektroodist kas + või -) liikuma tööelektroodile. See tekitab samuti n ja p dopeerimist.
Eelised lihtsalt keemilise dopeerimise ees:
Tekkivad polümeerid on stabiilsemad.
Võimalik palju kergemini kontrollida dopeerimise ulatust (suure tõenäosusega tööelektroodi potentsiaali kaudu).
Kergesti pööratav protsess (muudad tööelektroodi potentsiaali märki suure tõenäosusega)
4. Juhtivad polümeerid (kirjeldus, näited, keemiline ja elektrokeemiline dopeerimine, SK-tes rakendamine)
Kirjeldus:
Polümeerid on materjalid, mis koosnevad paljudest korduvatest struktuurilülidest ehk monomeeridest
Üldiselt isolaatorid – ei juhi elektrit ega soojust
Konjugeeritud kaksiksidemeid sisaldavates polümeerides esineb juhtivus (enamasti pooljuht-materjalid)
Juhtivust on suhteliselt lihtne muuta nii polümeeri sünteesi järgus kui ka valmis struktuuris, muutes juhtivuse isegi metalliliseks.
Konjugeeritud kaksiksidemed: üksik- ja kaksiksidemete vaheldumine ahelas, milles tekib elektronide delokalisatsioon
Delokaliseeritud elektronid ei kuulu kindlale sidemele või aatomile, vaid pigem aatomite grupile ning on väga liikuvad
Atraktiivne kombinatsioon juhtivusest ja mehaanilistest omadustest (painduvus, kõvadus, elastsus, töödeldavus)
Näiteid:

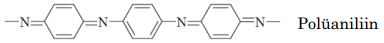
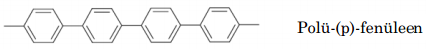
Keemiline ja elektrokeemiline dopeerimine
Konjugeeritud polümeerides mõõdukas juhtivus ~10-10 –10-8 S/cm
Materjali „dopeerides“ (osaline oksüdeerimine/redutseerimine) kasvab elektronjuhtivus mitu suurusjärku (isegi <1% korral)
Osaline oksüdeerimine ehk p-dopeerimine (elektron-vaene) – elektronide eemaldamisega tekitatakse positiivselt laetud korduv lüli
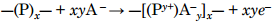
Nt jood-dopeeritud polüatsetüleen – konjugeeritud C-ahel + laenguga, laengut kompenseerivad I– ioonid
Osaline redutseerimine ehk n-dopeerimine (elektron-rikas) – elektronide lisamisega tekitatakse negatiivselt laetud korduv lüli
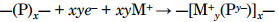
Nt Na-dopeeritud polüatsetüleen
Keemiline dopeerimine
Polümeeri töötlemine oksüdeerijaga (I2, Br2, jne) või redutseerijaga (tüüpiliselt sisaldab leelismetallikatioone)
Keeruline kontrollida dopeerimise ulatust
Ajaline elektrijuhtivuse vähenemine, vastasiooni keemiline reaktsioon polümeeri ahelaga
Hapniku keskkond kahjustav eelkõige n-dopeeritud polümeeridele, sest õhuhapnik oksüdeerib negatiivse ahela
Elektokeemiline dopeerimine
Polümeeriga kaetud tööelektrood sukeldatakse elektrolüüti (milles polümeer ei lahustu) koos abi- ja võrdluselektroodidega
Elektroodide vahel tekitatakse elektriline potentsiaalide erinevus – põhjustab elektroodil laengu ning lahusest vastasioonide sisenemise polümeeri (n- või p- dopeerimise kujul)
Stabiilsemad polümeerid – pole keemilist reaktsiooni vastasioonidega
Väga kerge kontrollida dopeerimise ulatust
Kergesti tagasipööratav protsess
SK-tes rakendamine
Superkondensaatorid:
Separaator materjali kõrge eripind – väiksem takistus ioonide massitrantspordile läbi separaatori
5. Erinevad komposiit-nanofiibrid (nanotorudega, metallide nanoosakestega), milleks kasulikud?
KOMPOSIITMATERJALID
Erinevad nanoosakesed (täiteaine) paiknevad polümeeri maatriksis või polümeeri fiibrite pinnal
Täiteaine lisatakse polümeerile selleks, et:
Vähendada hinda
Mehaanilisi omadusi parandada (nt carbon black, süsinikfiibrid, klaasfiibrid)
Täiteaine osakeste suurus peaks olema väiksem polümeeriahelate vahekaugusest lokaalsete pingete vältimiseks materjalis
KOMPOSIIT-NANOFIIBRID
Elastomeerides täiteosakesed <1 μm omavad märgatavat efekti tugevdamisel.
Osakesed >10 μm tüüpiliselt halvendavad mehaanilisi omadusi
Tugevdamise efekt parem kui:
Suurem eripind
Suurem fiibrite pikkuse ja diameetri suhe
Täiteaine ja polümeeri sobivus hea (sobiv pinnatöötlus)
Komposiit-fiibreid valmistatakse tavapäraste meetoditega, dispergeerides täiteaine nanoosakesed homogeenselt polümeerilahuses või sünteesides osakesed valmis polümeerfiibrite pinnale.
SÜSINIKNANOTORUD NANOFIIBRITES
CNTsid ja teisi süsinikmaterjale uuritakse põhjalikult omaduste parandamiseks tugevdavate lisanditena polümeerkomposiitides
CNTde ainulaadsus:
Tugevaimad fiibrid (>100 korda terasest tugevam)
Väga painduvad
Kerged (1.33–1.40 g/cm3)
Soojusjuhid
Elektronjuhid
Nt lisades ainult 5% ainet kahaneb takistus u 4 suurusjärgu võrra (juhtivuse tohutu kasv)
Nanofiibrite mehaaniliste omaduste optimeerimisel tähele panna:
Homogeenne CNTde dispersioon polümeerilahuses enne fiibrite valmistamist
Üksikute CNTde piki-orienteeritus
CNTd aglomeerunud kimpudeks – tuleb kulutada palju energiat nende eraldamiseks teineteisest:
Mehaaniliselt või ultraheliga pindaktiivsete ainete (Na-dodetsüülsulfaat) või dispergeerivate ühtendite (amfifiilne* kopolümeer, mõned polüimiidid) lisamisel
Pinna modifitseerimine (nt 6 M HNO3 keskkonnas ultraheli-töötlus – karboksüülrühmadega pinna modifitseerimine)
CNTde joondumine suurendab tõmbetugevust ja elektronjuhtivust
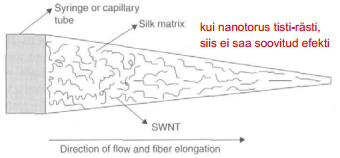
METALL-NANOFIIBER KOMPOSIIDID
Potentsiaalsed kasutusalad:
Katalüüs
Sensorid
Elektroonsed rakendused
Valmistatakse nanoosakestega polümeerilahuse otsesel elektrospinningul (metalliosakesed paneme polümeerilahusesse, mida hakkame elektroforeerima) või fiibrite vedel-/gaasifaasi järelreaktsioonil
Otsese elektrospinningu näited:
Cu nanoosakesed tekitatakse, redutseerides polüvinüülalkoholi (PVA) lahuses CuCl2 hüdrasiiniga (H4N2) – saadud suspensioonist valmistatakse otse PVA/Cu komposiit-nanofiibrid
Polüvinüülpüridiini (PVP) lahus etanoolis AgNO3 lisandiga pannakse reageerima H2S gaasiga, saades Ag2S nanoosakesed – segust valmistatakse PVP/Ag2S komposiit-nanofiibrid
Nanoosakeste tekitamiseks fiibri pinnale võimalik redutseerida nanofiibrisse segatud metalli sool:
in situ järelreaktsioonil
kuumutada fiibreid redutseerivas atmosfääris
Kõrgematel temperatuuridel kipuvad metalli nanoosakesed migreeruma fiibrite pinnale ning agregeeruma
Loeng 5. Superkondensaatorid (SK)
1. SK-s energia salvestamise mehhanism. Mille poolt on ära määratud SK energia ja võimsus, eluiga, efektiivsus?
Võimsus – energia kasutamise kiirus
Energia – tarvitatud või vabastatud energia hulk sõltub seadme võimsusest ning kasutamise kestusest:
Energia = Võimsus Aeg
Pikaajaliselt töötav madala võimsusega seade võib kasutada suurema hulga energiat, kui lühiajaliselt töötav kõrge võimsusega seade.
Akude elektroodidel toimuvad keemilised reaktsioonid on aeglased, kuid võivad toimuda pikaajaliselt – energia hulk suur, kuid võimsus väike
Ioonide adsorptsioon/desorptsioon EKKK elektroodide pinnal on väga kiire – suur võimsus (salvestatud energia kiire vabastamine), kuid väiksem energia hulk.
| Seade |
Aku |
SK |
| Eluiga (tsükleid) |
100 ... 10 000 |
< 1 000 000 |
| Efektiivsus (%) |
50-90 |
u 95 |
| Elektroodiprotsess |
Elektrokeemiline oks/red reaktsioon |
Füüsikaline adsorptsioon |
Energia ja võimsus – sõltub oluliselt elektrolüüdis kasutatavast solvendist: viskoossega väiksem energiahulk kättesaadav. Sõltub töötemperatuurist: madalal temperatuuril massiülekanne aeglane. Seda suurem, mida suurem on mahtuvus, rakupinge. Võimsus sõltub ka rakupingest ja takistusest.
Eluiga – ära määratud selle poolt, kui kondensaator töötab muultiku režiimiga, siis osaliselt võib toimuda elektrolüüdi lagunemise reaktsioon või elektrolüüdi pinnal parasiitsed reaktsioonid. Võib laguneda. Parasiitreaktsioonid tingitud rakupingest jms. Eluiga sadades tuhandetes tsüklites. Võrreldes akudega on eluiga oluliselt pikem, kuna protsess on peaaegu täielikult pöörduv ning ilma keemilise reaktsioonita.
Efektiivsus – elektriline efektiivsus. Peaaegu 100% lähedane. Põhiline languse põhjustaja sisetakistus. Mida suurem võimsusel töötab, seda suurem on takistuse mõju.
SK-s energia salvestamise mehhanism
Elektrilise kaksikkihi kondensaatorid (EKKK)
Elektrostaatiline laengusalvestus
Elektrolüüdi ioonide pöörduv adsorptsioon elektroodil
Elektroodi materjal (enamasti süsinik) suure eripinnaga (m2g-1) ning väga poorne
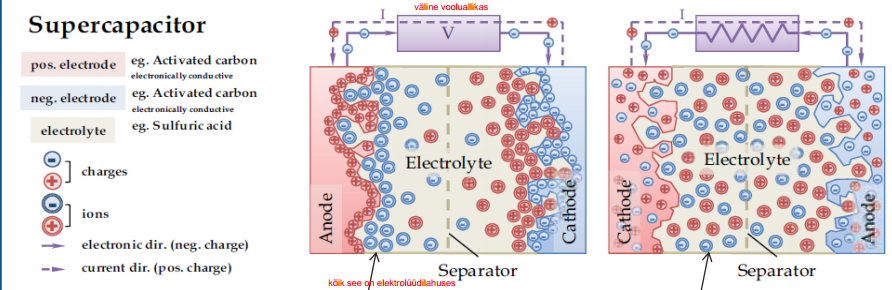
Vasakpoolne on laetud EKKK, parempoolne tühjendatud
Mõlemal elektroodil moodustub EKK, mida võib vaadelda kui tavalist tasapinnalist kondensaatorit, mille mahtuvus avaldub:
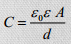
ε0, ε – vaakumi ja keskkonna dielektrilised läbitavused, d – elektroodide vaheline kaugus, A – elektroodide pindala
Võrreldes traditsioonilise elektrolüütilise kondensaatoriga, on d väga palju väiksem ning elektroodide pindala väga palju suurem ehk mahub rohkem laengut.
EKKKdes on + ja – elektroodid ühesugused, süsteemi võib vaadelda kui kahte järjestikku ühendatud kondensaatorit:
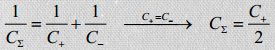
Wikist:
Laengusalvestusest:
elektrienergia salvestatakse elektroodidele (nagu akudeski), kuid mitte keemiliselt
ioonid liidetakse elektroodi pinnale füüsikalise adsorptsiooni teel.
Tänu elektroodi materjali suurele eripinnale >1000 m2 /g, ja süsiniku kõrgele erimahtuvusele, saadakse ka märkimisväärsed mahtuvused ~1 F/cm2 ühe elektroodi pinnaühiku kohta.
Seetõttu piisab suhteliselt väikesemõõtmelistest elektroodidest et saada märkimisväärne mahtuvus
SK laadimisel elektrolüüdi positiivselt laetud ioonid, katioonid, liiguvad katoodile (?), tekitades pinnal positiivse laengu
anioonid liiguvad anoodile (+), tekitades sellel negatiivse laengu.
Suurepinnalise süsiniku poorid toimivad seejuures laengusäilitajatena.
oluline optimeerida kogu süsteem selliselt, et kasutatava nanopoorse süsiniku poorid oleksid ioonidele sobivate "mõõtmetega".
Elektroodipaarist moodustub kaks järjestikku ühendatud kondensaatorit C+ ja C?.
Plaatide pindala määrab mahtuvuse
elektroodide vahelisest kaugusest, ehk elektrolüüdiga impregneeritud separaatori paksusest sõltub sisetakistus.
SK-s kogutakse laengud elektroodi pinnalt kokku voolukollektorite kaudu ning kui ühendada välisahelas + ja ? kokku, toimub tühjakslaadimine ja ioonid liiguvad lahuse sügavusse.
Laadimisel protsess kordub taas.
Ehitusest:
koosneb positiivsest ja negatiivsest elektroodist, mille välisküljele on ühendatud voolukogujad (kollektorid) ja sisemisi külgi eraldab separaator.
Kogu süsteem on impregneeritud sobiva elektrolüüdiga ja suletud korpusesse.
Kõrgema pinge saamiseks ühendatakse elemendid järjestikku kondensaatorpatareiks ehk mooduliks.
Pseudomahtuvuslikud kondensaatorid ehk redokssuperkondensaatorid
Pöörduv elektrokeemiline laenguülekande protsess (redoksreaktsioon)
Laeng salvestub läbi pseudomahtuvusliku käitumise – esineb kui termodünaamilistel põhjustel elektroodiprotsessi jätkumiseks vajalik laenguhulk q on rakendatava pinge U pidevalt muutuv funktsioon: C = dq/dU
Toimub mitme-etapiline redoksreaktsioon (mitte üks fikseeritud potentsiaalil toimuv reaktsioon nagu akudes).
Levinumad elektroodi materjalid: d-metallide oksiidid, juhtivad polümeerid, heteroaatomeid (N, O) sisaldavate funktsionaalsete rühmadega modifitseeritud süsinikud
Hübriidsuperkondensaatorid
Asümmeetriline süsteem:
Üks elektrood „aku-tüüpi“ ning teine „SK-tüüpi“
Saavutatav suurem rakupinge
Negatiivne elektrood on „aku-tüüpi“ grafiit, millesse interkaleeritakse Li-ioonid, positiivne elektrood on poorne süsinik, millel toimub anioonide pöörduv adsorptsioon.
Võrreldes EKKKdega, saadakse summaarseks mahtuvuseks kogu „SK-tüüpi“ elektroodi mahtuvus, sest Caku >> CSK
Ühtegi kommertsiaalselt kasutatavat veel pole
SK-de ühendamine
SKsid saab omavahel ühendada nii paralleelselt kui ka järjestikku
2. SK rakendused. Miks just SK on hea valik nendeks rakendusteks?
Energia kokkuhoiu rakendused
Kraanad, tõstukid, jne
Võimeline „kinni püüdma“ potentsiaalset energiat, mis kättesaadav tõstukil konteinerite alla laskmisel
Salvestatud energiat kasutatakse järgmise konteineri tõstmiseks
Superkondensaator võimaldab kasutada väiksema võimsusega põhi-energiaallikat
Õhusaaste vähendamine
Mõistliku suurusega aku võimsusest võib jääda väheks selliste rakenduste juures
SK-d pole nii temperatuuritundlikud kui akud, kasutatakse külmades piirkondades nt auto käivitamiseks
Energia optimaalne kasutus
Linnaliinibussid, prügiautod, pakiautod
Aku kasutamine korduvate lühikeste tsüklitena (≤10 s) on ebaefektiivne ning vähendab kiirelt aku eluiga
Lühiajalise protsessi käigus suudab kiire salvestusmehhanismiga SK „päästa“ suurema energiahulga
Kiire (10 s) laadimise korral kättesaadavast energiast tagasi SK korral 95%, aku ainult 50%
Tööriistada
SK eelistatud aku ees antud rakendustes:
Hea kvaliteediga suure võimsusega elektrienergia,
Tunduvalt pikem eluiga – ei vaja väljavahetamist,
Väga kiire laadimine.
Back-up mäluna kaamerates, mobiiltelefonides, mänguasjades, jne
Ööpäevane energiasalvestus
SK-sse salvestatakse energia öisel ajal, kui elektrienergia hind on odavam, ning kasutatakse päeval suure koormuse ning kõrgema hinna tingimustes.
Salvestatakse tuule- või päikeseenergiat kättesaadavuse hetkel.
3. SK elektrokeemiliseks uurimiseks kasutatavad meetodid – tsükliline voltammeetria ja impedants spektroskoopia (üldine põhimõte, millist infot SK kohta annavad)
Tsükliline voltammeetria
Elektroodi potentsiaali muudetakse fikseeritud kiirusega, näiteks 1 mV/s või 100 mV/s (potentsiaali laotuskiirus); ühtlase kiirusega muudetakse rakupotentsiaali, selle tulemusena hakkavad ioonid adsorbeeruma pinnale; graafik peab olema võimalikult nelinurkne: nii palju, kui paneme sisse, nii palju saame välja
Mõõdetakse voolu
EKKKde korral peaks olema voltamperogrammi kuju võimalikult lähedane ristkülikuga ning sümmeetriline nullvoolu -joone suhtes -> KEEMILISI REAKTSIOONE EI TOIMU !
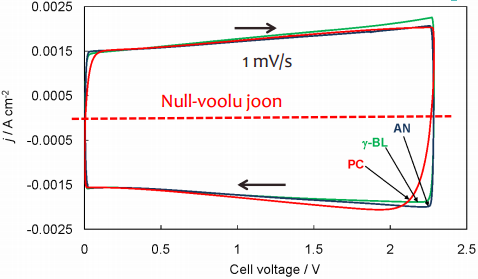 tekib ioonide puudujääk, süsteem ei suuda nii kiirelt stabiliseeruda - järelikult pole optimaalseim materjalide valik olnud; sellep tekivad kõrvalekalded ristkülikukujust
tekib ioonide puudujääk, süsteem ei suuda nii kiirelt stabiliseeruda - järelikult pole optimaalseim materjalide valik olnud; sellep tekivad kõrvalekalded ristkülikukujust
Keemiliste reaktsioonide esinemisel leiduvad voltamperogrammidel fikseeritud potentsiaalidel piigid
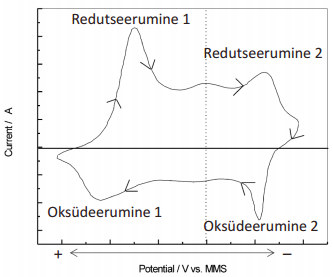
Meetodiga võimalik teada saada:
Optimaalne rakupinge,
Mahtuvuse väärtus,
Hinnanguliselt toimuvate protsesside kiirus (massiülekanne, adsorptsioon),
Keemiliste (kõrval)reaktsioonide esinemine,
Elektrolüüdi lagunemisreaktsioonid,
Orgaaniliste solventide korral vee-lisandi reageerimine,
Redoksmahtuvuslike reaktsioonide korral nende esinemise potentsiaali-vahemik.
„Elektrolüüdi vaesumise“ esinemine.
Impedants-spektroskoopia
Rakendatakse dc vool – elektroodide vahel tekib fikseeritud potentsiaalide erinevus.
Süsteemil lastakse jõuda tasakaaluolekusse.
dc-le lisaks rakendatakse väikse amplituudiga (5 mV) sinusoidaalne ac signaal.
ac mõjul tekkiv signaal väljendatakse kui impedants Z.
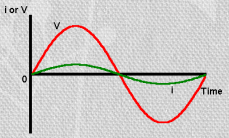 Takisti korral: U ja I on samas faasis, kuid I väärtus on peaaegu null
Takisti korral: U ja I on samas faasis, kuid I väärtus on peaaegu null
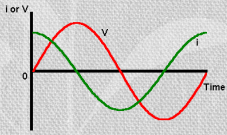
Kondensaatori korral: I on 1/4 tsüklit ees – ehk faasinurk on -90o (-1/4 täisringist)
f on alati sama U ja I jaoks!
Impedants väljendatakse U ja I signaalide suhtena.
Süsteemi lihtsamaks matemaatiliseks kirjeldamiseks esitatakse impedants komplekssuurusena:
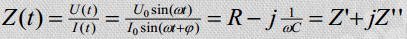
Seega:
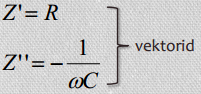
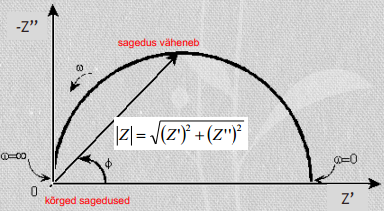 ω = 2πf – ringsagedus
ω = 2πf – ringsagedus
Saadav info:
Elektrolüüdi ja elektriliste kontaktide takistus Rs (f -> ∞),
Difusiooniline takistus elektroodi materjali poorides,
Mahtuvuse väärtus,
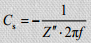
Karakteerne ajakonstant,
aeg, mis kulub ½ kondensaatoris salvestatud energia vabastamiseks.
Rakupinge hindamine, kus algavad lagunemisreaktsioonid.
Energia- ja võimsustiheduste arvutamine:
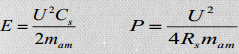
4. SK elektroodi materjalid (vajalikud omadused, näited, poorse struktuuri mõju SK
karakteristikutele, sealhulgas sobivus elektrolüüdiga)
Vajalikud omadused:
Hea juhtivus (vase juhtivust päris omama ei pea, aga ei tohi olla pooljuht või isolaator)
Hea elektrokeemiline stabiilsus
Temperatuuri-stabiilsus
Suur eripindala (1200 ... 1800 m2g-1)
Avatud poorsus (dpore= 0.7 ... 4.0 nm)
Võimalikult madal hind
Kergesti töödeldav
Näited:
Süsinikmaterjalid EKKKde jaoks:
Carbon blacks (nn söed)
Aktiveeritud süsiniku pulbrid või kangad
Amorfsed süsinikud (nt karbiidset päritolu süsinikud)
Süsinik nanotorud, sibulad ja nanosarved
Süsinik-aerogeelid
Poorse struktuuri mõju SK karakteristikutele
Elektroodi materjal
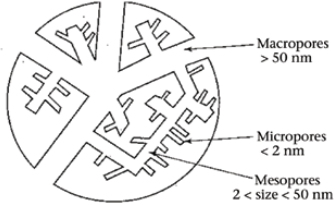 Mida suurem on elektroodi materjali eripind (specific surface area - SSA), seda suuremat mahtuvust võib eeldada
Mida suurem on elektroodi materjali eripind (specific surface area - SSA), seda suuremat mahtuvust võib eeldada
Tegelikult on ka kõige poorsemate materjalide mahtuvus limiteeritud
Puudub lineaarne suhe SSA ja mahtuvuse vahel
Osalise või täieliku solvaatkattega ioonid ei mahu väiksematesse pooridesse
Materjal peab olema mingil määral mesopoorne, et tagada ioonide kiire transport mikropooridesse üle kogu elektroodi materjali
Sobivus elektrolüüdiga
Kui poorid solvateeritud ioonidest suuremad, mahtuvus kasvab mõlemal poori seinalt. Kui poorid natuke väiksemad, mahtuvus väheneb, sest ainult 1 kiht ioone mahub, osa ruumi jääb kasutamata. Kui poor väiksem solvateeritud ioonist – mahtuvuse kasv tänu solvaatkatte osalisele eemaldumisele.
I – poorid solvateeritud ioonidest suuremad, mahtuvuse kasv mõlemalt poori seinalt. II – mahtuvus väheneb, sest ainult 1 kiht ioone mahub, osa ruumi jääb kasutamata. III – poori d solvateeritud ioonist väiksem – mahtuvuse kasv tänu solvaatkatte osalisele eemaldumisele.
mida väiksemaks poori muudame, siis ühel hetkel mahtuvus hüppab ülesse > pooridesse lähevad kat/anioonid ilma solvaatkatteta > mahtuvus muutub suureks, aga liikumine on üliaeglaseks muutunud e ajakonstandid muutuvad ülisuureks
vaja leida ideaalne poori laiuse ja iooni suuruse tasakaalu
5. SK vesi- ja mittevesilahustel põhinevad elektrolüüdid (vajalikud omadused, näited, eelised-puudused)
Solvent määrab maksimaalse potentsiaalide erinevuse positiivselt ja negatiivselt laetud elektroodide vahel (U).
Kahjuks vee lagunemise termodünaamiline ülepinge (1,23 V) 2–4 korda väiksem kui mõningate orgaaniliste solventide puhul (kuni 5 V).
Vee baasil valmistatud EKKK U ≤ 0,8 V, kuid atsetonitriili (AN) või propüleenkarbonaadi (PC) baasil valmistatud EKKK U = 2,7–3,5 V, sõltudes oluliselt vee (lisandi) kontsentratsioonist EKKKs.
Olulised omadused:
Elektrokeemiline stabiilsus (max U),
0.001% veesisaldus orgaanilises elektrolüüdis vähendab rakendatavat pinget ~10 mV.
Madal viskoossus,
Hea juhtivus,
Suur ioonide kontsentratsioon (hea lahustuvus solvendis),
Kõrge dielektriline läbitavus,
Minimaalne mõju keskkonnale,
Soodne hind.
Vee baasil elektrolüüdid EKKKdes
Elektrokeemiliselt stabiilne kuni ~1 V
Vesilahusega EKKK mahtuvus ~2 korda suurem kui orgaanilistel solventidel põhinev EKKK
Odavam kui orgaanilised solvendid
Võimalik valmistada kõrgema kontsentratsiooniga elektrolüüte
Näiteks:
Vees lahustunud soolad nagu Na2SO4 ja NaCl
KOH lahus (1 kuni 6 M)
H2SO4 lahus (1 kuni 4 M)
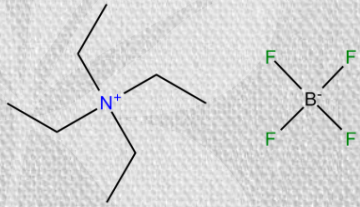 Orgaaniliste solventide baasil elektrolüüdid
Orgaaniliste solventide baasil elektrolüüdid
Elektrokeemiliselt stabiilne kuni ~3.5 V
Kommertsiaalselt rakendatud tetraalküül-ammonium soolad
Võrreldes H2O baasil elektrolüütidega
Madalam juhtivus (20-50 korda suurem takistus)
Saab kasutada madalamatel temperatuuridel (-50 oC)
Atseetonitriil (AN)
Madal viskoossus ja kõrge juhtivus
Kõrge dielektriline läbitavus
Keskkonnakahjulik -> peamine põhjus alternatiivsete solventide/elektrolüütide testimiseks
Propüleenkarbonaat (PC)
Kõrgem viskoossus ja madalam juhtivus vs. AN
Mitte nii kahjulik kui AN
γ-butürolaktoon (γ -BL või GBL)
Viskoossus ja juhtivus võrreldavad AN-ga
Psühhotroopne aine -> ei sobi tarbeesemetes kasutamiseks
6. Ioonsed vedelikud SK elektrolüütidena (omadused, eelised-puudused, näited levinumatest ioonidest, temperatuuri mõju)
Omadused, eelised-puudused
Ioonne vedelik – toatemperatuuril vedelad soolad
Teoreetiline elektrokeemilise stabiilsuse vahemik ~6 V
Ei saa kasutada madalatel temperatuuridel (kõrge viskoossus)
Võrreldes H2O või orgaaniliste solventidega
+ Väike aururõhk
+ Mitte-süttiv
– Suurem viskoossus
– Madalam juhtivus
– Viskoossuse vähendamiseks ja juhtivuse suurendamiseks:
Võiks kasutada kõrgematel temperatuuridel (kuni 60–80 OC)
Lisada väike kogus orgaanilist solventi
Mõju keskkonnale pole selge, kuid üliväike aururõhk vähendab veidi keskkonda sattumist.
Ioonseid vedelikke on palju, kuid kõik pole sobivad EKKK rakenduseks
Näited:
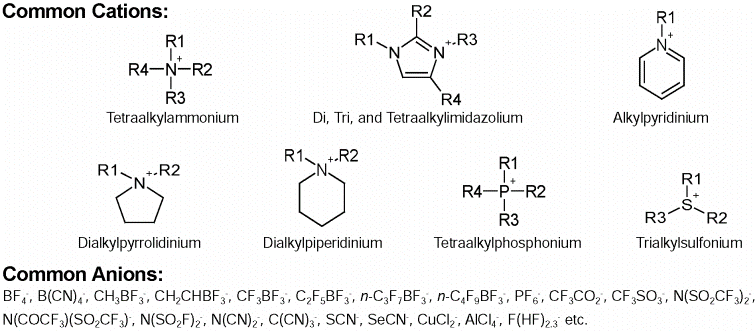
Temperatuuri mõju
Karbiidne süsinik + EMImBF4
Kõrgematel temp.del moonutusefektid:
EMImBF4 lagunemine,
H2O ja O2 jääkide lagunemine,
Funktsionaalrühmade redoksreakts.,
Adsorptsiooni tasakaalu nihkumine desorptsiooni suunas.
Puudub mahtuvuslik käitumine kõrgetel temp.del
Karakteerne ajakonstant τR kasvab.
Ehk ei sobi kasutamiseks kõrgel temp.-l!
7. SK separaator (vajalikud omadused, näited, mõju SK karakteristikutele)
Separaatori/membraani eesmärk takistada elektrilise kontakti tekkimist elektroodide vahel ehk lühistumist. (peaks olema võimalikult õhuke, muidu läheb ruum raisku ja SK kaal suureks, keemiliselt inertne, peab laskma elektrolüüdi iooni sisse-välja)
Vajalikud omadused:
Ei tohi olla elektronjuht
Peab olema ioonidele vabalt läbitav
Keemiliselt ja elektrokeemiliselt stabiilne
Madal tihedus
Sobiv poorne struktuur (pooride suurus)
Termiliselt ja mehhaaniliselt stabiilne ja kestev
Näited:
 Polüvinülideenfluoriid (PVDF)
Polüvinülideenfluoriid (PVDF)
Polüpropüleen
Tselluloos
Iga solvendi jaoks on oma ideaalne separaator
Mõju SK karakteristikutele
Uuritav süsteem – karbiidset päritolu süsinikust elektroodid, 1 M TEMABF4 + AN elektrolüüt ja erinevast materjalist (erineva paksusega) separaatorid
Tsüklilistelt voltamperogrammidelt näha:
Separaatori materjal ja paksus ei mõjuta praktiliselt mahtuvuse väärtust,
Mahtuvus määratud elektroodi materjali ja elektrolüüdi poolt.
Impedantsi kõveratelt näha:
Kõrgsageduslik takistus sõltub separaatorist – süsteemi summaarne takistus muutub,
Mida suurem poolkaar, seda aeglasem süsteem.
Energiatihedus praktiliselt sõltumatu separaatorist (mahtuvus).
Võimsustihedus mõjutatud süsteemi takistusest
antud juhul suurim tselluloosist separaatoritega
Loeng 6. Süsinikmaterjalide valmistamine
Süsiniku aatomite omadus moodustada erinevat liiki süsiniksidemeid võimaldab erinevate allotroopide* moodustumist:
Teemant (sp3 hübridisatsioon)
Grafiit (sp2)
Fullereenid ja nanotorud (sp2)
Amorfne süsinik (sp3+ sp2)
1. Klaassüsinik (omadused, sünteesimeetodid, rakendused)
Omadused:
Mitte-grafitiseeruv , väga isotroopne (ainult sp2)
Klaasjas välimus, väga jäik
Madal gaaside ja vedelike läbilaskvus (puudub avatud poorsus)
Hea temperatuuritaluvus ja keemiliselt inertne
Elektrijuht
Suletud poorsus – poorid moodustuvad tühimikest suvaliselt orienteerunud ning kokkupõimunud grafeeni kihtide vahel. Samuti kiirel karboniseerimisel gaasi eraldumise mõjul.
Süntees
Valitud polümeeride termiline lagundamine (tüüpiliselt fenoolsed polümeerid)
Polümeer peab kõrgel temperatuuril ristseostuma
Orgaaniliste ühendite aeglane karboniseerimine ja järelkuumutamine 3000 oC-ni
Kuumtöötluse temperatuur mõjutab omadusi (juhtivus, struktuur , läbilaskvus)
Rakendused
Elektroodi materjal elektrokeemias
Inertne sileda pinnaga elektrood mitmete redoksreaktsioonide kineetiliste parameetrite uurimiseks
Keemiatarbed (kõrg-temp. tiiglid)
Autoemissioon elektroonilistes seadmetes
2. Grafiitse struktuuriga süsinikud – grafiit, grafeen, süsinik-kangas (omadused, sünteesimeetodid, rakendused)
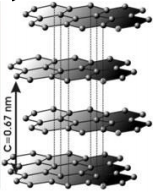 Grafiit
Grafiit
Omadused
3-koordinaatsed sp2 C-aatomid (3 σ ja 1 π side)
Heksagonaalne võre
Ühes suunas pehme materjal
Tumehalli värvi
Elektronjuht
Termodünaamiliselt stabiilsem kui teemant*
* Teemant ei muundu tavatingimustel termodünaamiliselt stabiilsemaks grafiidiks tänu väga suurele kineetilise energia barjäärile, teemant on „metastabiilne“
Valmistamine
Grafiiti saadakse mitmetest looduslikest maakidest nende rikastamisel
Sünteetilise grafiidi valmistamine:
Karborundist (ränikarbiidist SiC) aurustub Si välja 4150°C juures, jättes järele grafiitse süsiniku
Grafitiseeruvatest süsinikest kõrgel temperatuuril töötlemisel
Naftakoks segatakse kivisöe tõrvaga, pressitakse soovitud grafiit-detaili kuju (nt elektrood), kuumutatakse tõrva karboniseerimiseks ning grafitiseeritakse 3000 °C juures
Kasutamine
Nii looduslikku kui sünteetilist grafiiti kasutatakse Li-ioon akude elektroodi materjalina
Juhtiva lisandina superkondensaatorite elektroodides
Kõrgtemperatuursed tiiglid
Kaarlahenduse ahjudes elektroodi materjal (redutseerija), kus toodetakse terast, jne
Li-ioon akude/kondensaatorite elektrood
Algselt kasutati Li-ioon akudes liitium-metall (–) elektroodi
Korduval laadimisel/tühjenemisel tekkisid Li pinnal nõelad
Põhjustavad lühistumist ja ülekuumenemist
Li-metall asendati grafiitse süsinikuga
Li+ioonide interkaleerumine – Li+ difundeerub grafiidi kihtide vahele (korduval laadimisel/tühjenemisel elektroodi materjal paisub/tõmbub kokku, mis viib lagunemiseni)
Suur Li-mahutavus – 1 Li+ ioon 6 C aatomi kohta
Grafeen
Omadused
Elektrijuhtivus on ääretult hea
Eelised vs. Grafiit
Esineb rohkem nö äärestruktuuri (edge plane) mitte grafeenikihi külgpina (basal plane)
Eripind sama ruumala kohta tunduvalt suurem
Valmistamine
Mikrolaine-plasmast keemilise aursadestamisega (CVD) katalüüsitud substraadile
Kuumutatud nikkel-substraadile kõrgsageduskiirgusega (raadiolaine) tekitatud plasmast CVD sadestusega ilma katalüsaatori nanoosakesteta
Superkondensaatori rakenduses on Ni voolukollektor
40% Ar + 60% H2plasmas söövitatakse Ni
Suletakse Ar voog
Lisatakse CH4 gaas (C allikas)
Kuumutatakse Ni 1000 ºC ? sadeneb grafiitne C
Mööda Ni pinda kasvavate grafiidi saarekeste põrkumisel pööravad grafeenikihid üles suunas
Kasutamine
Grafeen elektroodid superkondensaatorile
Eripinda mõnevõrra vähem vs. poorsed süsinikud -> mahtuvus väiksem
Väga kõrge võimsus
Puudub pooritakistus (massiülekande protsessid kitsastes poorides)
Aktiivmaterjal (süsinik) on sadestatud otse voolukollektorile (Ni), mis vähendab kontakttakistust
Grafeen/grafiit on tunduvalt kõrgema elektronjuhtivusega ehk väike süsiniku takistus
Faasinurk -90º vastab ideaalselt mahtuvuslikule käitumisele
Mida suuremal võimsusel saavutatakse mahtuvuslik käitumine, seda suurma võimsusega saab seade töötada maksimaalsel mahtuvusel/energial
Süsinik-kangas
Omadused ja kasutamine
Peentest (5-10 μm) süsinikkiududest „punutud“ kangas
Kristalne süsinik (grafiit), mis asetseb paralleelselt kiu teljega
Väga kõrge tugevus/ruumala suhe
Kasutamine:
Komposiitidest polümeeridega valmistatakse nt helikopteri tiibasid (carbon fiber reinforced polymer)
Kasutatakse ka superkondensaatorite elektroodidena – pole vaja sideainet, et saada süsiniku-kiht
Struktuurilt on grafiitne, kuid materjali tõmbetugevuse garanteerib nn turbostraatne struktuur – grafeenikihid pole täpselt paralleelses asetuses nagu grafiidis, vaid on juhuslikult kaardus/volditud
Polüakrülonitriilist sünteesitud kiud on enamasti turbostraatsed ning väga kõrge tõmbetugevusega
Tõrvast sünteesitud kiud on grafiitsed ning väga jäigad ja kõrge elektronjuhtivusega
Süntees
PAN peened fiibrid saadakse elektroformeerimise või polümeeri tõmbamise meetodil
Fiibreid kuumutatakse õhus ~300 °C juures – vabanetakse H-sidemetest ning oksüdeerib materjali
Inertatmosfääris (Ar) karboniseeritakse ~2000 °C juures – tekib grafiitne (turbostraatne) struktuur
Järeltöötlusega on võimalik omadusi veel reguleerida
3. Amorfsed süsinikud – aktiveeritud süsinik, carbon black, aerogeel (omadused, sünteesimeetodid, rakendused)
Aktiveeritud süsinik
Omadused:
Puudub ulatuslik kristallstruktuuri korrapära
Lokaalne korrapära, lokaliseeritud π elektronid
sp3 ja sp2 sidemed segamini
Palju vabasid radikaale liikumatus süsiniku struktuuris* (‘dangling bonds’)
sp2/sp3 määrab omadused:
Elektronjuhtivus
Soojusjuhtivus
Kõvadus
Tihedus
* Süsinikku saab stabiliseerida radikaalide hüdrogeenimisel
B. Orgaaniliste ühendite lagundamine (levinuim, pm pürolüüs)
Süsinikurikaste orgaaniliste lähteainete kuumutamine (karboniseerimine, pürolüüs) inertatmosfääris
Lähtematerjalid
Naturaalsed: kookoskoor, puit, tõrv, süsi
Sünteetilised polümeerid
Osasid saadud süsinikke aktiveeritakse pürolüüsi järgselt – nn aktiveeritud süsinikud
Avab suletud poorid – eripind kasvab
Pikemal oksüdeerimisel poori keskmine suurus kasvab
Füüsikaline aktiveerimine CO2 või veeauruga >250 °C
Keemiline aktiveerimine – enne karboniseerimist lisatakse lähteainele hapet, tugevat alust või soola (H3PO4, KOH, NaOH, CaCl2, ZnCl2). Karboniseerimine toimub nii madalamal temperatuuril ja kiiremini, koos samaaegse aktiveerimisega
Carbon black
Omadused:
Toodetakse suurtes kogustes tööstuslikult
Ümara kujuga kolloidsuurusega osakesed – agregaadid <1 μm
Suure juhtivusega tahmadel on hargnenud avatud poorsusega struktuur, väike ühtlane osakeste suurus, keemiliselt puhas (hapnikuvaba) pind
Süntees:
Erinevate süsivesinike osaline põletamine või lagundamine gaasifaasis
Furnace black (d < 50 nm) – nafta pürolüüsist saadava tõrva või pigi osaline põletamine
Acetylene black (d = 45-55 nm) – etüüni lagundamine (mitte põletamine)
Thermal black (d = 100-500 nm) – gaasiliste süsivesinike pürolüüs
Rakendused:
Süsinikelektroodi materjal või juhtiv lisand
Tugevdav lisand kummi-toodetele (rehvid, juhtmed) – juhib soojust ära, seega vähendab termilisi kahjustusi ja suurendab eluiga
Printeritahmad ja värvid
Nahatöötlusvahendid
Aerogeel
Omadused
Gaasis dispergeerunud tahke materjal
Väga madal tihedus (< 0.1 g cm-3)
Üsna haprad
Soojusisolaator (väga poorne), praktiliselt kustutab 3 soojusülekande liiki (juhtivus, konvektsioon, kiirgumine):
Koosneb enamjaolt gaasist, gaasid on halvad soojusjuhid (eriti SiO2 -aerogeelid, sest SiO2 ise halb juht – metall-/süsinik-aerogeel juhivad paremini)
Konvektsioon minimaalne, sest õhk ei saa ringelda tahkes maatriksis
Süsinikaerogeel on hea kiirgusinsulaator – C adsorbeerib IR-kiirgust, mis on soojuse kandja tavatemperatuuril
Valmistamine
Valmistatakse geelist superkriitilisel* kuivatamisel
Vältida tahke materjali kokku tõmbumist/varisemist
* Kõrgel temperatuuril ja rõhul eemaldatakse geelist vedel faas
Rakendused:
SiO2 -aerogeel on aknamaterjal (väike soojuskadu)
Keemiline adsorbent, etc.
NASA kasutas kosmosetolmu kogumiseks Stardust kosmoselaeval
Süsinik-aerogeel
Omadused
Osakeste suurus nm-skaalas, kovalentsidemetega omavahel seotud
Peamiselt mesopoorsed, tüüpilise poorisuurusega ~7-10 nm
Eripind kuni 1000 m2g-1
Elektonjuhtiv (sõltub aerogeeli tihedusest)
Süntees:
Sool-geel meetodil sünteesitud orgaaniline aerogeel pürolüüsitakse inertgaasi atmosfääris
Geel saadakse näiteks formaldehüüdi ja metüülresortsinooli polükondensatsioonil
Rakendused:
Päikesepaneelid – päikeseenergia kollektor (peegeldab ainult 0.3% kiirgusest IR alas)
Katalüsaatori kandja
4. Amorfsed süsinikud – CDC (omadused, sünteesimeetodid, rakendused)
Omadused
Amorfsel CDC-l kitsas poorijaotus
Sünteesitud C omadused sõltuvad:
Lähtekarbiidist
Sünteesi temperatuurist
Kuumutamise kestusest
Järeltöötlusest
C aatomite asetus ning ruumiline jaotus karbiidis määravad ära sünteesitud CDC süsinikmaterjali poorijaotusfunktsiooni
C vahekaugused on erinevad olenevalt lähtematerjalidest (st nt mis metall C-metall võrgustikus on; mõnedes karbiidides on ka 2 metalli - saab väiksema ja suurema pooriga C-materjale)
Sünteesimeetodid
A. Halogeenimismeetod (eesmärk võtta C-metall võrgustikust metall välja)
Karbiidset päritolu süsinik – carbide derived carbon (CDC)
Selektiivne metalliaatomite välja söövitamine karbiidi struktuurist kõrgel temperatuuril (>600°C) ning normaalrõhul
Keemiline reaktsioon: 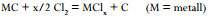
O2-vabas keskkonnas
MClx juhitakse süsteemist välja
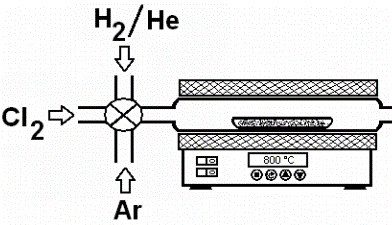 Proov puhastatakse Cl2 ja MClx jääkidest:
Proov puhastatakse Cl2 ja MClx jääkidest:
Intertgaasi voolus
Kuumutades H2 käes
H2 kasutatakse poorsuse avamiseks ja pooride suuremaks söövitamiseks
Reaktsiooni viiakse läbi ka teiste halogeenide (peamiselt F2) ja halogeenhapetega (HF, HCl)
Kloreerimine kõige soodsam ja suuremas skaalas teostatav meetod
B. Hüdrotermiline karbiidide söövitamine:
Karbiidi reaktsioon superkriitilise veega:
Vesi temperatuuril ja rõhul kriitilisest punktist üleval
Tc ~ 647 K = 374 oC
Pc ~ 22 Mpa = ~ 220 atm
Suure reageerimisvõimega ja madala viskoossusega
Reaktsiooni produktid: C, MeOx, CH4, CO2, CO, H2
H2O:SiC suhe:
Madala suhtega C ja SiO2 sadenesid
Vahepealse suhtega C sadenes ja SiO2 lahustus üleliigses vees
Kõrgel suhtel ei moodustunud kumbki, toimus ainult aktiivne SiC oksüdeerumine
Süsiniku saagise kriitiline faktor on moodustuvate C-sisaldavate gaaside hulk
Nt CH4 on mittestabiilne kõrgel T, kuid kõrge P suurendab stabiilsust ja seega väheneb C saagis
C. Karbiidide termiline lagundamine:
Kõrgel temperatuuril lagunemine vaakumis või inertgaasi atmosfääris (kõrge T ja alandatud rõhk – metallide välja lendamiseks hea)
Karbiidid sulavad inkongruentselt – karbiidi moodustav element aurustub, sest C sulamistemperatuur ületab enamike metallide oma
Süsinikul on madal aururõhk kõrgetel T-del võrreldes paljude metallidega
Osakeste kuju säilib hästi. Vaakumis lagundamisel võib olla tekkinud süsiniku pinnal näha isegi karbiidil eksisteerinud kriimustusi.
Amorfse süsiniku kasutamine
Elektroodi materjal superkondensaatorites
Suur eripind
Avatud poorsus
Keemiliselt stabiilne
Termiliselt stabiilne
Hea elektrijuhtivus
Vesiniku ja metaani salvestamine
Pöörduv gaasi salvestamine on kütuseelemendi jt tehnoloogiates kriitilise tähtsusega
Võimalused salvestamiseks:
Füüsikaline adsorptsioon – tseoliitidel ja süsinikmaterjalidel
Kemosorptsioon H2 salvestamiseks metallhüdriididena
Katalüsaatori kandja
Pt-katalüsaatorit kasutatakse hüdrogeenimise ja oksüdeerimise reaktsioonidel
Samuti hapniku redutseerumise reaktsioon PEM kütuseelemendi katoodil
Süsinikmaterjalid sobivad suure kättesaadava eripinna tõttu
Molekulaarsõelad
5. Süsinik-nanotorud (omadused, sünteesimeetodid, rakendused)
Omadused
| Mitmeseinalised nanotorud (MWCNT) |
Üheseinalised nanotorud (SWCNT) |
| nanomeetri järgus diameetriga keskmist nano-toru ümbritsevad omavahel ~0.34 nm kaugusega grafeeni kihid |
Üks grafeeni kiht moodustab nanomeetri järgus diameetriga torukese. Minimaalne stabiilse nanotoru diameeter on ~0.4 nm (kuni 30 nm) |
Nanotorude pikkus mõnikümmend nm kuni mitu µm
Struktuur
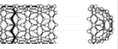 Siksak (zigzag):
Siksak (zigzag):
Mõned C-C sidemed nanotoru teljega paralleelsed
Mittekiraalne struktuur
 Tugitool (Armchair):
Tugitool (Armchair):
Mõned C-C sidemed nanotoru teljega risti
Mittekiraalne struktuur
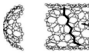 Kiraalne*:
Kiraalne*:
„Kruvikeeraja“ ümber nanotoru telje
* Kiraalses molekulis puudub sisemine sümmetriatasand ja selle peegelpilt ei lange kokku algse molekuliga
Nanotorud võivad olla metallilised või pooljuhid
Juhtivus praktiliselt ei sõltu nanotoru pikkusest, küll aga diameetrist ja kiraalsest nurgast, mille all nanotoru on „kokku keeratud“
Teadaolevad sünteesimeetodid annavad segu erinevate struktuuridega CNTdest, seega juhtivad omadused varieeruvad
Süntees
A. Kaarlahendusega
Rakendatakse 20-25 kV pinge 1 mm vahekaugusega 5-20 μm diameetriste süsinikelektroodide (grafiit) vahel 500 torr rõhuga voolava He all
Süsinikuaatomid eralduvad (+) elektroodilt ning moodustavad nanotorusid (–) elektroodil
Et sünteesida SWCNTd, väike kogus Co, Ni või Fe lisatakse katalüsaatorina (+) elektroodile
Saadakse SWCNTd 1-5 nm diameetri ja 1 μm pikkusega
Ilma katalüsaatorita tekivad MWCNTd
Osa süsinikust sadeneb tahmana
Nanotorude saagis oleneb He rõhust (vähemalt 500 torri)
Kaarlahendusega saadud nanotorud ei sisalda katalüsaatorite lisandeid
Sünteesitud MWCNT -d on kõrge kristallilisusega ja neil on vähem defekte võrreldes teiste meetoditega
B. Laseraurustamine
Näide:
Ar gaasi sisaldav kvartstoru ja grafiit-märklaud (target) kuumutatakse 1200°C
Vesijahutusega Cu kollektor asetatakse torusse, kuid mõnevõrra ahjust välja
Grafiit-märklaud sisaldab veidi Co ja Ni katalüütiliste nukleatsiooni-tsentritena nanotorude tekkimiseks
Võimas impulsslaserkiir suunatakse märklauale, mis aurustab süsinikku grafiidist
Ar kannab C aatomid kõrg-T tsoonist Cu kollektorile, millel nad sadenevad nanotorudena
Saab sünteesida nanotorusid 10-20 nm diameetri ja 100 μm pikkusega
SWCNTde diameetrite jaotus väiksem kui kaarlahenduse meetodiga
Erinevate nanotorude sünteesiks saab varieerida süsteemi temperatuuri, laserkiirguse intensiivsust (tihedust), katalüsaatorit.
C. Keemiline aursadestus
Kõrgel temperatuuril lagundatakse süsivesinik-gaas nagu C2H4, C2H2, CH4
Gaasi lagunemisel tekkivad C aatomid sadenevad jahutatud substraadil, mis võib sisaldada erinevaid siirdemetallide nanoosakesi katalüsaatorina (nt Fe) või oksiide (nt Fe2O3 ja Al2O3)
Katalüsaator võib olla ka laguneva ühendi koostises – näiteks ferrotseen Fe(C5H5)2
Saab sünteesida avatud otstega CNTsid – teiste meetoditega mitte
Otsi saab avada oksüdeerimisel CO2 või O2 kõrgel temperatuuril või nanotorude keetmisel konts. HNO3
Meetod võimaldab järjestikust sünteesi – kõige lihtsam ja eelistatum suuremas koguses sünteesiks
SWCNTd:
Pürolüüs
Lahja süsivesinike-metallorgaaniliste ühendite segu
Reaktsioonitingimusi tuleb täpselt kontrollida, muidu tekivad MWCNTd
MWCNTd:
Elektrolüüs süsinikelektroodide ja sula halogeensooladega süsteemis (Ar atmosfääris)
Hüdrotermiline meetod
Polüetüleeni ja vee segu, Ni katalüsaator
T ~ 800 oC ja P = 60 ... 100 MPa
6. Milliste meetoditega ja millist infot võiks saada süsinike poorsuse ning kristallstruktuuri kohta?
Röntgendifraktsioon-analüüs (XRD)
Röntgenkiirte lainepikkus λ väiksem kui nähtaval valgusel
λ võrreldav kaugustega aatomite vahel tahketes struktuurides -> difraktsioon esineb monokromaatset kiirgust kasutades
Kristalsel materjalil esineb spetsiifiline aatomstruktuur, mis annab karakteerse XRD spektri
Raman spektroskoopia analüüs
Nähtava valguse alas valguskvandid ergastavad erinevates sidemetes elektrone
Madalamale energiatasemele naastes kiirgavad elektronid kvandi
Kiiratud kvant:
Ergastava kvandiga sama l (Rayleigh hajumine)
Erinev, tavaliselt väiksem l algsest (Raman hajumine)
Kiirgunud kvantide l detekteeritakse ning saadakse Raman spekter
Jälgitakse erinevate aatomite vibratsiooni, rotatsiooni jt madala sagedusega protsesside signaali – saadakse info keemiliste sidemete loomuse kohta
Grafitiseerumise aste muutub lähtekarbiidi ja sünteesi temperatuuriga – sõltub tugevalt lähtestruktuurist ja keemilise sideme loomusest karbiidis
Loeng 7. Tahke- ning vedelfaasi süntees
1. Kuidas mõjutab lähtematerjali pulbri jahvatamine kompaktse detaili valmistamist? Olulised pulbri omadused
Lähteaine pulbri jahvatamise mõju kompaktse detaili valmistamisele
Pulbri omadused mõjutavad valmistatava seadmete efektiivsust ja eluiga
Nt SOFC elektrolüüt peab olema tihe oksiidide segu
Väga peen jahvatus oluline
SOFC elektroodid peaksid olema poorsed
Mitte nii peenjahvatus
Mida ebahomogeensem jahvatus, seda ebaühtlasema struktuuriga lõpp-produkt
Peenema jahvatuse korral reaktsioonipinda rohkem – süntees kiirem (Reaktsiooniaeg on võrdeline osakeste suuruse ruuduga)
Jahvatamine tekitab defekte kristallstruktuuris – ulatuslikum difusioon ning kiirem paakumine (ning materjali tihenemine)
Olulised pulbri omadused
Osakese suurus (sh suurusjaotus) ja kuju
Stöhhiomeetriline koostis
Puhtus (ka pinnal)
Aglomeraadid
Jne
Pulbreid segatakse detaili valmistamisprotsessis vajadusel lisanditega – poorimoodustajad, juhtivad lisandid, jne
Osa detailidest läbivad kuumutamise faasi
Eriti oluline keraamiliste detailide korral, mis just kuumutamise käigus saavad sobiva kristallstruktuuri (polümorfi) ning toimub tihenemine/poorsuse moodustumine
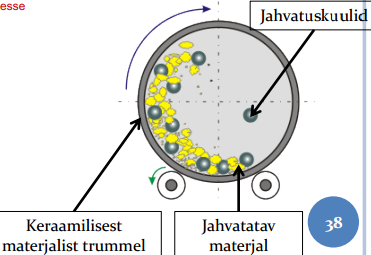 2. Märgjahvatamine vs. kuivjahvatamine kuulveskis (kirjeldus, eelised-puudused)
2. Märgjahvatamine vs. kuivjahvatamine kuulveskis (kirjeldus, eelised-puudused)
Põhimõte:
Kuivjahvatamisel – trumlis on jahvatuskuulid + jahvatatav materjal
Kuulid annavad kineetilist energiat materjalile, nt lõhuvad inaktiivset reaktsioonikihti
Märgjahvatamine – lisatakse ka vedelfaas
Ka pindaktiivseid ühendeid
Optimeerida
Kuulide suurust
Kuulide hulka
Keemilist koostist
kuulid võimalikult kõvast materjalist, et ei saaks jahvatavasse materjali lisaks ebasoovitavat kuulide materjali, võib segada edasisi protsesse
Jahvatussegu hulka
Trumli rotatsiooni kiirus
KUULVESKIS JAHVATAMINE (kuivjahvatamine)
Meetodi eelised:
Mehaaniliselt lihtne ja robustne
Suhteliselt odavad süsteemid
Puudused:
Saadava pulbri omadusi raske kontrollida
Kuulid kuluvad ning saastavad materjali
Küllaltki aeglane protsess (mõni päev)
Saastumist saab vähendada:
Optimeerides jahvatamise kestust
Kasutades kõvasid materjale
Kasutades kuule jahvatatava materjaliga sarnase keemilise koostisega
Regulaarne kuulveski inspekteerimine
Keraamilise trumli katmine kulumiskindla polümeeriga
Märgjahvatamine
Solvendi eemaldamine:
Odavaim meetod filtreerimine – lahustuvad komponendid ( ja nanoosakesed) eemaldatakse koos vedela faasiga
Aurustamine pihustus-kuivatamisel (kui H2O)
Pihustatakse ja kuivatatakse kuuma gaasi joas
Sobilik kuumatundlike materjalide korral
Aurustamine lahtisest anumast ahjus – lahustuv materjal „kilena“ pinnal ning võivad sadeneda välja suured rasked osakesed
Levinuim solvent H2O:
Sobiva puhtusega saadaval madala hinnaga
Mitte-süttiv ja ohutu
Puudus: tugevalt hüdreeritud pinnaga pulbri keemiline aktiivsus väiksem (kui järgneb reaktsioon, paagutamine)
Eelis: Hüdrofiilsete mineraalide (nt silikaadid) jahvatamine efektiivsem vesikeskkonnas kui vedelates süsivesinikes – pinna vabaenergia väheneb märgumisel
Märgjahvatamine vs kuivjahvatamine
Märgjahvatamise eelised:
Lihtsam eraldada jahvatatud materjali täidisest,
Kuivjahvatamise korral elektrostaatiliselt tõmbunud kuulide pinnale
Intensiivsem ja kiirem
Seletatakse pinna defektide (osakeste lõhkumisel tekkinud „radikaalid“) küllastumisega vee molekulide abil – küllastumine + osakestevaheline veekiht soodustavad osakeste lagundamist
Puudused:
Solvent tuleb eraldada
Vedela faasi molekulid adsorbeeruvad pinnale
Kuivjahvatamise käigus saab segust üle suunatud õhujoa abil eemaldada peeneid osakesi
3. Vibroenergia veski, „Attritor“ veski ja jugaveski pulbri töötluseks (kirjeldus, eelised-puudused)
Vibroveski
Põhimõte:
Veski trumlis - 90% jahvatuskuule + jahvatatav materjal
Trummel vibreerib (amplit. < 5 cm, 10-20 Hz)
Eelised:
Jahvatamine palju kiirem
Osakeste suurus reguleeritav
Näiteks kuulide suurusega (3 mm Al2O3 kuulidega saab pulbri osakesed 1-3 µm)
Suurem tootlikkus sisendvõimsuse kohta
Väiksed hoolduskulud – vähe liikuvaid detaile, kulumiskindlast metallist, keraamilisest materjalist või elastomeerist väljavahetatav kate
Puudused:
Kuulid kuluvad ning saastavad materjali
Ilmselt kallim kui kuulveski
Tekkivate osakeste suurusjaotus on üsna lai
Kuule on vaja rohkem kui kuulveskis
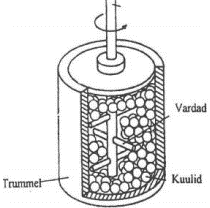 „ATTRITOR“ VESKI
„ATTRITOR“ VESKI
Pulbri jahvatamine toimub vertikaalses kuulidega täidetud trumlis, mille keskel keerleb külgvartega telg
Jahvatamine toimub materjali ning jahvatuskuulide omavahelise hõõrdumise ning põrkumise käigus
Eelised:
Kiire osakeste suuruse vähenemine
Hea energiakasutus
Saadakse väga peened osakesed: d < 1 µm
Kiire ning efektiivne -> Vähem saastumist
Puudus:
Vajab vesijahutust
JUGAVESKI
Pulber kantakse jahvatuskambrisse kiires õhujoas, millele vastu juhitakse teine õhujuga.
Osakesed purunevad põrkumisel ning juhitakse jaotuskambrisse, kus tsentrifugaaljõu abil eraldatakse peened osakesed, suured suunatakse uuesti jahvatamisele.
Sisestatava pulbri osakeste suurus peab olema ≤10x soovitud lõpp-mõõtmetest
Gaas – tavaliselt suruõhk, oksüdeerimise vältimiseks kasutatakse N2 või Ar
Kandajsk võib lisaks gaasile ka vedelik olla
Eelised:
Puudub saastumine – pole liikuvaid detaile, minimaalne kontakt kambriga
Ei vaja jahutust
Kitsas osakeste suurusjaotus
Osakeste suurus kuni 1 μm
Puudus:
Vajab eeljahvatamist
4. Tahkefaasi süntees (meetodi kirjeldus koos näitega)
Tahke-faasi süntees - reaktiivide segu (pulbrite) kuumutamine
Saadus on:
Puhas
Homogeenne materjal
Kindla stöhhiomeetrilise koostisega
Kindel tera-/kristalliidisuurusega
Kaks viimast määratud sünteesitingimustega
Reaktsioonikiirus <- reaktsioon tahkes faasis
Molekulid, aatomid, ioonid – peavad difundeeruma tahkes faasis
Osakeste vahel ja seesmiselt
Temperatuuri kasvades difusioon kiireneb
Ioonide difusioonikoefitsiendid tahkes faasis on mitu suurusjärku väiksemad kui vedelas või gaasifaasis – kõrge T vajalik reaktsiooni toimumiseks mõistliku kiirusega
Reaktsiooni ulatuse määrab reageerivate osakeste suurus – mida väiksemad osakesed sama materjali hulga kohta, seda suurem kokkupuutepind reageerivate osakeste vahel ning seda lühem difusiooni kaugus.
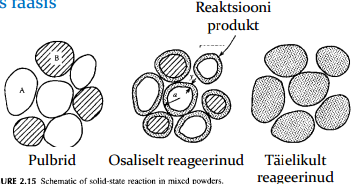
Sünteesietapid koos näitega:
YBa2Cu3O7-δ peene homogeense pulbri valmistamisest
Segatakse eelnevalt jahvatatud oksiidpulbrid Y2O3, BaO2 ja CuO
Stöhhiomeetrilistes hulkades
Kuumutatakse mõni tund u 950 oC juures
Proov jahvatatakse uuesti
saadakse osakesed r ≈ 10 um
Lõhutakse produktist moodustunud pindkiht osakestel
Produkti väliskihti tekivad augud, pole enam vajalik difundeerumine, vaid saab otse pinnal reageerida
Pressitakse tabletiks
Suurendab kontaktpinda
Paagutatakse 950 °C juures
Sulamistemperatuuri lähedal
Tablette kuumutatakse
puhta O2 atmosfääris -> stöhhiomeetriline koostis
500-600 °C juures; järelkuumutamine aitab materjalil paremini kokku paakuda
Materjali mehhaaniline stabiilsus
juhtivate materjalide korral paraneb juhtivus; kontaktpind erinevate osakeste vahel paraneb, st juhtivus paraneb
Jahutatakse aeglaselt toatemperatuurile
Ainult nii saab vältida mõranemist ja purunemist jahutamise käigus
Etappe b) – c) korratakse mitu korda.
Heterogeenne reaktsioon:
Lagunemise reaktsioon – tahket ainet kuumutatakse, et saada uus tahke ühend ning gaas. Kasutatakse lihtsamate oksiidide valmistamiseks karbonaatidest, hüdroksiididest, nitraatidest, jne: CaCO3 (s) CaO (s) + CO2 (g)
5. Prekursor-tehnika homogeense pulbri valmistamiseks (meetodi kirjeldus koos näitega)
1) Valmistatakse homogeenne lähteainete segu (nt mingite oksiidide v soolade pulbrid):
Näiteks lähteainete koossadestamisel (kas hüdrolüüsil või lisades mingit sobivat ühendit lahusesse millega ioonid moodustavad mittelahustuva ühendi/kompleksi)
Koossadestamiseks on vajalik
Lähedased soolade lahustuvused ning sadenemiskiirused
keeruline valmistada puhtaid, spetsiifilise stöhhiomeetrilise koostisega faase, kui ühendite lahustuvused omavahel ei klapi
Vältida sadestunud materjali kihistumist – tuleneb erinevast hüdrolüüsi/sadenemise kiirusest
Üleküllastumine
Eeltoodud etappide juures on oluline tingimuste optimeerimine, kui seda ei tee, siis tekib segu, kus nanotasandil on meil erinevate oksiidide kihid (aga vaja on segu ilma kihistumiseta)
2) Reaktsioon toimub hästi segunenud lähteainete vahel
kuumutamine
Meetodi eelised:
Homogeenne segu
Suur kontaktpindala reageerivate faaside vahel
Ioonid peavad läbima tahkes faasis difundeerudes lühema vahemaa
lühema aeg kuumutamisele
Reaktsioon toimub madalamal T-l
Väiksemate osakestega produkt
NÄIDE
Tahkeoksiid-kütuseelemendi katoodimaterjali, Y3Fe5O12 saaks sünteesida Y2O3 ja Fe2O3 peente, hästi segatud pulbrite stöhhiomeetrilisest segust 1100 °C juures
Reaktsioon on kiirem, kui valmistada tahke segu stöhhiomeetrilises koguses Y(OH)3 ja Fe(OH)3 koossadestamisel Y3+ ja Fe3+ lahustuvate soolade (nitraadid, kloriidid, atsetaadid, oksalaadid, jne) vesilahusest
Kompleksoksiid saadakse prekursor-materjali kuumutamisel 900 °C juures:
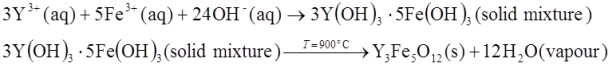
6. Vedel- või sulafaasi süntees (meetodi kirjeldus koos näitega)
Vedelfaasi süntees
Vedelfaasis
Osakeste difusioon kiirem kui tahkes faasis
Lihtsam segada (kiirem segunemine ja massitransport)
Tekib kohe soovitud koostisega tahke sade
mitte järgneval sademe kuumutamisel
Nii vesi- kui ka mittevesilahused
Solvendina kasutatakse ka sulasoolasid, sulametalle (fluxes), ioonseid vedelikke
Näiteid:
PbI2 kiire moodustumine Pb(NO3)2 ja KI lahusest:
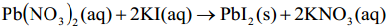
Metallorgaanilised lähteained
Ligandiga nikli nanoklaster L2Ni reageerib alküülfosfiini (R3P) ning alküülfosfiin-telluriidiga (R3PTe) keevas tolueenis (80 °C) mõne tunni jooksul, tekib polükristalliline sade NiTe
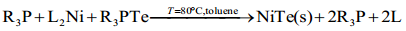
Otsene reaktsioon Ni ja Te pulbrite vahel võtaks mitu päeva kuumutamist 300-400 °C juures
Lisa eelis: Erinevaid metalliklaster-vaheühendeid saab eraldada, muutes reaktsiooni stöhhiomeetria
Sulafaasisüntees
Reaktsioonid või kristallide moodustumine sulafaasis ehk fluksis (soolad, oksiidid, metallid) ei erine oluliselt lahuses toimuvast.
Eelised:
Küllaltki madal aururõhk
Vajadusel võimalik kasutada väga kõrgeid reaktsioonitemperatuure (võrreldes solvendil põhineva keskkonnaga)
Võrreldes tahke-faasi reaktsiooniga on ka siin madalam temperatuur reaktsiooni toimumiseks
Saadakse peente osakestega produkt (suur eripind) ning tekkivate kristallide suurust saab kasvatada süsteemi aeglasel jahutamisel.
Vees mittelahustuva produkti eraldamine lahustuvast fluksist on lihtne.
Produkti saastumist sulasoolaga välditakse valides sulafaasiks ühendid, mille ioonide suurused on väga erinevad produkti ioonidest (PbZrO3 süntees näiteks B2O3 fluksis)
Näide sünteesist sulasoola ja –oksiidi segus:
Granaat (mineraal) Y3Fe5O12 suuri monokristalle saab valmistada:
Granaat lahustatakse sula PbO ja PbF2 eutektilises segus
Süsteem jahutatakse, tekivad kristallid
PbO ja PbF2 lahustatakse äädikhappes (Y3Fe5O12 lahustumatu)
Y3Fe5O12 saab nt välja filtreerida või sadestada
Sulafaasireaktsioonide eriline võimalus:
Reagendid võivad käituda nii solvendi kui ka reaktsioonianumana
Paljusid oksiide sünteesitakse väga kõrgetel temperatuuridel
Nt La2O3 ja Ti2O3 vaheline reaktsioon (produkt LaTiO3), kus mõlema lähteaine sulamistemperatuur on üle 2000 oC – seega on vajalik nn eksootiline anum reaktsiooni läbiviimiseks
Tekitatakse tahke kest reagentidest, mis toimib anumana
Anumana kasutatud reagentide osa eemaldatakse pärast mehhaaniliselt (lõigatakse ümbert ära) ning seda saab kasutada järgmises eksperimendis
7. Tahke faasi ioonjuhtivus – kuidas toimub ning millest sõltub?
Juhtivuseks on vaja palju tsentreid, läbi mille spetsiifilised ioonid saaksid liikuda madala aktivatsioonienergiaga mehhanismil
Kristallvõre defektid (vakantsid)
Tunnelid kristallstruktuuris
Väheasustatud tasandid struktuuris
Nende kõigi kolme puhul on oluline stöhhiomeetria optimeerimine ja osakese suurus
Ioonide suurus ning laeng on olulised:
väiksed ühelaengulised ioonid liiguvad kiiremini, sest mitmelaenguliste ioonide korral tekib kõrge energiabarjäär ümbritsevate ioonide polarisatsiooni mõjul
Oksiididel on tihti mitu kristallilist polümorfi – muundumine ühest teise võib põhjustada mehaanilise degradeerumise, samas ainult kindel struktuur on võimeline ioone juhtima.
Sünteesi käigus võime saada mitu erinevat polümorfi, mistõttu on eriti oluline ühtlane aine jaotus, et ei tekiks erinevaid kihte materjalis.
Veel sarnaseid dokumente
Füüsikalised uurimismeetodid - kordamisküsimused (sarnasus: 26)Eksamiküsimused Aine “Vedelikkromatograafia ja massispektromeetria” jaoks (sarnasus: 24)
Kordamisküsimuste vastused aines Kolloidkeemia (sarnasus: 23)
