Materjalide keemia III kordamisküsimused 2/2
Lisamise aeg:
2015-02-01 13:27:36Vaatamiste arv:
24116Tagasiside:
1 0Kordamisküsimused - Materjalide keemia III 2014/2015
Loeng 8. Õhukeste kihtide valmistamine. Gaasifaasi süntees
1. Õhukeste kihtide valmistamine – kiletõmbamine (tape-casting) ja kalandeerimine (calendering)
Õhukeste tahkete kilede olulisus energeetikas:
Efektiivsemate energiasalvestus-seadmete, sensorite, mikroelektroonika, jne väljatöötamiseks oluline tehnoloogia arengusuund
Näiteid erinevatest kiletehnoloogia rakendustest:
Parem soojusjuhtivus – vähenenud ülekuumenemise oht
Parem elektron- ja/või ioonjuhtivus – väiksem süsteemi sisetakistus
Vähendatud mass ja ruumala
Nanoosakeste pastast õhukese kihi valmistamise meetoditel toimub kihi mõningane kokkutõmbumine – pragunemise oht.
Kiletõmbamine ehk Tape-casting:
Tape casting võimaldab valmistada õhukesi kihte paksusega 1 μm kuni 1 mm ja kuna saadud leht on painduv, on lihtne teda rullile kerida ja ladustada. Selle meetodi suureks eeliseks on võimalus saada suur partii ühtlase pinnaga, ühesuguse paksusega, ainelise koostisega ja jaotusega kihte. Aine peab olema voolisena, mida on lihtne mehaaniliselt mõjutades õhukeseks kihiks viia.
Kõigepealt tuleb pastast lahustunud gaas eemaldada, sest muidu on pärast tape casting’ut toorlehes väikesed augud. Õhumullide poolt tekitatud augud ongi kõige levinumad toorkihi defektid. Lahustunud gaasid saab eemaldada vaakumiga.
Materjali pasta kiht kantakse liikuvale roostevabast terasest kandjale.
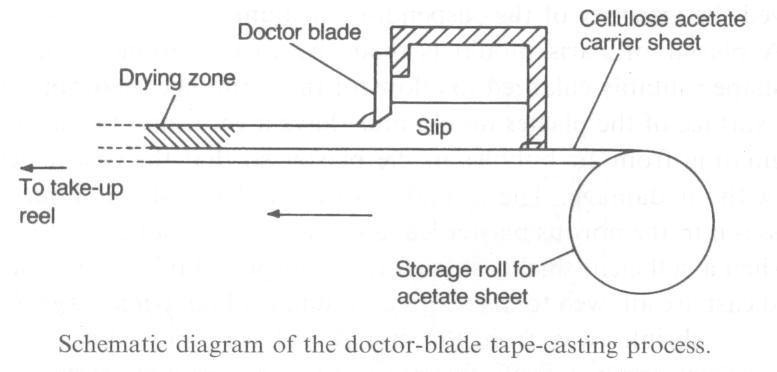 Kandja kannab pasta lõiketera alt läbi. Saadava kihi paksust reguleeritakse lõiketera (doctor blade) kõrgusega.
Kandja kannab pasta lõiketera alt läbi. Saadava kihi paksust reguleeritakse lõiketera (doctor blade) kõrgusega.
Järgmiseks läheb kiht ahju, kus teda kuumutatakse. Solvent aurustatakse kuumutamisega või õhujoa abil.
Saadud kile eelmaldatakse kandjalt.
Pasta koostisosad:
Pulber – väikese osakeste suuruste jaotusega peenike pulber. Pulbrid on tape casting’u puhul kõige olulisemad komponendid. Pärast sideaine eemaldamist ja lõpptöötlemist on pulber ainuke komponent, mis jääb alles ja määrab produkti omadused. Teised pasta komponendid, on selleks, et saavutada soovitud kuju ja tihedusega toorkiht.
Solvent –kasutatakse selleks, et pulber oleks voolis, mida annab viia kahemõõtmeliseks õhukeseks kihiks. Lahusti eesmärk on jaotada kõik komponendid ühtlaselt üle kogu pasta, et saadav kiht oleks võimalikult homogeenne. Enamasti kasutatakse polaarsest ja mittepolaarsest solvendist koosnevat solvendisüsteemi, mis ühelt poolt suurendab komponentide lahustuvust solvendis, teisalt aga võimaldab eemaldada toorkihti lihtsalt kandjalt.
Vesi või orgaaniline solvent (heksaan-etanool, heksaan-etüülatsetaat)
Dispergent -
eraldada ja hoida eraldi pulbri osakesi, et sideaine saaks nendega individuaalselt seonduda,
suurendada pulbri hulka mõistlikel viskoossustel voolises,
vähendada solvendi hulka pastas, nii raha säästmise kui ka kuivamisaja lühendamise eesmärgil ja
põleda välja enne paagutamist, et lõpp-produkt sisaldaks ainult soovitud komponente.
nt Polüakrülaadid, rasvhapped
Sideaine –Kasutatakse kihi kooshoidmiseks. Sideaine määrab toorkihi painduvuse, tugevuse, plastilisuse, lamineeritavuse, vastupidavuse jms, lisatakse eelkõige kõvadele ja habrastele pulbritele.
nt Polüvinüülalkohol
Plastifikaator – kihi plastseks muutmine
Glütseriin, ftalaadid
Paagutamisel (kuumutamisel) tekib poorsus, sest:
Solvent aurustub
Sisaldab kuni 30% orgaanilisi ühendeid, mis põlevad välja
Hoolimata suurest poorsusest kihis, on teatud tingimustel võimalik paagutada tihedaks (isostaatiline kuumpressimine –pressitakse kõigist suundadest)
Saadud kiht on:
mehaaniliselt vastupidav
vastupidav ka järgnevaks töötluseks
aluskihiks sobiiv
Kiletõmbamist kasutatakse:
Li-ioon akude
KE-de,
 superkondensaatorite,
superkondensaatorite,
päikesepaneelide,
sensorite, jne õhukesekihilised funktsionaalsed elemendid
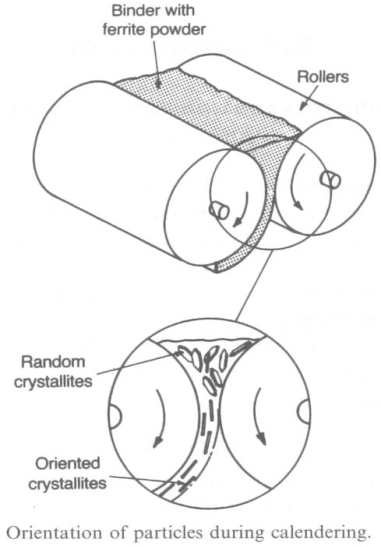
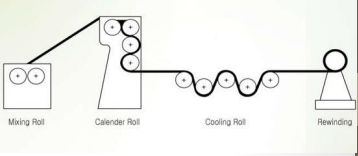
Kalandeerimine ehk valtsimine:
Pulbri ja sideaine segu juhitakse erineva kiirusega pöörlevate roostevabast terasest rullide vahele
Esimene terasrullide paar:
Erinev kiirus tingib segus tugeva hõõrdejõu, lõhutakse aglomeraadid ja hõõrdumisel vabaneb soojus – H2O jahutusega rullid
 Teine terasrullide paar:
Teine terasrullide paar:
Tekitatud kihi paksust reguleeritakse lõpuks teiste, võrdsel kiirusel liikuvate rullide vahelt läbi pressides
Saadav materjal:
Poorsus väiksem võrreldes kiletõmbamisega:
Solvendi aurustumist pole
Pulber hästi dispergeerunud väiksemas koguses sideaines
Saadud kihid on mehaaniliselt vastupidavad
Kihti saab edasi töödelda sarnaselt tape-casting meetodil saadud kihtidele mitmekihiliste seadmete valmistamiseks
Laboratoorsel tasemel saab käsitsi segada pulbri sideainega (tuleb lisada pisut solventi) ning kasutada lihtsama ehitusega rullpressi, et õhukesi kihte valmistada (~100 mm)
Meetodit kasutatakse ka erinevate raskesti segunevatest materjalidest „pastade“ segamiseks – näiteks plast/keraamika, süsinik/metall – millest saab vormida väikseid keeruka kujuga detaile
2. Õhukeste kihtide valmistamine – seguga katmine (slurry coating) ja siiditrükk (screen-printing)
Seguga katmine: Tiheda õhukese kihi valmistamine madala konts.-ga (1-2 vol%) tahke pulbri suspensioonist H2O, EtOH jt orgaanilistes solventides
Katmine pihustamise, voolamise, määrimise, tilgutamise teel
Kaetakse mitu kihti substraadile
Täpselt kontrollitud vahepealne kuivamise etapp
Kattekiht paagutatakse lõpuks koos substraadiga
Substraadi vs. kihi soojuspaisumine – oht praguneda
Kuivanud/paagutatud kiht seostub keemiliselt substraadiga
Sõltuvalt segu koostisest, saab valmistada stabiilseid 5-30 μm kihte.
Polümeeri-segude kihte kuumutades, saab valmistada läbimatuid kihte substraadile. Korrosiooni- ja kuumuskindlad kattekihid, jne
Siiditrükk: Läbi võrgu pressitakse substraadile õhuke materjali kiht, kihi paksus on määratud võrgu paksuse ja avade suuruse poolt (pm võetakse võrk, siis määritakse sinna peale mingit pastat, siis tõmmatakse žiletiga üle selle võrgu nii, et selle pastakiht tuleb täpselt sama paks kui see võrk. Siis võrk võetakse ära ja jääbki pastakiht alles, mis siis pannakse ahju ja see muutub tahkeks)
Erineva mustri/kujuga kihtide valmistamine
Täpsus kihi paksusel kuni 50 μm
Hea reprodutseeritavus
Võrk korduvkasutatav – vähendatud aja- ja rahakulu
Odav ja lihtne meetod
Kasutatakse laialdaselt KEdes kandvale kihile järgmise kihi tekitamiseks
3. Õhukeste kihtide valmistamine – füüsikaline aursadestus ja sputtering
Gaasifaasist sadestamise meetodid on …
Kallid
Keerukad
Saadud kihid kvaliteetsed
Hästi kontrollitav tulemus
Gaasifaasist õhukeste kihtide sadestamise meetodid väga kallid, kuid kihtide kvaliteedi tõttu siiski laialdaselt rakendatud.
Kõige vähem keerukas – füüsikaline aursadestus (PVD)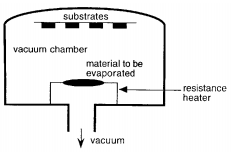
Füüsikaline aursadestus põhineb ainult füüsikalistel protsessidel (aurustumine ja kondenseerumine) ning ei toimu keemilist reaktsiooni materjali pinnal (nagu CVD korral)
Sadestatav materjal aurustatakse laserkiire, kaarlahenduse, raadiosageduse mõjul
Oksiidist, metallist, jt materjalidest „lüüakse välja“ nanoklastreid (säilib stöhiomeetriline koostis).
Aurustatud osakesed sadestatakse sobival substraadil - tekib õhuke kiht
Suhteliselt aeglane meetod - kihi kasvatamise kiirus ~1 µm h-1
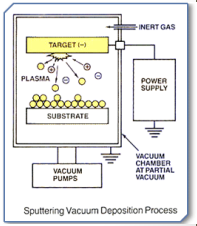 Sputtering:
Sputtering:
PVD meetod, mis kasutab ioniseeritud gaasimolekule materjali atomiseerimiseks
Gaasi-ioonidest ja e – koosnev kõrge energiaga plasma tekitatakse suure pinge rakendamisel madala rõhuga inertgaasile (Ar)
Plasma ioonidega põrkumisel materjal atomiseerub
Eraldatud aatomid sadenevad substraadil
Materjalist välja löödud sekundaarelektronid aitavad plasmat säilitada
Aeglane sadestamine – 0.1 µm h-1
Kasutatakse metallikihtide sadestamiseks.
Kihi tihedust suurendatakse:
Substraadi kuumutamisega (nt alalisvoolu abil)
Sadestatud kihi valgustamine laserimpulsiga
Magnetron sputtering – püsimagnet on aurustatava materjali taga
Sadestamise kiirus – 10 µm h-1ˇ(10 x kiirem kui ilma magnetronita)
Magnetväli hoiab sekundaarelektrone aurustatava pinna läheduses
e – liiguvad spiraalselt magnetväljas, tekitades põrkumisel juurde inertgaasi ioone
plasma säilitamine madalamal rõhul
Kuna aurustatud aatomid on neutraalsed, siis magnetväli neid ei mõjuta
4. Õhukeste kihtide valmistamine – keemiline aursadestus ja elektrokeemiline aursadestus
Keemiline aurustussadestus meetod (CVD)
Õhuke kiht kasvatakse läbi keemilise reaktsiooni substraadi pinnal
Gaasilised reaktandid transporditakse substraadile, kus toimub nende adsorbeerumine ning keemiline reaktsioon pinnal
Veidi kiirem kui PVD (PVD – 1-10 µm h-1)
Hea meetod metallide, metalli oksiidide, karbiidide ja haliidide kihtide sadestamiseks
Saab katta suurt pinda, rakendatav masstootmisena
Aatomkihtsadestus
CVD eriliik, kus õhukese kihi sadestamine pinnale toimub monokihi haaval.
Materjali pinnale lastakse ühte tüüpi gaasilist prekursorit (sadestatavat ainet), mis adsorbeerub ja reageerib materjali pinnaga moodustades sinna monokihi.
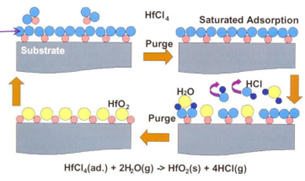 Kui materjali pind on ainega küllastunud (kõik vabad adsorbeerumise kohad on täidetud), siis materjal rohkem adsorbeeruda ei saa ning ülejäänud gaas eemaldataks kambrist.
Kui materjali pind on ainega küllastunud (kõik vabad adsorbeerumise kohad on täidetud), siis materjal rohkem adsorbeeruda ei saa ning ülejäänud gaas eemaldataks kambrist.
Seejärel lastakse kambrisse teist gaasilist prekursorit, mis on võimeline reageerima eelmise aine kihiga. Tekib uus monokiht.
Selliseid tsükleid korratakse, kuni saadakse soovitud arv kihte. Erinevad gaasid pole kunagi kambris üheaegselt, vaid alati kõigepealt üks ja siis teine.
Suurim eelis on see, et saadakse väga ühtlane kihi paksus ja kihi paksust saadakse väga täpselt kontrollida tsüklite arvu järgi (mitte reaktsiooni aja järgi nagu CVD-s üldiselt)
Reguleeritavad tingimused soovitud omadustega kihi saamiseks
Reaktant-gaasid
Termiline stabiilsus (töövahemik 100-1000 °C)
Piisav aururõhk efektiivseks substraadile transpordiks
Kättesaadav kõrge puhtusega
Ei tohi anda kõrvalreaktsioone (substraadiga, kambri seintega)
Kandjagaasi valik ja selle voolukiirus
Rõhk kambris mõjutab
Reaktant-gaaside kontsentratsiooni
Reaktantide difusiooni substraadile ja produktide difusiooni eemale
Madalamal rõhul tekivad ühtlasemad kihid, vähem defekte
Substraadi temperatuur
Tavaliselt kihi moodustumine endotermiline reaktsioon
Mõjutab sadenemise kiirust
Mõjutab sademe struktuuri (kõrgel T kristalne, madal T amorfne)
Elektrokeemiline aursadestus:
EVD on üks CVD vorm, mis kasutab elektrokeemilist potentsiaali-gradienti, et tekitada poorsele substraadile õhukese ioon- või elektrijuhtivusega metalloksiidi kihi (1-100 µm).
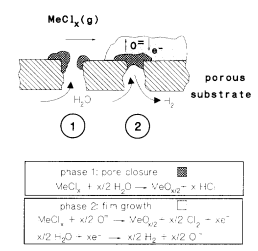 See koosneb kahest etapist:
See koosneb kahest etapist:
Esimene etapp: tavalise keemilise aursadestuse teel (reageerivad MeClx ja H2O aurud) suletakse poorid. Kui poorne pind on oksiidide sadenemise teel suletud, siis pole lähteaine aurud enam teineteisega kontaktis ja keemiline reaktsioon ei saa enam toimuda. Siis tekib gaaside kontsentratsioonide erinevus - ühel pool rõhk suur, teisel pool väike.
Teine etapp: Kihi kasv jätkub elektrokeemilise potentsiaaligradiendi tõttu. Oksiidikiht jätkab kasvamist metalliühendi pool, sest veeauru poolel tekkinud O2- ioonid difundeeruvad O2 rõhugradiendi tõttu läbi oksiidikihi. Seal O2- ioonid reageerivad metallkloriidi auruga ja sadenevad oksiidina.
Kihi kasvamise kiirus pöördvõrdelises seoses kihi paksusega
KE tehnoloogias kasutatakse seda elektrolüüdi või vahelüli kihtide sadestamiseks
Loeng 9. Detailide vormimine ja paagutamine. Poorsete materjalide valmistamine
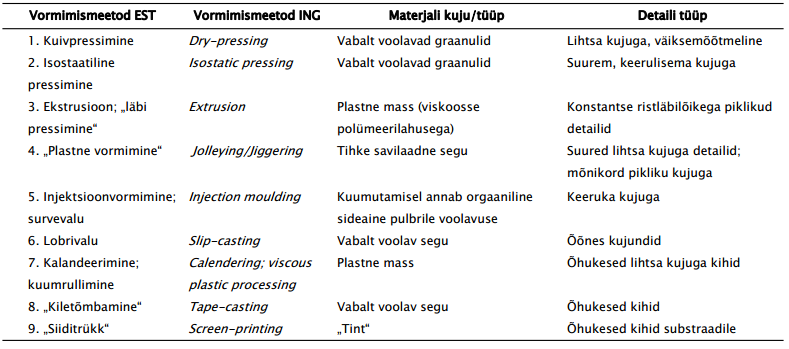
1. Detailide valmistamine – kuivpressimine ja isostaatiline pressimine
Kuivpressimine:
Detail pressitakse vormis liikuvate stantside vahel:
Stantside vahemik täidetakse materjali pulbriga (graanulitega)
Graanulid ei tohi agregeeruda – peavad „vabalt voolama“
Graanulid paiknevad vormiga ühendatud mahutis
Pressitakse kokku fikseeritud ruumala või rõhuni (75-300 MPa)
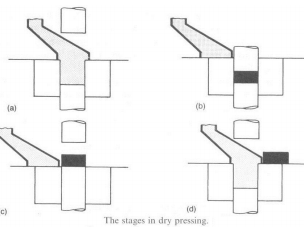 Sobiv meetod lihtsate ühtlaste mõõtmetega detailide valmistamiseks
Sobiv meetod lihtsate ühtlaste mõõtmetega detailide valmistamiseks
Graanulite suuruse varieerumisel segregeerumine ja tiheduse varieerumine
Lisatakse pulbrilist määrdeainet (nt. Ca-stearaat):
Lihtsustatud graanulite voolavus
Vähendatud hõõrdumine pressiga
Hõõrdumisel saastumise vähendamiseks kasutatakse kõrgpoleeritud vormi ja stantse
Nt karastunud teras
Kontrollitud pressimise kiirus – pulbri keskel oleva õhu väljapääsemine ja risk praguneda pressimise suunaga risti
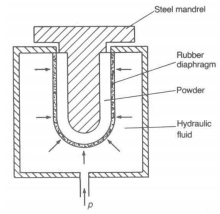
Isostaatiline pressimine:
Painduvas konteineris hüdrostaatilise rõhu abil pressimine
Pulber asetatakse kummi-(plast-)kotti, mille keskele asetatakse jäik sobiva kujuga südamik
p ≥ 280 MPa rakendatakse läbi vedel- või gaasifaasi
(pm pulber, millest tahket objekti tahetakse valmistada, pannakse plastikkotti, siis pannakse see mingi kindla kujuga vormi ja siis pannakse see vorm veeanumasse. Pumbaga pumbatakse sinna anumasse vett juurde ja seega rõhk tõuseb ja surub selle pulbri kokku selle vormi kujuliseks. See on hea just seepärast, et surutakse võrdselt kõigist suundadest ja saadakse seeda parem tihedus ning saadakse valmistada ka keeruka kujuga detaile (lihtsalt peab olema vastava kujuga vorm). Vee asemel saab kasutada ka gaasi ja gaasi rõhku tõsta)
 Eelised (vs. kuivpressimine):
Eelised (vs. kuivpressimine):
Minimaalne pulbri liikuvus
Külgseinad puuduvad (hooldusvabadus)
Suuremad ja keerukamad detailid
Jäik südamik
Ühtlasem detaili tihedus
Rõhk erinevatest suundadest
Pulber ei pea olema niivõrd homogeenne
Aeglane rõhu alt vabastamine
Algselt pulbri vahel olnud õhk pressitakse kokku ning kiirel vabastamisel võib lõhkuda detaili
Tihti rakendatakse rõhku teist korda veel
Rakendused
Mitmete keraamiliste detailide masstootmine
Kõrgepinge seadmete isolaatorid ja keraamilised detailid
Kütuseelementide elektroodid ja keraamilised ümbrised, jne
Mõnikord kuivpressimisel valmistatud detaili viimistletakse kuuma või külma isostaatilise pressiga, nt väga tiheda elektrolüüdi kihi valmistamiseks poorsele KE elektroodile
 2. Detailide valmistamine – ekstrusioon, lobrivalu (slip-casting) ja survevalu (Injection moulding)
2. Detailide valmistamine – ekstrusioon, lobrivalu (slip-casting) ja survevalu (Injection moulding)
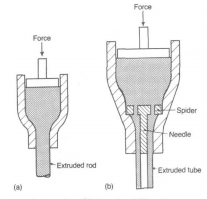
Ekstrusioon:
(pm tehakse mingi pasta, siis see surutakse läbi mingi vormi nii, et teiselt poolt tuleb soovitud kujuga asi välja.. nagu hakklihamasin, kust ühest otsast topid asja sisse ja siis jõu toimel ajad selle aukudest läbi ja saad teise kujuga asja. )
Kasutatakse pideva ristlõikega ning suure pikkus/laius suhtega detailide valmistamiseks (nt igasugu torud)
≥10% keraamika materjalid
pasta valmistatakse H2O-ga segades
Keraamikavabad materjalid
Lisatakse viskoosne vedelfaas (H2O + mõni % tärklist, polüvinüül-alkoholi, metüültselluloosi, jne)
Orgaanilist seepi lisatakse määrdeaine ja märgumise parandajana
Põhjalik segamine vajalik
Pasta surutakse läbi sobiva suurusega aukudega maatriksi
Segu vakumeeritakse kergelt enne surumist, et vabastada õhumullidest
Sideaine – pressitud detail piisava mehaanilise tugevusega käsitlemiseks enne kuivamist
Puudused:
Märgatav kokkutõmbumine kuivamisel (ka paagutamisel) vs. isostaatiline pressimine
Raske kontrollida väga täpseid mõõtmeid ilma paagutamis-järgse detaili töötluseta
Lobrivalu:
(Kasutatakse põhiliselt keraamika jaoks: Tehakse valmis „lobri“, mis on pm vedelikus dispergeeritud pulber. See lobri valatakse spets kujuga kipsvormi ning solvent imbub poorsesse kipsi ja vormi sisse jääb alles see tahke kiht. Seejärel seda kuivatatakse ja saadaksegi vastava kujuga detail)
„Lobri“ - pulber (keraamika, metalli nanoosakesed, süsinik) dispergeeritakse vedelikus (üldiselt H2O, EtOH, etüülatsetaat)
Kõrge tahkete osakeste kontsentratsioon (~50 vol%)
Peened osakesed (<10 μm)
 Mudeldetaili järgi tehakse kipsvorm (mõõtmed arvestavad materjali kokkutõmbumist kuivamisel/ paagutamisel)
Mudeldetaili järgi tehakse kipsvorm (mõõtmed arvestavad materjali kokkutõmbumist kuivamisel/ paagutamisel)
Vormi sisepind sile valmistatava detaili kahjustusteta eemaldamiseks
Vormi valatakse lobri
Solvent imbub poorsesse kipsi, jättes tahke kihi
Kui piisava paksusega kiht on vormi sisse kaetud, liigne lobri valatakse välja
Kuivatatakse detail
Suspensioonile lisatakse deflokulante – pulbriosakeste elektrilisi omadusi mõjutatakse nii, et osakesed tõukuksid teineteisega ning ei agregeeruks
Pulbri peeneteralisus (kõrge eripind) kindlustab elektrostaatiliste mõjude domineerimist gravitatsiooni üle
Raskete pulbriosakeste korral saab tõsta lobri viskoossust, et ei toimuks väljasadenemist
Üldiselt kiht piisavalt tihe (≤5% poorsus):
Aeglane solvendist vabanemine aitab osakestel tihedalt pakkuda
Defektide tekke võimalus väike (vs. kuiva pulbri meetodid)
Kasutatakse keeruka kujuga detailide tootmiseks
Al2O3 tiiglid, torud, jne
Si-, Mg-, Zr-oksiidid, Si, SiC+C (samuti kompleksoksiidid)
Metallidest (W, Mo, Cr) ja WC, ZrC, MoSi2 detailid
Survevalu:
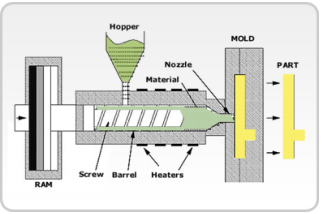 Kasutatakse plastikust keeruka kujuga asjade valmistamise jaoks (ämbrid, prügikonteinerid, igasugu plastikdetailid..).
Kasutatakse plastikust keeruka kujuga asjade valmistamise jaoks (ämbrid, prügikonteinerid, igasugu plastikdetailid..).
Pulber (40-80 vol%) segatakse termoplast-sideainega ja valatakse ühte suurde koonusesse (hopper).
Koonuse all keerleb üks hästi suur kruvi, mis lükkab koonusest tulevat materjali edasi.
Kruvi diameeter lõpupoole suureneb, mis tähendab, et materjal lükatakse rohkem kokku ja samal ajal seda ümbertringi kuumutatakse, seega see materjal muutub plastseks (nii rõhu kui kuumutamise kui ka hõõrdumise tõttu).
Kui see plastne materjal jõuab kruvi lõppu, siis lükatakse see sealt edasi vormi sisse, kus see siis omandab soovitud kuju ja jahtumisel tahkub.
Termoplast-sideaine põletatakse detailist aeglaselt välja
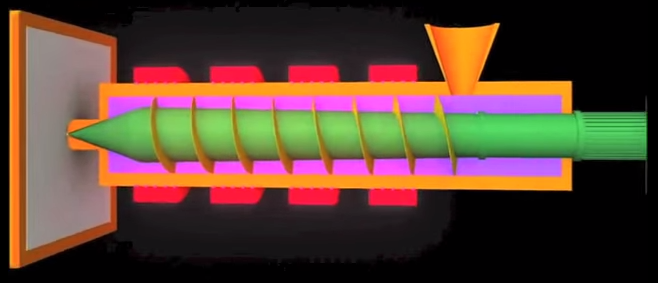 Suurema polümeeri kogus tõttu esineb detailidel:
Suurema polümeeri kogus tõttu esineb detailidel:
Suur poorsus
Märgatavam kokkutõmbumine
Ulatuslikust kokkutõmbumisest (~20%) olenemata hea mõõtmete kontroll
Kasutatakse:
Akude, kütuseelementide, superkondensaatorite elektroodide, piesokeraamiliste muundurite, jne tootmine
3. Materjalide tihendamine – tahkefaasi- ja vedelfaasi-paagutamine
Paagutamine : protsess mille käigus tihendatakse ja tahendatakse materjali kas kuumutamise, ja/või rõhu suurendamise teel ilma, et materjal sulaks päris vedelikuks.
(Nt lumepalli tegemine on rõhu abil paagutamine)
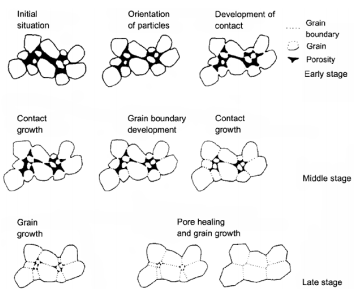 Materjalis olevad aatomid difundeeruvad läbi osakeste piirpindade ja sellega liidavad osakesi teineteisega moodustades ühtse tahkise. Kuna paagutamisel ei kuumutata materjale nende sulamistemperatuurini, siis kasutatakse paagutamist eelkõige just kõrge sulamistemperatuuriga ainete vormimiseks, nt volfram ja molübdeen.
Materjalis olevad aatomid difundeeruvad läbi osakeste piirpindade ja sellega liidavad osakesi teineteisega moodustades ühtse tahkise. Kuna paagutamisel ei kuumutata materjale nende sulamistemperatuurini, siis kasutatakse paagutamist eelkõige just kõrge sulamistemperatuuriga ainete vormimiseks, nt volfram ja molübdeen.
Enne paagutamist on 1-10um suurused pulbriosakesed sideaine poolt koos hoitud, kuid kuumutades hakkab sideaine järk-järgult välja põlema/aurustuma. Samal ajal aga säilib osakeste vahel piisaval hulgal puutepinda, et säilitada kuju.
Tahkefaasi paagutamine:
Materjal kuumutatakse ~0.8-0.9Tsula –ni, sest sellisel temp-l omavad materjali ioonid piisavat liikuvust.
Tihenemine toimub osakeste piirpinna energia vähenemise arvelt. Piirpinna vabaenergia väheneb, sest piirpindu jääb vähemaks (osakesed muutuvad suuremaks) ja kõrge energiaga tahkis-vedelik piirpinnad asendatakse madalama energiaga tahkis-tahkis piirpindadega.
Mida väiksemad on esialgsed osakesed, seda suurem on nende pinna kumerus ja seda suurem on energiamuutus paagutamisel, seega tahetaksegi võimalikult väikseid osakesi.
Tiheda faasi tekkeks vajalik osakese sisemusest difusioon pooride täitmiseks – toimub läbi vakantside tahkise struktuuris.
Vedelfaasi paagutamine
Kasutatakse eelkõige kõrge sulamistemperatuuriga materjalide korral, mille tahkefaasiliseks paagutamiseks peaks kulutama palju energiat.
Pulbrile lisatakse lisand, mis peab sulama enne paagutatavat pulbrit ning milles pulber on veidi lahustuv.
Kui tahkefaasi paagutamisel peab toimuma osakeste transport läbi tahke faasi difusiooni, pinddifusiooni või läbi sublimeerumise/sadenemise, siis vedelfaasi paagutamisel saab kasutada ära "sadeneva lahuse" nähtust:
paagutatavate tahkete osakeste vahel on veidi vedelat faasi, milles tahke materjal osaliselt lahustub. Seega on võrreldes tahkefaasi paagutamisega üks lihtsamini toimuv osakeste transpordi võimalus juures - lahustumine kõrge pinnaenergiaga punktidest ning sadenemine madalama energiaga punkti, näiteks osakeste piirpinna äärde.
Nt paagutatakse vedelfaasis elektrokeraamilisi Al2O3 substraate mikroskeemidele või katalüsaatoritele
Osakeste suurus määrab materjali mehaanilis-elektrilised omadused, seega oluline kontrollida materjali töötluse tingimusi. Mõjutatud:
Lähtepulbris osakeste suurusest (suurusjaotus)
Kuumutamis-režiimist
Keemilisest koostisest
Mõjutatakse osakeste kasvu ja tihenemise kineetikat:
Väga kiirel paagutamisel kõrgel T-l tekivad väikesed tihedad osakesed
Kuumpressimisel saadakse väga tihe faas ilma olulise osakeste suurenemiseta
Tiheda faasi kuumutamisel sobiva režiimiga saab soodustada osakeste kasvu
Esineb dopante, mille lisamisel materjalidele saab kontrollida osakeste suurust paagutamisel
4. Kuumpressimine ja isostaatiline kuumpressimine (kirjeldus, eelised-puudused)
Paagutamist on kahte tüüpi: rõhu all paagutamine ehk kuumpressimine ja rõhuta paagutamine. Mõnel juhul pole võimalik saada poorsusest vaba detaili „rõhuta paagutamisel“
Siis kasutataksegi kuumpressimist, mis on kõrgel rõhul ja kuumusel paagutamine
Kasutatakse eelkõige kõvade ja habraste materjalide jaoks
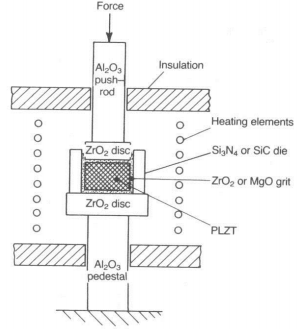 Nt Si3N4 ja SiC korral
Nt Si3N4 ja SiC korral
Keerukas vabaneda poorsusest olulise kristalliitide kasvuta
Selleks kasutatakse paagutamist pressvormis
Rõhk mängib olulist rolli poorsusest vabanemisel
Temperatuur hoitakse kristalliitide minimaalse kasvu vahemikus
Vormi ja stantside materjali valik:
Metallid ei sobi >1000 ˚C – plastsed ning vorm moondub rõhu all, materjal kättesaadav vaid lõhkudes vormi
Erisulameid (enamasti Mo-ga) kasutatakse kuni 1000 ˚C p ~ 80 Mpa
Al2O3, SiC ja Si3N4 kasutatakse <1400 ˚C p ~ 80 Mpa
Grafiiti kasutatakse <2200 ˚C (10 < p < 30 MPa)
1200 ˚C ainult murdosa Al2O3, SiC või Si3N4 tugevusest, kuid kõige tugevam materjal T > 1800 ˚ C
Tekitab redutseeriva keskkonna – vajab kaitset oksüdeerijatest
Kuumpressimine on paljude materjalide tiheda faasi saamiseks ainuke meetod
Isostaatiline kuumpressimine:
Paljude keraamiliste materjalide tootmisel kasutatav protsess, mille abil vähendatakse metallide poorsust ja suurendatakse materjali tihedust. Paranevad materjali mehhaanilised omadused.
Materjalile pannakse nii kõrge temperatuuri kui kõrge rõhuga (avaldatakse isostaatilist gaasirõhku) anumasse. Kasutatav gaas on enamasti Ar. Intertgaas on vajalik selleks, et materjal ei reageeriks sellega keemiliselt. Kambrit kuumutatakse, see põhjustab anumas rõhu kasvu. Kasutatakse ka gaasi juurdepumpamist. Rõhku rakendatakse materjalile igast suunast (e isostaatiliselt)
Paagutamine või järeltöötlus viiakse läbi gaasi või solvendi (H2O, õli) kõrgel rõhul (30-100 MPa)
Ahi ehitatud kõrgrõhu mahuti sisse, kuhu asetatakse objekt
Rakendatakse sobiv N2, Ar või vedelfaasi rõhk ning T tõstetakse sobival režiimil
Pulber või avatud poorsusega detail asetatakse plastsesse läbimatusse ümbrisse
Nt Pt, metallist detailide korral keraamilised materjalid või klaas
Eelised:
Välditud pressi ja materjali vastastikmõju
Võimalik paagutada keerukama kujuga detaile kontrollitud atmosfääris
Pole tiheduse varieerumist vormi seintega hõõrdumise tõttu
Väiksemate detailide korral saab paagutada mitu korraga
5. Poorsete materjalide valmistamise meetodid (4 meetodi kirjeldus omal valikul)
1. Kaltsineerimine fikseeritud T, kus toimub osakeste kasvamine
Jahvatatakse ja selekteeritakse kindla suurusega osakesed
Sellisest pulbrist detailides läbiv poorsus kuni 30 μm avadega
Eripind S BET < 1 m2g-1 – makropoorsed materjalid
2. „Poorimoodustajate“ ehk orgaaniliste ühendite või süsiniku osakeste (d > 20 μm) lisamine keraamilisele pulbrile
Määratud suurusega õõnsused poorimoodustaja väljapõletamisel
>5 vol% avatud poorsuse saavutamiseks
Kontroll struktuuri üle, ei sõltu oluliselt paagutamise tingimustest (kui T paag ~0.8-0.9 T sula)
Saadakse peamiselt makropoorsed materjalid
3. Suure koguse vahutekitit (foaming agent) sisaldava sideaine lisamine
Gaasi eraldumine sideaine-pulber voolisest, mis tahkub sideaine polümerisatsioonil
Poorsus võib olla pidev või katkendlik, olenevalt sideaine koostisest ning muutub vähe väljapõletamisel ja paagutamisel
Suuri õõnsusi sisaldavad materjalid (kuni mõni mm)
4. Eksisteeriva poorse struktuuri reprodutseerimine vaha abil
Nt korallid, vedelkristallid, erinevad 2D ja 3D struktuurid
Kaetakse vahaga ja lahustatakse algne tahkis (CaCO3, vedelkristall)
Poorne vaha kaetakse kontsentreeritud keraamilise pulbri (metalli nanoosakeste, süsiniku, jne) seguga
Vaha sulatatakse ning paagutatakse tekkinud struktuur
Meetod odavam kui katta sobiv tahke vahtstruktuur – materjali struktuur vastab vahu tühimikele mitte pole koopia
5. Selektiivne ühe elemendi oksüdeerimine või redutseerimine keemilisest ühendist – karbiidid, nitriidid, oksiidid 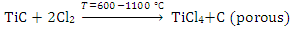
Mikropoorsed materjalid S BET < 2500 m2 g-1
6. Lagundamisel gaase eraldavate ühendite termiline töötlus
CO2 ja N2 eraldumine tekitab meso-makropoorse struktuuri
Nt kompleks-tahkeoksiid pulber, mille SBET ≥ 20 m2 g-1 (a) või SBET ≥ 150 m2 g-1 (b)
7. Selektiivne keemiline või elektrokeemiline lahustamine
NiAl või NiZn selektiivsel lahustamisel poorse Ni-katalüsaatori süntees
Stöhhiomeetrilised Ni ja Al pulbri kogused sulatatakse Aratmosfääris, et saada mikroheterogeenne segu või NiAl tahk lahus
KOH või NaOH vesilahust saab kasutada Al selektiivseks lahustamiseks NiAl sulamist
Al(s) + OH-(aq) + 3H2O ? [Al(OH)4]-(aq) + 3/2H2(g)
Poorset Ni-katalüsaatorit kasutatakse
Metaani reformimisel
Benseeni hüdrogeenimisel (mittepolaarne solvent, tööstuses nailoni tootmise lähteühend, kalorimeetri standard)
H2 salvestamiseks Ni pindkihis
Loeng 10. Vesinik kütusena. Vesinikku salvestavad materjalid
1. H2 kui kütus võrdluses nn tavapäraste kütustega
Fossiilsete kütuste asemel elektrienergia tootmiseks H2 kasutamine eeldab efektiivsete H2 salvestamise tehnoloogiate väljatöötamist
H2 eelised:
Suur energiasisaldus, 243 kJ/mol
Kerge
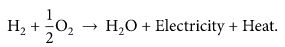 Ei teki kahjulikke heitgaase energia muundamisel – tekib ainult vesi (ei teki kasvuhoonegaase jne)
Ei teki kahjulikke heitgaase energia muundamisel – tekib ainult vesi (ei teki kasvuhoonegaase jne)
Kasutatav sarnaselt teistele kütustele (õlid, gaasid)
Muundatav otse elektrienergiaks
Vesinik on kõige levinum element maakeral – rohkem saadaval kui fossiilkütused
• Võtmetegur – leida tehnoloogia H2 salvestamiseks võimalikult kergelt ja kompaktselt
H2 puudused:
Hind – vaba H2 ei eksisteeri looduses, vaid seda saab vee elektrolüüsil, mis on väga kallis.
puuduvad nö vesiniku puurkaevud
Praegused elektrolüüsiprotsessid vajavad rohkem energiat, kui saaks sealt tuleva H2 põletamisel.
Kuigi vesinikul on kõrge energiatihedus massi kohta, siis on tal paraku madal energiatihedus ruumala kohta võrreldes süsivesinikel põhinevate kütustega. Seega ongi vesiniku salvestamine üks suurimaid takistusi vesiniku kütusena kasutamisel, sest kõrgrõhuga mahutid on suured ja rasked.
Et suurendada energiatihedust ruumala kohta on mõttekas H2 hoida vedeliku kujul. Aga ka vedelikuna on selle tihedus 4x väiksem kui bensiinil ja seega on sama energiahulga jaoks vaja palju suuremaid mahuteid.
Lisaks sellele nõuab vedeliku kujul hoidmine aga väga madalaid temperatuure (keemistemp -253 C) ja kõrget rõhku.
seega on see väga süttimis- ja plahvatusohtlik
vedeldamisel on suur energiakadu
hästi isoleeritud mahutid on kallid ja rasked
Ohutusprobleemid:
H2 -õhk segu süttib kergelt
Lekkimisoht kiire difusiooni tõttu
Materjalide vesinikrabedus
2. H2 surugaasi, veeldatud H2 ja hüdriidide/poorsete materjalide võrdlus – eelised-puudused
H2 surugaas:
Kerge kuid mahukas vs. süsivesinikud
Sama energiahulga kohta vaja suuremaid ja raskemaid mahuteid
Süsinik-fiiber mahutid kerged, kuid ülikallid..
Tugevamkokkusurumine nõuab energiakadu
7.2% HHV-st (H2 heating value) kulub 1000 kg H2 kokkusurumiseks rõhule 20 MPa (200 bar)
Suru-H2 mahutid vesinikautodes rõhul 350-700 bar
Ohutusprobleemid:
H2 - õhk segu süttib kergelt
Lekkimisoht kiire difusiooni tõttu
Materjalide vesinikrabedus
Vesinikhaprus on nähtus, kus metall (nt roostevaba teras) muutub vesinikuga kokkupuutel hapraks. Seda põhjustab metallivõre defektidesse difundeerunud vesinik, mis avaldab materjalile seesmisi lisapingeid.
Väike H2 molekul tungib enamik materjalidest läbi (sealhulgas teras)
Pragude hargnemine viib rabeduse tekkeni
Vajab pidevat hooldust
Täieliku purunemise oht
Vedel H2:
Surugaasiga võrreldes suurem tihedus
Krüogeensetel tingimustel (keemistemp –253 °C)
Vedeldamisel suur energiakadu
Hästi isoleeritud mahuti on kallis (ja raske).
Mitte-korrossiivne, seega materjalile ainukesed nõuded vastupidavus madalale temperatuurile ja H2 läbimatus
~4x väiksem volumeetriline energiatihedus vs süsivesinik-kütused (bensiin)
Süttimis- ja plahvatusohtlik.
Piisavalt külm atmosfäärist O2 vedeldamiseks (või tahkumiseks) – kontsentreeritum.
Väga väike energia vajalik süttimiseks segus O2-ga

Metallhüdriidide tehnoloogia:
MHFC eelis: vesiniku salvestamine on võimalik rakus endas absorbeerituna metallhüdriidide komponendiks. Nagu vesi ja nuustik, nii on ka hüdriidid võimelised absorbeerima vesinikku, mida vabastatakse aeglaselt vesiniku konts-i vähenmisel keskkonnas. Absorptiooniulatus on u 2%, seega FC-d ei pea välja lülitama selleks, et kütusepaaki vahetada (saab lühiajaliselt ise hakkama).
Madalam rõhk ja H2 endotermiline vabanemine – ohutuim
Vabanev H2 ülipuhas – kasutatav otse tundlikes kütuseelementides
H2 on kõige tihedam, seega saab hakkama väiksemate konteineritega
miinus: madal efektiivsus
| Salvestusmeetod |
Volumeetriline H2 mahtuvus (kgH2 m–3) |
Probleemid |
| Suru-H2 rõhul 80 MPa |
~40 |
Ohutus ↑p tõttu; kokkusurumise hind; mahutite vesinikrabedus * |
| Vedel H2 –252 °C krüogeenses mahutis |
~71 |
Suured soojuskaod; ohutus; vedeldamise hind |
| Tahkefaasiline hüdriid |
80–160 |
Mitte ükski eelnevatest |
3. Nanostruktuursetes materjalides vesiniku salvestamine (kuidas toimub, näited materjalidest, eelised-puudused)
2 liiki H2 salvestavaid nanostruktuurseid materjale:
1.Dissotsieerivad materjalid
H2 molekulid dissotsieeruvad aatomiteks, mis seostuvad materjali struktuuriga (kemosorptsioon)
Nt. metallhüdriidid
2.Mitte-dissotsieerivad materjalid
Tänu mikropoorsele struktuurile ja suurele eripinnale salvestatakse H2 molekul-pind vastastikmõjude abil (füüsikaline sorptsioon)
Nt. Süsiniku ja boornitriidi (BN) nanostruktuurid, klatraadid*, metallorgaanilised struktuurid, jne
 klatraat on keemiline ühend, mis koosneb üht tüüpi molekuli võrestruktuurist, mille sees on „kinnipüütud“ teist tüüpi molekul
klatraat on keemiline ühend, mis koosneb üht tüüpi molekuli võrestruktuurist, mille sees on „kinnipüütud“ teist tüüpi molekul
Adsorptsiooni tsentrid nanomaterjalides:
Väline pind (adsorptsioon)
Osakeste piirpind
Absorptsioon materjali sisemusse
Nanomõõtmetes materjal mõjutab tugevalt H2 absorptsiooni ja dissotsiatsiooni termodünaamikat ja kineetikat:
Difusiooni vahemaa väheneb
Difusiooni kiirus kasvab
Väikse massiga süsteemid, mille H2 salvestusvõime on suurem
H2 -salvestus süsinik-nanomaterjalides
Süsinikmaterjalide atraktiivsed omadused gaaside salvestamiseks:
Adsorptsiooni-võime
Suur eripind
Pooride mikrostruktuur
Väike tihedus (kerged)
Palju looduslikke sünteesi lähtematerjale
Füüsikaline sorptsioon (Van der Waals’i jõud)
Limiteeritud <1 H/2 C(<4.2 m%)
Sideme-energia ~0.1 eV
Kemosorptsioon (C kõrgeima hõivatud molekulaarorbitali kattumine H elektroni hõivatud lainefunktsiooniga, ületades H2 dissotsiatsiooni aktivatsiooni energiabarjääri)
Kuni 2 H /1 C(16.5 m%)
Sideme-energia 2-3 eV
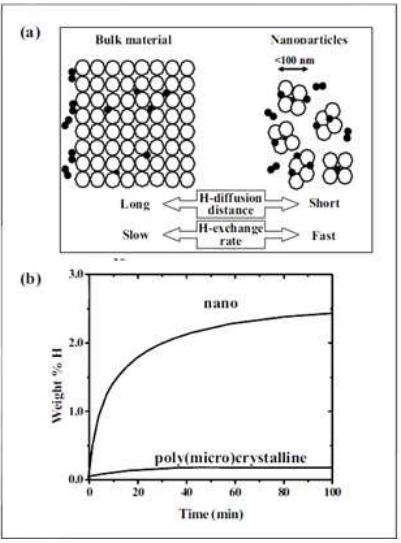
A major bottleneck in the ongoing research in this area is the effective and efficient storage of hydrogen. Nanomaterials offer great promise. Storage and retrieval of hydrogen involves an important phenomenon called ‘sorption’. Adsorption and desorption are the two processes involved and the associated thermodynamics is vital in the design and optimization of the materials for hydrogen storage.
Nanoparticles help promote fast hydrogen exchange by shortening diffusion distances for hydrogen. This is facilitated by the increased porosity and smaller size leading to increased diffusion-limited rates. Surface energies and materials properties at the nanoscale help tune the energetics of adsorption and desorption to reduce the release temperature and hasten the release process.
Näited materjalidest:
H2 -salvestus poorses süsinikus
CDC-de unikaalsed omadused gaaside salvestamiseks:
Kitsas poorijaotus
Eripind kuni 2000 m2 /g
Kuni ~80% avatud poorsus
Mõõdukas hind
Odavam vs. CNTs, ligilähedane hind sünteetiliste aktiveeritud süsinikega
Palju erinevaid lähtekarbiide: B4 C, ZrC, TiC, SiC, VC, WC jne.
Kõik erineva poorse struktuuriga
H2 -salvestus nanotorudes
SWCNT-de H2 salvestusvõime toatemperatuuril teoreetiliselt 3-10 m%
Väga kerged
Väikeste mõõtmetega – suure eripinnaga
Eesmärk suurendada H:C suhet ja tugevdada H–C sidet 300 K juures
H2 -salvestus metallorgaanilistes ühendites
Metal-organic frameworks(MOF) on sünteetilised kristalsed mikropoorsed ühendid
Koosnevad metalli ioonidest või klastritest, mis on ühendatud orgaaniliste molekulidega (linkeritega)
Metalli ja linkeri valik mõjutab struktuuri ja omadusi:
Metalli koordinatsiooniarv mõjutab pooride suurust ja kuju, määrates ligandide arvu ja suuna
H2 mahtuvus kuni 4 m%(-195 °C)
Toatemperatuuril ~1 m%
Väga suure poorsuse tõttu volumeetriline mahutavus probleem
4. Füüsikalised hüdriidid (vesiniku salvestamise/vabastamise mehhanism, van’t Hoffi võrrand + kirjeldus, hüdriidide näited ning nende plussid-miinused)
Metallid ja sulamid, mis absorbeerivad pöörduvalt vesinikku
Klassifitseeritakse kui A, A2B, AB, AB2 ja AB5, kus
A on siirdemetall (nt Ti, V), haruldane muldmetall (La, Pr,Gd, Sm) või Mg
B on Al, Cr, Co, Fe, Ni or Mn
Metallhüdriidide (MH) kasutamise eeldus – võime füüsikaliselt adsorbeerida/absorbeerida ning vabastada H2 mitmeid kordi ilma materjali degradeerumiseta
Absorptsioon – vesinik absorbeeritakse materjali sisemusse (mitte ainult pinnale)
MH struktuuris toimub atomaarse H sisenemine kristallograafilise struktuuri vahemikesse
H2 kõigepealt adsorbeerub dissotsiatiivselt pinnale.
H difundeerub nanostruktuursesse tahke A või AB jne. Faasi.
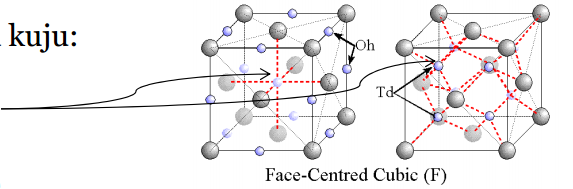 „Lahustunud aatomid“ võtavad kuju:
„Lahustunud aatomid“ võtavad kuju:
Juhuslik tahke lahus;
Korrapärane hüdriid-struktuur
Mõlemad suure volumeetrilise pakketihedusega
H2 hulka väljendatakse hüdriidi molaarse või m% koostisena
Volumeetriliselt võib olla H-sisaldus sama kõrge kui vedelas H2
Absorptsioon üldiselt eksotermiline.
Maksimaalseks H2 mahtuvuseks tuleb jooksvalt soojust eemaldada.
Absorptsioon/desorptsioon tasakaal määratud H2 rõhuga
Kui T= const korral p>ptasakaal -> moodustub hüdriid
Alla ptasakaal H2 vabaneb ja metall/sulam pöördub algsesse olekusse
ptasakaal sõltubT-st– ↑ptasakaal kui↑T
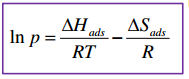
Van Hoffi võrrand:
?Hads varieerub oluliselt erinevatel materjalidel
?Sads küllaltki sarnane
Kindla MH van’t Hoff’i graafik (lnp vs. 1/T) on lineaarne – annab kasulikku infot H2 absorptsiooni/desorptsiooni kohta
Optimaalse MH säilitus-Tjärgi jaotatakse füüsikalised hüdriidid 3 gruppi:
Kõrg-temperatuursed (HT)
Kesk-temperatuursed (MT)
Madal-temperatuursed (LT)
LT kategooria parimvalik „tavakasutuseks“ kütuseelemendi H 2 allikana
Vajalik soojus H2 desorptsiooniks tuleb kütuseelemendi jääksoojusest
Näited:
LaNi5 Absorbeerib vesinikku pöörduvalt, moodustades LaNi5H6.5 (AB5 sulam)
Mahtuvuse parandamiseks asendada La võrepunkti väike kogus Zr või Ti ja Ni asemel Al, Cr, Co, Mn, V
Hüdriid moodustub tava-T
Reaktsiooni ?Hon madal (31 kJ/mol H2 )
Pole vaja suurt soojushulka anda desorptsiooniks
Mitusada tsüklit ilma vesiniku mahutavuse vähenemiseta
Absorptsiooniga kaasneb materjali ulatuslik paisumine,mis viib peeneks puruks pragunemiseni, kuid sellega suureneb eripind ja kineetika paraneb
La on agakallismetall
Hüdriid sisaldabainult 1,5 m% H2
Veel näiteid füüsikalistest hüdriididest: MgH2, Mg2NiH4, VH2, TiFeH1.5
5. Komplekshüdriidid (vesiniku salvestamise/vabastamise mehhanism, näited hüdriididest, katalüsaatorite mõju, struktuuri mõju)
Metallhüdriidid (nt MgH2, NaAlH4, LiAlH4, LiH, LaNi5H6, TiFeH2 ja pallaadiumhüdriid) on kasutatavad vesiniku salvestamiseks (erineva efektiivsusastmega), seda tihtipeale pöörduvalt. Mõned on lihtsasti kütustena kasutatavad tavatemp-l ja rõhul, mõned on tahked ja toodetakse graanulitena. Eelised: hea energiatihedus ruumala kohta. Puudus: energiatihedus kaalu kohta väga väike.
Enamik metallhüdriide seostuvad H2-ga väga tugevalt. Sellepärast on H2 vabastamiseks vajalik kõrge temp-i rakendamine. Seda energiakulu on võimalik vähendada kasutades sulameid, mis koosnevad nõrgast ja tugevast hüdriidimoodustajast: nt LiNH2, LiBH4 ja NaBH4. need moodustavad vesinikuga nõrgema sideme, seega vaja rakendada madalamat energiat salvestatud vesiniku vabastamiseks. Puudus: kui interaktsioon on liiga nõrk, siis vesniku taassalvestamiseks vajalik väga kõrge p, mis nullib energiasäästu.
Alternatiivne viis dissotsiatsioonitemperatuuri vähendamiseks on aktivaatoritega dopeerimine. Seda kasutatakse Al-hüdriidi puhul (puudus: keeruline süntees ja raske vesiniku taassalvestamine -> vähekasutatud).
Komplekshüdriidid - H salvestatud keemilise sidemena lahustuvates soolades M+[AHX]-
M – Na või Li (Mg)
A - B või Al
H2 vabaneb soolade termilisel lagundamisel
Reaktsioonid on pöörduvad ainult ↑p ja ↑T tingimustel
H2 salvestamiseks „alanaadid“ Na[AlH4] ja Na3[AlH6] eelistatumad
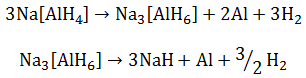 Lagunemine kahes astmes:
Lagunemine kahes astmes:
1 aste: 50-100°C, vabaneb 3,7 m% H2
2 aste: 130-180°C, veel 1,9 m% H2
Ti-katalüüsitud Na[AlH4]on termodünaamiliselt sarnane klassikalistele madaltemperatuursetele hüdriididele (nagu TiFeH, LaNi5H 6) – H2 salvestamise/vabastamise T katalüsaatori mõjul madalam
Kui kasutada kas või ainult 1. astet, siis Na[AlH4] H-mahutavus massi kohta on rohkem kui paljudel AB, AB2 võiAB5 madaltemperatuursetel hüdriididel
Katalüsaatorite mõju:
Nanokatalüsaatoritega komplekshüdriidid:
The enhancement of reaction kinetics at low temperatures and the requirement for high hydrogen storage capacity (>6.0 wt%) of hydrogen storage materials could be made possible by catalytic doping. If nanostructured materials with high surface area are used as the catalytic dopants, they may offer several advantages for the physicochemical reactions, such as surface interactions, adsorption in addition to bulk absorption, rapid kinetics, low-temperature sorption, hydrogen atom dissociation, and molecular diffusion via the surface catalyst. The intrinsically large surface areas and unique adsorbing properties of nanophase catalysts can assist the dissociation of gaseous hydrogen and the small volume of individual nanoparticles can produce short diffusion paths to the materials’ interiors. The use of nanosized dopants enables a higher dispersion of the catalytically active species [35] and thus facilitates higher mass transfer reactions.
Suure eripinnaga nanostruktuursete katalüsaatoritega dopeerimise eelised:
Adsorptsioonitsentreid veel juures lisaks absorptsioonile
Kiirem kineetika
Sorptsioon madalamal T-l
Lihtsustatud H2 dissotsiatsioon
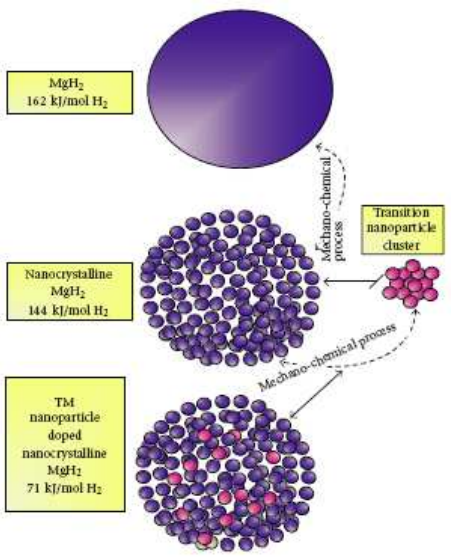 Nanomõõtmetes katalüsaator dispergeerub paremini ning aitab kaasa massiülekande protsessidele
Nanomõõtmetes katalüsaator dispergeerub paremini ning aitab kaasa massiülekande protsessidele
Struktuuri mõju:
MgH2 (de)hüdrogeenimise reaktsioon väga aeglane ja suur H. Vaja kõrget T
Kineetika parandamiseks:
Jahvatamine nanokristalliliseks pulbriks. Tekitab pinnadefekte (kõrgem pinna-energia) ja suurendab eripinda – endotermiline lagunemine juba mad. T-l
Vesiniku vabastamine toimub termilisel lagunemisel. Kui jahvatada peeneks pulbriks ehk tekitada juurde pinda, pinnadefekte, siis mida rohkem seda on, seda madalamal temperatuuril toimub vesiniku vabastamine.
Nanokatalüsaatoritega segamine, toob temperatuuri alla, sest metalli nanoosakesed annavad juurde sorptsiooni aktiivtsentreid.
6. Keemilised hüdriidid (vesiniku salvestamise/vabastamise mehhanism, näited hüdriididest, eelised-puudused)
H2 eraldumine toimub hüdriidi keemilisel reaktsioonil H2O-ga. Kõrgetel temp-del stabiilne – H2 eraldamine termilisel aktivatsioonil ei sobi
Pöördumatud reaktsioonid, kuid! 50% H2 hulgast tuleb H2Ost – „vee lõhustajad“ (water-splitting agents) 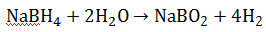
Hüdriidi saaks säilitada seguna mineraalõli ja dispersandiga
Õli moodustab kaitsva kihi peente (~20 mm) hüdriidi osakeste pinnal
Õli reguleerib reaktsiooni kiirust vee ja hüdriidi segamisel
Dispersant takistab osakeste suspensioonist väljasadenemist
Kaitsekiht võimaldab ohutut säilitamist õhukeskkonnas ilma O2 ja veeauruga kokkupuuteta
Nt: CaH2, LiAlH4, LiH, LiBH4, KH, MgH2, NaH
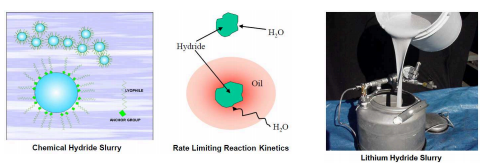
Keemiliste hüdriidide miinuspool: hüdriidi regenereerimine
Massi, ruumala ja hinna poolest siiski atraktiivne H2-salvestamise meetod kütuseelemendi-autodele.
Palju sõltub ümbertöötluse keerukusest ja hinnast
7. H-sisaldus erinevates hüdriidides, hüdriidide süntees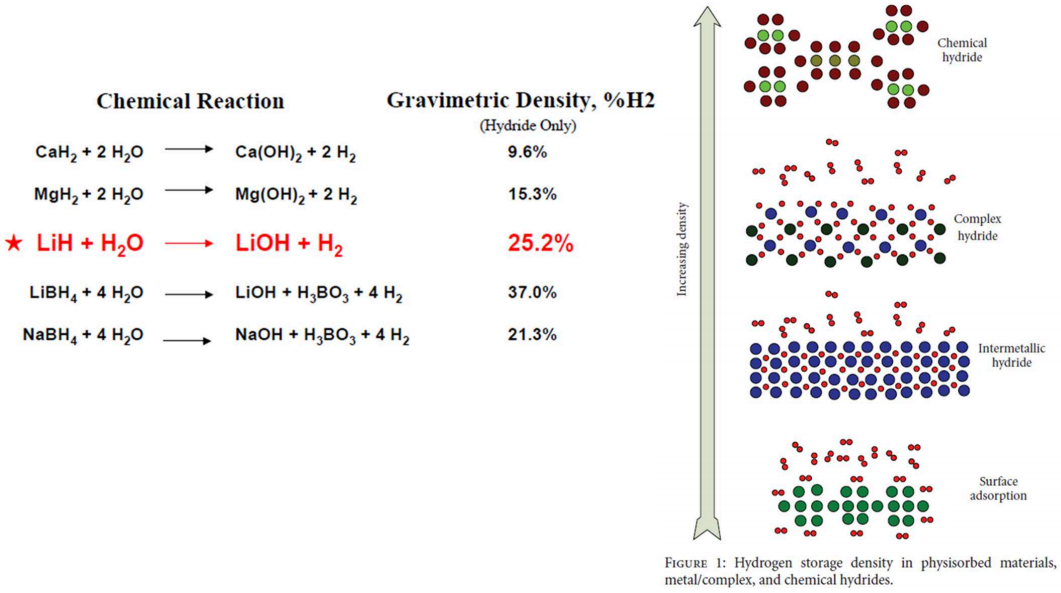

Kompleks- ja keemiliste hüdriidide süntees
Üldiselt metall + H 2 reaktsioonil, aga võimalik ka H2O või hüdroksiidiga reaktsioon:
Füüsikaliste metallhüdriidide (LaNi5 , TiFe, jne) süntees
Mehaanilisel metallide legeerimisel/sulandamisel (mechanical alloying)
Jahvatatakse kuulveskis metallid, kuum isostaatiline pressimine ja järelkuumutus
Kaarlahendusega või induktsioon-ahjudes metallide sulatamisel
Metalloksiidide, -hüdroksiidide, -kloriidide, -karbonaatide segude redutseerimine H2 või inertgaasi atmosfääris

Loeng 11. Masstootmises patareid ja akud
1. Patareide/akude tööpõhimõte, töövõime hävinemise põhjused, olulised omadused
Energiasalvestusseadmed, milles toimub keemilise sideme energia muundamine elektrienergiaks läbi spontaansete elektrokeemiliste reaktsioonide. Akudes on elektroodideks erinevad elektrokeemiliselt aktiivsed ühendid mitmetes erinevates elektrolüüdi lahustes, mis võtavad tihti ise osa toimuvatest elektroodireaktsioonidest.
Laadimine ja tühjenemine
Aktiivmaterjalidega toimuvaid protsesse esitatakse elektrokeemiliste reaktsioonivõrranditega. Tühjenemisel ühel elektroodil oksüdeerumine, teisel redutseerumine. e – liiguvad (–) (+) elektroodile läbi välise vooluahela. NB! Elektrivoolu suund defineeritud (+) (–). Laadimine on protsesside teistpidi suunamine välise vooluallika abil.

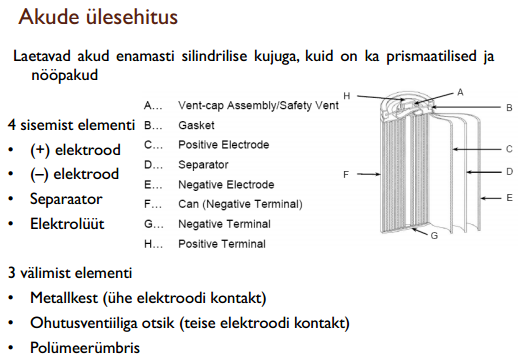
Töövõime hävinemise protsessid:
Aktiivmaterjali tihenemine:
poorsuse vähenemine takistab kättesaadavust elektrokeemiliseks reaktsiooniks
Aktiivmaterjali paisumine ning pudenemine elektroodiplaadilt
Mitteaktiivsete faaside moodustumine:
Tekivad kõrvalreaktsioonil, lagunemisel;
Elektriliselt isoleerivad piirkonnad materjalis
Metalsete nõelte sadenemine:
Lühistumise oht
Voolukollektorite korrosioon:
Suurenenud sisetakistus
Ülelaadimisel gaaside teke elektroodidel:
Läbilöögi efekt
Olulised omadused:
Eluiga
Aku eluea definitsioon – täieulatuslike laadimise/tühjenemise tsüklite arv enne aku mahtuvuse langemist <80% algsest nimiväärtusest
Stabiilne pinge väärtus tühjenemisel
Aku töötamisel on oomiline pingelang (IR)
IR suureneb kõrgetel võimsustel ning sisetakistuse kasvades, kui elektroodireaktsiooni produktid kogunevad ning takistavad edasist reaktsiooni
Kunagi ei lasta akul nö täielikult tühjeneda – tühjenemise pinge alumine piir oleneb vastavast akust
Kõrge energiatihedus (Wh kg-1) ja võimsus (W kg-1)
Lai töötemperatuuri vahemik
Aeglane iseeneslik tühjenemine
Iseeneslik tühjenemine – voolutarbija puudumisel elektroodireaktsioonide iseeneslik toimumine
Kiirelt laetav
Ülelaadimise ja ületühjenemise vastupidavus
Usaldusväärne töötamine
Hooldusvaba
Ohutu (ka õnnetuse olukorras)
Valmistatud kättesaadavatest, odavatest ning keskkonnaohututest materjalidest
Tööea lõppedes materjalide taaskasutus/ümbertöötlus
2. Galvaanielemendi termodünaamika, Nernsti võrrand
Termodünaamika II seadus:
G = H – T S
G < 0 protsess/keemiline reaktsioon toimub spontaanselt produktide moodustumise suunas
Reaktsiooni toimumisel püstitub elektroodide vahel potentsiaalierinevus (rakupinge E)
Pöörduva reaktsiooni max elektriline töö:
w max = G (T,p = const.)
Vajalik energiahulk n elektroni ülekandeks pingel E:
w = nF E
Seega, spontaansel reaktsiooni vabaenergia:
G = -nF E
Galvaanielemendis: G < 0 ja E > 0
S = – (∂G/ ∂T)= nF(∂E / ∂T) nFdE /dT
H = G + T S = –nF E + nFTdE /dT

Nernst’i võrrand reaktsiooni nullvoolupotentsiaali arvutamiseks. Saab hinnata reaktsiooni pöörduvust.
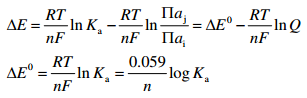 ΔE 0 – standard-potentsiaal (+) ja (–) vahel nullvoolu tingimustes, kui kõigi ühendite (ioonide) aktiivsus a = 1
ΔE 0 – standard-potentsiaal (+) ja (–) vahel nullvoolu tingimustes, kui kõigi ühendite (ioonide) aktiivsus a = 1
3. Patareid (näited koos elektroodireaktsioonidega, eelised-puudused)
Leclanché element:
(–) Zn Zn2+ + 2e–
(+) 2MnO2 + 2H2O + 2e– 2MnOOH + 2OH– ΔE 0 = 1.26 V
C lisatakse MnO2 juhtivuse parandamiseks
ZnCl2 elektrolüüt – absorbeerunud (+) poorides ja pasta-separaatoris (nt. tärklis) – “kuiv rakk”
Zn käitub ka kestana ülejäänud elementidele
Eelised:
Odav
Puudused:
Lühike säilitusaeg (kiire iseeneslik tühjenemine)
Suurel voolutihedusel kiire pingelangus
Rakendused:
Taskulambid, suitsuandurid, uksekellad
50 aastat tagasi enamik patareisid
Zn-Mn leelispatarei:
Edasiareng Leclanché elemendist:
Konts. KOH (~30%)
Zn elektrood peene pulbri kujul
Raku ülesehitus vastupidine: MnO2 segu Zn ja separaatori ümber, elektrilises kontaktis nikeldatud teras-kestaga
Eelised:
Kõrgem efektiivne mahtuvus
Madalam töötemp.
Pikem eluiga >4 aasta 20°C (‘fit and forget’ applications)
Väiksem lekkimisoht vs. Leclanché
Puudused:
Kallim
Rakendused:
Mänguasjad, pardlid, kaamera välk, kellade patareid, jne.
Olemas ka laetavate akudena
Liitium-patareid
(–) Li – e– Li+
(+) Mitmed erinevad (MnO2, CFx, MoO3, V2O5 jne.)
Elektrolüüt: LiPF6 või LiBF4 lahus orgaanilises solvendis (propüleenkarbonaat, dimetoksüetaan)
Li orgaanilises solvendis stabiilne tänu korrosiooniproduktidest tekkivale kihile
tahke kaitsekiht, mis takistab edasist solvendi pindreaktsiooni
Eelised:
Suur rakupinge ~3.0 V
Kõrge energiatihedus
Aeglane iseeneslik tühjenemine
Lai töötemperatuuri vahemik
Väga kerge
Rakendused:
Back-up mälu, südamestimulaatorite, kellade, kaamerate, kalkulaatorite patareid
4. Plii-akud (elektroodireaktsioonid, erinevad konstruktsioonid, eelised-puudused, rakendused)
Pliiakud:
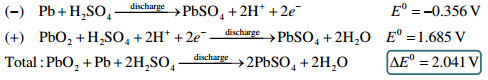
Elektrolüüt, H2SO4 võtab osa elektroodireaktsioonidest
Aku laetudolekut saab määrata elektrolüüdi tiheduse järgi.
Tühjenemisel H2SO4 H2O
250-1000 tsüklit, mõjutatud:
Temperatuurist
Töötamine >50 °C vähendab 50%
Tühjenemise ulatus
Keskmiselt tühjenemine ulatuslikumalt – lühem eluiga
Disainitud tühjenema 50–80% ulatuses
Efektiivne laadimise:tühjenemise aegade suhe 5:1
Rakendused:
Sõidukite aku
Tööstus-seadmed (tööriistad)
Stand-by/back-up süsteemid (UPS)
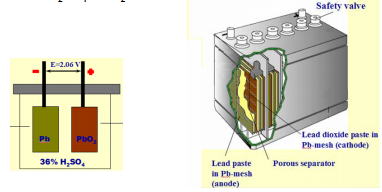
Pliiaku „ujutatud“ disain:
Selle disainiga akud nö avatud ning elektroodide kõrvalreaktsioonidel tekkivad gaasid pääsevad välja.
Mahtuvus sõltub tühjenemise võimsusest!
Eelised:
Odav
Vastupidav ka lühiajalisel optimaalsest režiimist väljaspool töötamist
Head tööomadused nii kõrgel kui madalal temperatuuril
Puudused:
?E > 2.39 V vesi laguneb H2 ja O2 – “gaseerimis-pinge“
↓?E kui ↑T
Nõuab elektrolüüdi monitoorimist
H2 ja O2 eraldumisel süsteemi avadest suures koguses tekib süttimisoht
Happelahuse aurustumisel on korrosioonioht aku ümbrusele
Pliiaku ventiil-reguleeritud disain:
Nö kinnine süsteem, mis reguleeritud ventiilide abil
Elektrolüüt fikseeritud absorbent separaatoris (klaasfiiber) või geelis (SiO2)
Eelised:
Suuteline töötama suurte vooludega
Katalüütiliselt O2 tagasi veeks (~85% ef.)
(+) protsess laadimisel aeglasem – seal oksüdeeritakse veest O2 , mis katoodil redutseeritakse ning seotakse PbSO4
Vee kadu süsteemist väike – hooldusvaba
Takistab korrodeerivate gaaside eraldumist
Odav
Puudused:
Lühem eluiga
Tundlikum temp. muutustele ja ülelaadimisele/-tühjenemisele
Kiire iseeneslik tühjenemine
Pb raske – madal energia- ja võimsustihedus
Pb mürgine – regulatsioonid keelamiseks
5. Leelisakud: Ni-Cd vs. Ni-MH (elektroodireaktsioonid, eelised-puudused, rakendused)
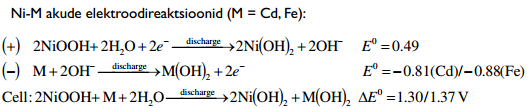
Rakendused:
Elektroonika (kalkulaatorid, kaamerad, lap-topid, taskulambid, jne)
Elektri-/hübriidsõidukid
Militaar- ja kosmoserakendused
Raudtee-tööstus
Stand-by võimsus tööstuses ja elektrienergia tootmises
Eelised:
Koormusele reageerimisaeg mõni ms, annab kohe maksimaalse võimsuse
Efektiivne nii kõrgel kui madalal temp.
Püsiv tühjenemise pinge
Hea tsükleeritavus (<3500 tsüklit)
Ükskõik millises laadimisastmes võib seisma jätta
Kiirem laadimine vs. pliiaku
Puudused:
Kallis
Keskkonnamõju – toksiline lahustuv Cd
Cd raske metall
“Mäluefekt“ – põhjustab akut säilitama väiksemat energiahulka
Kättesaadav energiahulk väheneb, kui korduvalt laadida ainult osaliselt tühjenenud akut
Aku „mäletab" väiksemat mahtuvust
Võib säilitada –20 kuni 40 ˚ C
>32 ˚ C iseeneslik tühjenemine kiirem – eelistatud <21°C
Ni-metallhüdriid:(+) Ni(OH)2
(–) vesinik salvestatuna metallhüdriidis (MH)
Kasutatakse 2 tüüpi MHsid:
AB5 (A – La, Ce, Nd, Pr, Gd segu; B – Ni, Co, Mn, Al)
Eeliseks aeglasem iseeneslik tühjenemine
AB2 (A – Ti ja/võiV; B – Zr või Ni, modifitseeritud Cr, Co,Fe ja/või Mn)
Eeliseks suurem energiatihedus
Metallhüdriidides H absorbeerumine ekso- või endotermiline
Akule halb – soovitav ilma soojusefektideta elektroodireaktsioon
Sobivad ekso- ja endotermiliste hüdriidide homogeensed sulamid
Rakendused:
Elektroonilised seadmed (tööriistad, algselt mobiilides ja laptopides samuti)
Avariivalgustus
Elektrisõidukid (veel demonstratsiooni järgus)
Eelised:
Püsiv rakupinge tühjenemisel
30% suurem mahtuvus vs. Ni-Cd
25% suurem võimsus vs. Ni-Cd
Võimeline andma suuremat hetkvõimsust
Hea tsükleeritavus
Puuduvad toksilised komponendid (Cd, Pb)
„Mäluefekt“ puudub
Puudused:
Kallis (isegi rohkem vs. Ni-Cd)
Kiirem iseeneslik tühjenemine
Kõrgemal temp. aeglasem laadimine
Seotud MH soojusefektiga
6. Li-akud (põhimõte, erinevad variandid, elektroodimaterjalid, eelised-puudused, rakendused)
Li eelised elektroodi materjalina:
Väga kerge
Kõrge redutseerumispotentsiaal E° = -3.05V
Atraktiivne (–) elektrood
Suurem energiatihedus (Wh kg-1 ) vs. teised metallid
Puudused:
Ei saa kasutada H2O keskkonnas
Dendriitide moodustumine laadimisel
Võimalikud elektrolüüdid:
LiPF6 , LiBF4 , LiClO4 orgaanilistes solventides (karbonaadid,γ-butürolaktoon, jne.)
Polümeerelektrolüüdid
Ioonsed vedelikud
Keraamilised materjalid
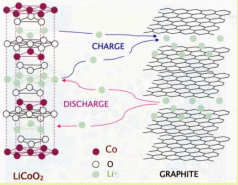 Kasutatakse interkaleerumis-elektroode:
Kasutatakse interkaleerumis-elektroode:
Interkalatsiooni all mõeldakse seda, et liitium ioonid saavad siseneda ja väljuda aine kihtide vahelt ilma, et aine kristallstruktuur muutuks.
Grafiiti kasutatakse anoodina seetõttu, et liitiumi interkalatsioon grafiidile võimaldab head reaktsiooni pöörduvust väga madalatel potentsiaalidel.
Aku tühjenemise ja laadumise protsessid on jägmised:
Laadimine: LiCoO2 + C6→ Li1-xCoO2 + C6Lx
Tühjenemine: Li1-xCoO2 + C6Lx → LiCoO2 + C6
Aku pannakse kokku „tühjenenud“ olekus
Li+ interkaleerumine grafiiti on kiirust limiteeriv protsess
Eelised:
~4.0 V tõttu salvestavad Li-ioon akud rohkem energiat vs. Ni-MH/Ni-Cd (1.2 V)
Samal töörežiimil pikem kestvus laadimiste vahel
Aeglasem iseeneslik tühjenemine vs. Ni-akud
Hooldusvabadus
Püsiv pinge tühjenemisel
Mingi hetk järsem langus, ei tühjendata alla 3 V
Puudused:
Kallis
Ülelaadimine või soojenemine >100 °C lagundab (+)
Vajalik kallite kaitsemehhanismide lisamine
Veega kokkupuutel (–) süttib koheselt
Madalam võimsus vs. Ni-akud, eriti madalal temp.
Li-polümeer
kõrge dielektrilise konstandiga polümeerid suudavad lahustada Li-soolasid. Polümeer võimaldab pakkida seadme ruumalasse kokku suurepinnalise süsteemi (mitu m2) – suure summaarse voolu. Rullitud silindriks või volditud kokku. Vedeliku puudumise tõttu pole vaja rasket kaitsvat ümbrist
Valmistatakse õhuke polümeerikiht. Kaetakse (–) Li-fooliumiga, komposiit (+) elektroodiga ja voolukollektoritega.
Eelised:
Odavam tootmine vs. Li-ioon
Palju erinevaid võimalusi disainis
Mehaanilisel vigastusel väiksem süttimisoht
Kerge
Vastupidav
Esimeste seadmete piirangud:
Vajalik töötemp. 80–120 ˚C
Küllaltki väike eluiga
Kiirem mahtuvuse vähenemine vs. Li-ioon
Laadimisel samad nõuded, mis Li-ioon aku korral
Hoida kuivas kohas temperatuuril –20 kuni 30 °C
Pikemaajalisel säilitamisel 10 kuni 30 C°
Otsesest päikesevalgusest eemal
Säilitada laadimisastmel 40%
Üle tüki aja laadimisel võib võtta mitu tsüklit nominaalse mahtuvuse saavutamiseks
Rakendused (Li-ioon ja Li-polümeer):
Elektroonika seadmed – praktiliselt kõik mobiilid, laptopid, jne
Elektrisõidukid
Li-ioon/radikaal
Elektroodiks orgaaniline molekulaar-radikaal
Orgaanilisi radikaale saab stabiliseerida keemilise töötlusega tava-T pikaajaliselt eksisteerimiseks:
Radikaali tsentri steerilise stabiliseerimisega
Resonantsstruktuuridega, milles paardumata elektron osaleb
Eelised:
Radikaal-polümeeri elektritakistus väike – väga kiire laadimine (30 s)
Geeli kasutamisel väga paindlik
Rakendused:
Polümeeridel põhinevate Li-akude nišši rakendused üliõhukeste akuplaatidena (näiteks ümber randme keeratavad telefonid jne)
| Aku tüüp |
Suhteline hind |
Raskus |
Temp (ºC) |
Eluiga (tsüklit) |
Säilitusaeg (kuud) |
Tööpinge (V) |
| Pliiaku |
X |
Väga raske |
-15 – 50 |
180+ |
6 |
2.0 |
| Ni-Cd |
2X |
Raske |
-20 – 65 |
500+ |
6 |
1.2 |
| Ni-MH |
2.5X |
Mõõdukas |
-10 – 60 |
500+ |
12 |
1.2 |
| Li-ioon |
4X |
Kerge |
-10 – 60 |
500+ |
12 |
3.7 |
| Li-polümeer |
5X |
Kerge |
-10 – 60 |
500+ |
12 |
3.7 |
Loeng 12. Arendusjärgus olevad akud
1. Leelisakud: Ni-Zn ja Zn-õhk (elektroodireaktsioonid, eelised-puudused, võimalikud rakendused)
Ni-Zn:
Zn on atraktiivne (–) elektroodiks:
Kõrge elektroodi potentsiaal
Kõige elektropositiivsem tavalistest H2O lahusest sadestavatest metallidest

Võimalikud rakendused:
Kandidaat elektrisõidukitele
Stand-by energiaallikas
Eelised:
Kerge (Zn vs Cd või MH)
Energia- ja võimsustihedus suurem vs. pliiaku, Ni-Fe või Ni-Cd
Väike sisetakistus – atraktiivne kiire laadimise/tühjenemise tõttu
Puudused:
Zn lahustuvus KOH-s – vähendab eluiga ja mahtuvust
Näidatud kuni 500 tsüklit
Dendriitide moodustumine laadimisel (ka (+) elektroodil)
põhjustab aku lühistumist
Zn-õhk:
Sarnane kütuseelemendiga – kütuseks Zn peene pulbri segu KOH-ga
Tühjenemisel Zn oksüdeerub (–) elektroodil – [Zn(OH)4 ]2- , mis omakorda laguneb lahuses ZnO-ks:
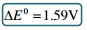
Uudne kahest aspektist:
Gaasiline(+) aktiivühend (hapnik)
„Mehaaniliselt“ laetav
„Mehaanilise“ laadimise eelised:
(+) aktiivmaterjal piiramatus koguses kättesaadav
Mõne minutiga teostatav
Mitte-mehhanilise laadimise probleemid:
Zn dendriitide moodustumine
O2 reaktsioon halvasti pöörduv
Laadimise pinge palju suurem – tsükli efektiivsus ainult 50%
Rakendused:
Elektrisõiduki veojõu-aku prototüübid testitud
Ühekordsed Zn-õhk patareid kasutusel kuulmisaparaatides
2. Läbivoolu-akud (põhimõte, erinevad variandid, elektroodireaktsioonid, eelised-puudused, võimalikud rakendused)
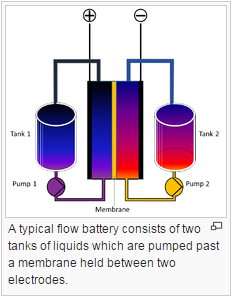 Läbivoolu-akud üldiselt
Läbivoolu-akud üldiselt
Kaks erinevat elektrolüüdilahust, lahused membraaniga eraldatud
Toimub ioonvahetus (tekitab elektrilaengu voolavuse), mis toimub läbi membraani samal ajal, kui mõlemad lahused tsirkuleerivad oma ruumiosas.
elektrolüüt sisaldab ühte või eneamat elektrokeemiliselt aktiivset osakest (võtavad osa elektroodireaktsioonidest või võivad adsorbeeruda elektroodi), mis voolavad läbi elektrokeemilise raku, mis pöörduvalt toodab keemilisest energiast elektrienergiat.
Osa elektrolüüdilahusest ladustatud eraldi (sarnasus KEga) mahutitesse, seda pumbatakse läbi raku pidevalt.
Ehk siis tegu tavalise elektrokeemilise rakuga (aku), aga ekelektrolüüdilahust hoitakse väljaspool akut ennast, mitte elektroodide ümber akus. Elektri tootmiseks söödetakse elektrolüüdilahust rakku väljastpoolt. Kogu toodetava energia hulk sõltub mahutite suurusest.
Läbivoolu akude ja osalt ka hübriidakude eelised:
Paindlik disainivõimalus
Pikk eluiga (pole faaside vahelist ülekannet -> tahkis-tahkis)
Kiire reageerimine koormusele
Emissioonivaba
Madal hoolduskulu
Kiire laadimine vahetades elektrolüüdi vedelikku
Puudused: keerukad vs tava-akud, vajavad pupmasid, sensoreid jmt, energiatihedused üldiselt madalad vs Li-ioon aku
Ühest küljest akude omadused:
Laetav
Laadimisel/tühjenemisel metallikatioonide oks/red (või mingite anioonide)
Samas sarnased kütuseelementidele:
Reageerivaid ühendeid hoitakse akuseadmest väljaspool
Mahtuvus (energiahulk) määratud reagentide reservuaaride suuruse poolt
Energia ja võimsus on teineteisest eraldatud
Elektroodid saab disainida maksimaalseks võimsuseks (katalüütilised, elektrilised ja transpordi omadused) ilma vajaduseta samaaegselt energiatihedust optimeerida
suhteliselt odav suuremahuline energiasalvestus hoolimata madalast gravimeetrilisest ja volumeetrilisest energiatiheusest
Separaatoriks mikropoorne plast või ioonselektiivne polümeer
(+) ja (–) omavad elektrolüüdi läbikande süsteemi, millega reageerivad ühendid kantakse elektroodi pinnale
Redoks-läbivooluaku – reagendid lahustunud elektrolüüdis
Pöörduv KE, elektrokeemilised komponendid elektrolüüdis lahustunud.
Energia sõltumatu võimsusest, kuna kättesaadav energia hulk sõltub ainult elektrolüüdi ruumalast, võimsus aga elektroodi pindalast ja omadustest, sisetakistusest
Erinevad ioonid (nt. Cr2+ ja Fe3+) või sama ioon erineva o.-a.-ga(nt. V3+ and V5+)
Nt vanadium-redoksaku, broom-polüsulfiidredoksaku
Hübriid-läbivooluaku – vähemalt üks aktiivmaterjal aku sees, toimub faasimuutus (mitte lihtsalt o.-a. muutus)
Üks või enam elektroaktiivsetest materjalidest on tahke kihina aku sees -> toimub faasimuut
Sellisel juhul koosneb rakk pm ühest akusarnasest elektroodist ja ühest KE elektroodist (kütus väljast). Kättesaadav energiahulk piiratud elektroodide pindalaga.
Nt Zn–Br2 hübriid-läbivooluaku
Eelised (nii hübriidi kui redoksi)
Kiire reageerimine koormuse muudatusele
Puudub vajadus moodulisiseselt rakkude omavahelist reguleerimist
Hübriid-aku korral skaleerimine piiratud
Hooldusvaba
Vastupidavus ülelaadimisele ja ületühjenemisele
Ability for deep discharges without affecting cycle life
Puudused:
Vaja keerulisi pumpasid, sensoreid
Elektrolüüdi voolu regulatsioon
välised reservuaarid
Vanaadium-redoksaku:
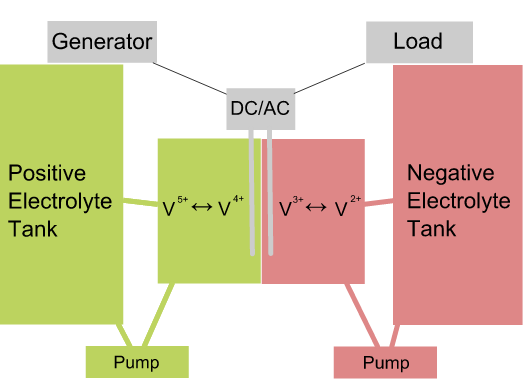 Koosneb:
Koosneb:
rakuruumis elektrolüüdid eraldatud ioonvahetusmembraaniga (prootonid)
kaks mahutit – mõlemad baseeruvad V’l
positiivne mahuti VO2, VO2+
negatiivne mahuti V3+ ja V2+
Põhineb V eksisteerimisel mitmetes o.-a.-des:
4 erinevat võimalikku o.-a.-d
Seega kasutatakse ainult ühte elektroaktiivset materjali kahe asemel
Laetuna (+) ahelas V5+ lahus ja (–) ahelas V2+ lahus
Tühjenemisel V4+ ja V3+
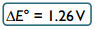
Eelised:
Kõrge eluiga, kuni 15000 tsüklit
Limiteeritud funktsionaalsete detailide materjalide poolt, mitte regeerivate ühendite poolt lahuses
Puuduvad materjali probleemid, kuna reagentide lahused pole korrodeerivad
Piiramatu mahtuvus (reguleeritud mahutite suurusega)
Laetav lihtsalt elektrolüüdimahutite puudumisel
Puudused:
Madal energiatihedus (kuni 25 Wh kg-1)
Pole tõenäoline kandidaat elektriautodele
Võimalikud rakendused:
Taastuvenergia salvestamine
Broom-polüsulfiid redoksaku
Anioonide oksüdeerumine ja redutseerumine mõlemal elektroodil.
+ 2–(+) Br2 lahustunud NaBr lahuses (NaBr3)
(-) Väävel naatriumpolüsulfiidina (Na2Sn)
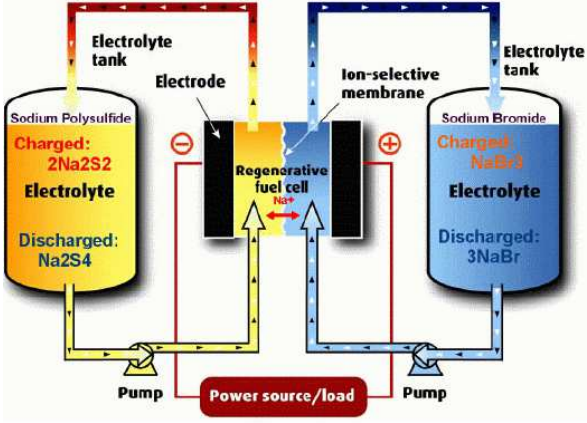
Eelised:
Väga kiire reageerimine koormuse muudatustele
~75% summaarse efektiivsusega
Töötab toatemperatuuril
Puudused:
Töötamise käigus tekib reaktsiooni kõrvalprodukte, mis tuleb paarinädalase intervalli tagant süsteemist eemaldada – seega vajab hooldust
Võimalikud rakendused:
Arendatud suureskaalaliseks energiasalvestuseks elektrijaamades ning elektrivõrgustikus kasutamiseks (koormusühtlustamine
Zn-Br2 hübriid-läbivooluaku
Tühjenenuna mõlemas elektrolüüdiahelas konts. ZnBr2 lahus.
Br2 väga lenduv ja reageerimisvõimeline vedelik– laadimisel tekkiv Br 2 seotakse orgaaniliseks kompleksühendiks (alküül-morfoliinium(/pürrolidiinium)-bromiid) ehk vesilahusega segunematuks õliks
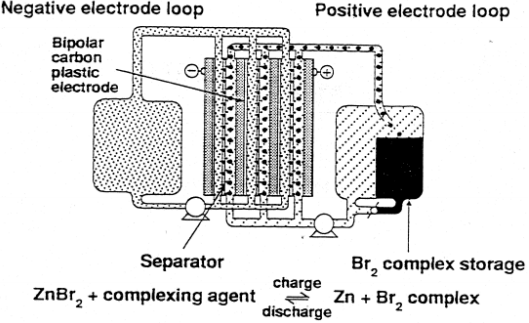
Eelised:
Kõige kõrgema energiatihedusega kõigist läbivooluakudest
Zn sadenemisel (–) ei teki dendriite tänu elektrolüüdi voolamisele
Süsteem koosneb kergetest plastikmaterjalidest
Puudused:
Probleemiks Br2 keemiline aktiivsus paljude plastikute suhtes
Ohutus, kasutades Br 2 näiteks elektrisõidukis ehk tarbekaubas
Võimalikud rakendused:
Elektrisõidukid
Suureskaalalised süsteemid elektrivõrgustikus energia salvestamiseks
3. Naatrium-akud (põhimõte, erinevad variandid, elektroodireaktsioonid, eelised-puudused, võimalikud rakendused)
Termaalaku – kasutab tahket tavatemperatuuril inaktiivset elektrolüüti.
Aktiveerides saab kätte kogu energia väga kiirelt
Sulasoolade kõrge ioonjuhtivus – seetõttu ka suured energia mahtuvused
Na eelised elektroodimaterjalina:
Kõrge potentsiaal E 0 = –2.71 V
Külluslik ja odav
Mitte-toksiline
Kerge
Na probleem:
Väga aktiivne reageerimaks H2O-ga
Na-S aku
Sulatatud soolaga süsteem
(+) elektrood - vedel väävel
Tahke elektrolüüt – keraamiline tuub beeta-alumiiniumiumist
korrosiooniprobleemid
Na+ difundeeruvad läbi elektrolüüdi
Tekib vedela väävliga mittesegunev vedelik Na2S5
2. aste S-elektroodi poolel
Reaktsioonid on pöörduvad
Kõrg-temperatuurne aku, milles vedel Na (–) ja vedel S (+) aktiivmaterjalid
Töötemp. 300–400 ˚C
Paigutatud kuumutusega isoleeritud mahutisse
Elektrolüüdiks keraamiline NaAl2O3 toru, mille sees vedel Na
Vedel Sn paikneb elektrolüüdi ja välise kesta vahel
S puudub elektronjuhtivus, seega paikneb grafiitmaatriksis
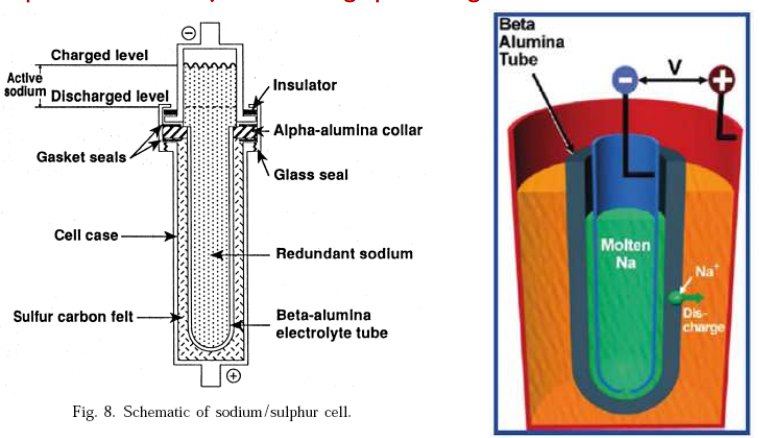
Eelised:
Vedela Na tõttu pole dendriitide moodustumise probleemi
Odavad ja keskkonnasõbralikud aktiivmaterjalid
Hea tsükleeritavus
Kõrge energia ja võimsus
Puudused:
Kuum Na2S3 väga korrodeeriv terase jt sulamite suhtes
Elektrolüüdi pragunemisoht
Süttimisoht
Võimalikud rakendused:
Elektrisõidulik
Kosmoserakendused (satelliidid)
Na-NiCl2 aku (ZEBRA)
Elektrolüüt: aku töötemp-l sula-olekus NaAlCl4 (-) elektrood: sula Na (+) elektrood: Ni (laadimata kujul), laetuna NiCl2 Separaator: kasutatakse sest nii Na kui ka elektrolüüt on töötemp-l sulanud (materjaliks Na juhtiv beeta-almina keraamika)
Eelised Na/S ees:
Pannakse kokku „tühjenenud olekus“
Na moodustub in situ
Ni (ja NiCl2) kättesaadav ja odav
Pole tõsiseid korrosiooniprobleeme
Kahekordse terasümbrisega elimineeritud ohutusprobleemid
Madalam töötemperatuur 250-350 ˚C
Puudused:
Kõrgel temperatuuril hoidmise vajadus
Keraamilise elektrolüüdi vastupidavus
Võimalikud rakendused:
Test-elektriautod
Suuremahulised stand-by süsteemid
Na-ioon aku
Sarnaselt Li-ioon akudele, on võimalik sünteesida ka mikrostruktuurseid materjale, milles toimub fikseeritud potentsiaalil Na+ ioonide interkaleerumine
Grafiitset süsinikku ei saa Na-ioon akudes (–) elektroodina rakendada, sest Na ei interkaleeru pöörduvalt, kuid paljudesse teise struktuuriga (ebakorrapärastesse, mittegrafitiseeruvatesse) süsinikesse on edukalt Na+ ioone sisestatud
Üks grupp (+) elektroode on Nax MnO2 , mille kristallstruktuuris on tunnelid Na+ liikumiseks. Seda on uuritud erinevate polümeerelektrolüütidega, kuid on näidatud ka, et saab vesilahusest edukalt Na interkaleerida/deinterkaleerida
4. Akude, superkondensaatorite ja kütuseelementide tööpõhimõtte ja sellest tulenevate omaduste võrdlus (energia ja võimsus, ajaline stabiilsus, efektiivsus)
| Akud |
Superkondensaatorid |
Kütuselemendid |
|
| Tööpõhimõte |
Keemilise sideme energia muudetakse elektrienergiaks läbi spontaansete elektrokeemiliste reaktsioonide. Need redoksreaktsioonid toimuvad pikaajaliselt – energia hulk on suur, kuid võimsus väike |
Füüsikaline adsorptsioon elektroodidel. Laadimise käigus toimub elektrostaatiline laengusalvestus - elektroodi pinnale tekitatakse elektriline kaksikkiht. Tühjenemise käigus toimub ioonide desorptsioon, mis tingib suunatud laengute liikumise e elektrivoolu |
Seade, mis muundab kütuse keemilist energiat otse elektrienergiaks. Reaktsiooni kontrollitud suunamisel läbi seadme on võimalik reaktsioonienergiat kasutada efektiivselt elektrienergia tootmiseks. |
| Energia ja võimsus |
Kõrge energiatihedus (kuni 160 Wh/kg), madal võimsustihedus (1-3 kW/kg) |
Energiatihedus on madal (0,5-30 Wh/kg), kuid võimsustihedus suur, isegi üle 50 kW/kg. |
Esineb väga erineva võimsusega KE-sid (kuni 10 MW-ni). Energia- ja võimsustihedus sõltuvad suuresti sellest, millisel kujul on kütus salvestatud. Näiteks hüdriidina salvestatud vesiniku korral võib energiatihedus olla 10 korda suurem kui Li-ioon akul |
| Ajaline stabiilsus |
Eluiga on tüüpiliselt 100-10000 tsüklit. Ühe tsükli laadimise/tühjenemise aeg varieerub minutitest tundideni |
Eluiga on väga pikk, kuni miljon tsüklit. Ühe tsükli laadimise/tühjenemise aeg on lühike, sekundite suurusjärgus |
Ebapiisav eluiga ning usaldusväärsus. Vajavad soojendamist kindla töötemperatuuri saavutamiseks (0,1-10 h) |
| Efektiivsus |
Hea, 50-90% |
Kõrge, 95% |
Mõõdukas, 35-60% (kuid oluliselt suurem, kui sisepõlemismootoril (ca 25%) |
Loeng 13. Füüsikalised energiasalvestussüsteemid (FESS). Tuule- ja geotermaalenergia
Hooratta FESS (põhimõte, kasutatavad materjalid, eelised-puudused)
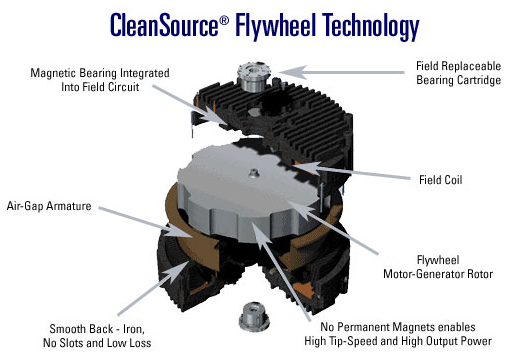
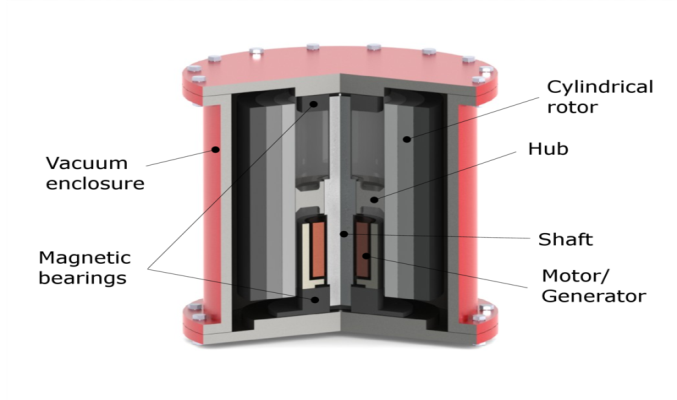
Kuidas töötab?
Hooratta FESS salvestab elektrienergiat hooratta kineetilise energiana (hooratas hakkab kiiresti pöörlema). Kui vaja hoorattast energiat kätte saada, siis generaator muundab osa rootori liikumise kineetilist energiat elektrienergiaks. Seda süsteemi on hea kasutada, kui on karta elektrienergia fluktuatsioone ning meil on vaja elektrienergia stabiilsust suurte võimsuste korral.
Millest koosneb ?
Hooratast, mis ringi liigub elektrimootoris/generaatoris, nimetatakse rootoriks. Mootor on seade, mis teeb elektrienergiat kineetiliseks energiaks. Generaatori puhul on asi vastupidi (toodetakse mehhaanilisest energiast elektrienergiat). Vaakum on vajalik rootori hõõrdumise vähendamiseks. Magnetlaagrite „magnetic bearing“ eelis mehhaanilise ees on rootori „toetamine“ (õhus hoidmine) ilma füüsilise kontaktita, mille tõttu kaob vähem energiat hõõrdumisse. Hooratast tehakse kahest materjalist: süsinikkiust ja terasest. Süsinikkiud on tugevam ja kergem, mille tõttu saab temaga saada suuremaid pöörlemiskiiruseid (võimalik salvestatav energia on võrdeline pöörlemisekiiruse ruuduga).
Eelised:
Kiire mehhanism – kõrge võimsus
Puuduvad elektrokeemilistele seadmetele omased elektrilised kaod
Pikk eluiga -> 20 aastat või kümneid tuhandeid tsükleid
Disaini ja suuruse paindlikkus
Ehitatud kättesaadavatest materjalidest
Perioodilise hoolduse vaba (lihtsasti väljavahetatavad detailid)
Praktiliselt sõltumatu keskkonna temperatuurist
Puudused:
Kõrge valmistamishind
Väike energiahulk
Mehaaniliste laagritega süsteemis hõõrdumine
Magnetlaagrite puhul on kadu suurusjärgu võrra väiksem
Hüdroenergia – pumpjaamad ja jõevoolujaamad (põhimõte, süsteemi kirjeldus, eelisedpuudused)
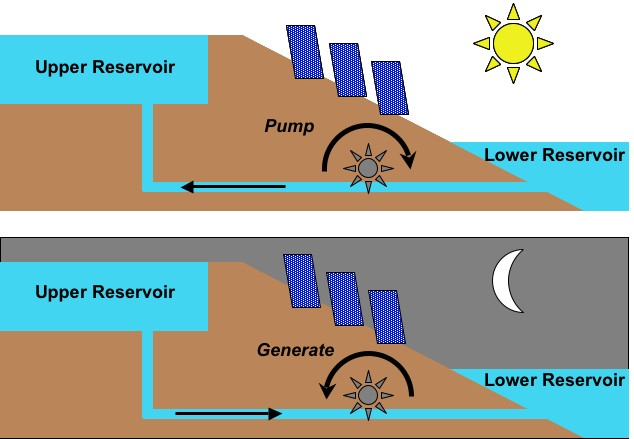
Hüdroenergia – elektrienergia tootmine langeva või voolava vee potentsiaalsest/kineetilisest energiast.
Pumbajaam
Pumbajaama idee on elektrienergia salvestamine vee gravitatsioonilisse potentsiaalsesse energiasse. Kui on elektrienergia liig, siis pumbatakse vesi kõrgele reservuaari. Elektrienergia defitsiidi puhul töötab süsteem vastupidiselt: kõrgemalt reservuaarist vesi paneb turbiini liikuma, mille tulemusena genereeritakse elektrienergiat.
Antud pildil on kujutatud päikeseenergia ning vee-energia sümbioos elektrijaam. Päeval, kui on elektrienergia ülejääk, pumbatakse vett ülesse reservuaari. Öösel kui on päikese-energia üldine defitsiit, siis seda kompenseerib vee-energia.
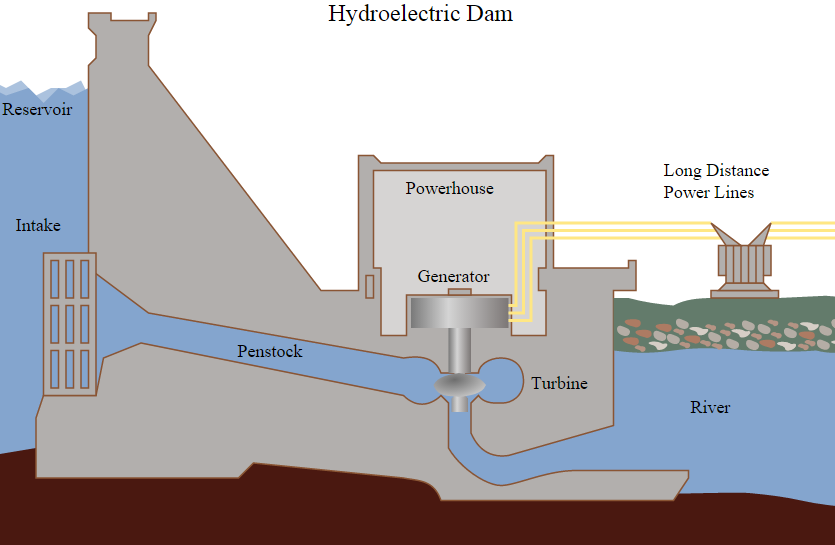
Jõevoolujaam (tammiga värk)
Idee - Ehitad tammi, mille tulemusena vee tase tõuseb enne tammi. Lastes vett läbi turbiini madalamale jõkke voolata toodetakse generaatoriga elektrienergiat.
Eelised:
Hästi väljakujunenud tehnoloogia
Suuremahuline elektritootmine madala tootmiskuluga
Jaama pikk kasutusiga
Kõrge summaarne efektiivsus <90%
Rekreatsioonipaigad ning kaladele soodne eluala
Puudused:
Sobib vaid mägisele maastikule
Pumpjaama jaoks 2 piisavalt suurt reservuaari mõistlikul kaugusel
Väga suuremahulised süsteemid, mille ehitamine aja- ja kapitalikulukas
Võib ohustada ajaloolisi maamärke
Loomuliku looduskeskkonna ulatuslik mõjutamine/hävitamine
Tamm ohtlik jalamil paiknevatele asulatele
3. Tõusu ja mõõna energia (põhimõte, süsteemi kirjeldus, eelised-puudused)
Loodete energia salvestamine - hüdroenergia liik, tõusu ja mõõna energia elektrienergiaks
3 erinevat tehnoloogiat:
Loodeturbiinid (Tidal stream generator)
Loodete tõkestamine (Tidal barrage)
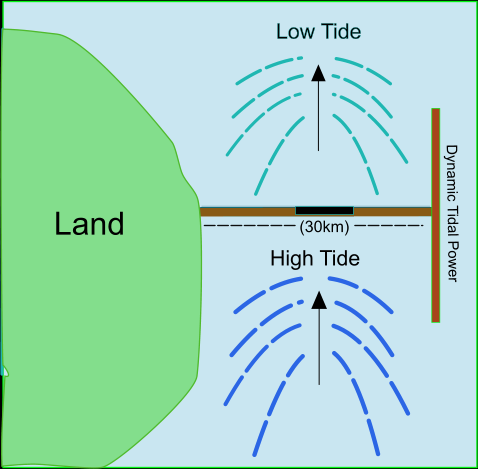
Dünaamiline loodete energia (Dynamic tidal power)
Loodeturbiinid.
Kolmest eeltoodud tüübist kõige odavamad ja loodussõbralikumad. Töötab nagu tuulegeneraator: vee liikumine paneb tiiviku liikuma.

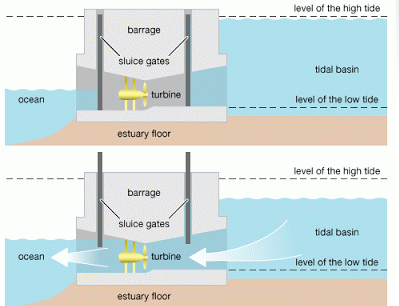
Loodete tõkestamine
Tammi-laadne ehitis - püütakse lahte või jõe-suudmes liikuvate veemasside energiat
Tõusu- ja mõõnavesi liigub läbi süsteemi lüüside
Lüüside väravaid reguleeritakse kindlatel loodete tsükli hetkedel
Elektrit toodetakse nii tõusu kui ka mõõna ajal

LiBH4 and NaBH4
Dünaamiline loodete energia
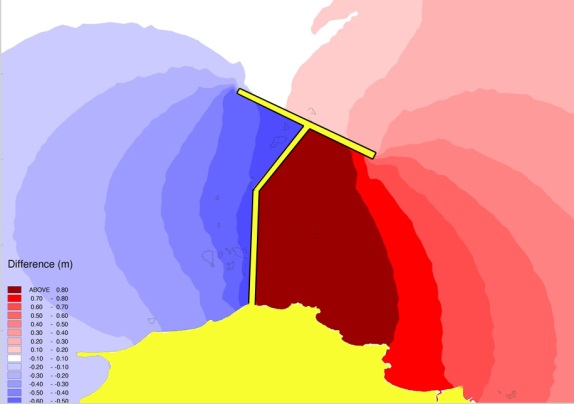
Väga lubav, aga proovimata meetod loodete energia elektrienergiaks muundamisel. Seisneb pika tammi ehitamises risti rannikualaga (vaata pilti), mis segaks vee liikumist loodete toimel. Selle tulemusena tekiks tammi eripooltel erinev veetase, millest saab turbiinide abilt toota jällegi elektrienergiat.
4. Laineenergia (põhimõte, süsteemi kirjeldus, eelised-puudused)
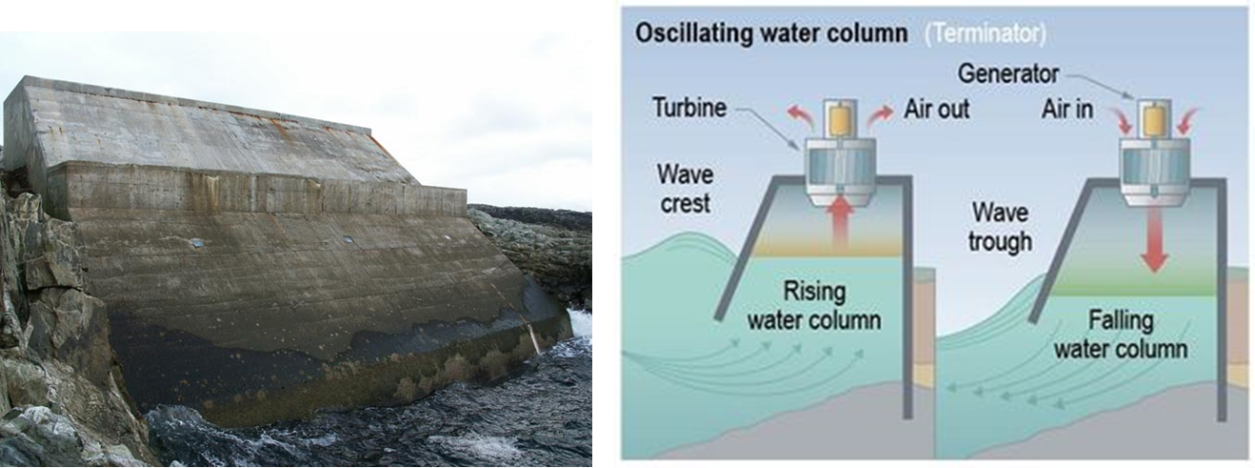
Rannajoonel asuvad süsteemid – kõikuva nivooga veesammas
„sambasse“ sissetungiv laine sunnib sambas olevat õhku ülesse poole liikuma (vaata pilti). Ülesse liikuv õhk paneb turbiini liikuma, mille tulemusena genereeritakse elektrit. Teistpidi töötab ka (laine taandumisel paneb vastupidises suunas liikuv õhk turbiini käima).
Avameresüsteem – lainelohe (Wave Dragon)
Laineenergia muundatakse potentsiaalseks energiaks ning seejärel elektrienergiaks (nagu ikka).
Laine suunatakse kaardus kaldpinda pidi veekogumis-reservuaari, kust see läbi turbiiniga toru voolab tagasi merre

Eelised:
Potentsiaalselt ulatuslikult kättesaadav taastuvenergia
Aastaringne
Keskkonnamõju minimaalne
Puudused:
Palju konkureerivaid lainegeneraatorite disaine
Rajatised peavad vastu pidama tugevatele jõududele
Muutlik väljundvõimsus mere prognoosimatu loomuse tõttu
Pole lähitulevikus majanduslikult konkurentsivõimeline
5. Suruõhk FESS (põhimõte, eelised-puudused)
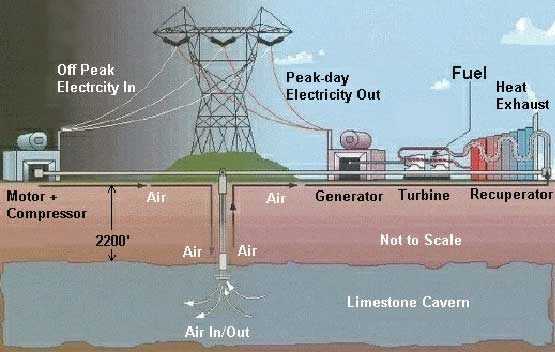
Suuresti analoogne pumbajaama põhimõttele. Üleliigse energia korral ainult ei pumbata vett kusagile kõrgele reservuaari, vaid surutakse õhk kokku ja hoiustatakse maa-aluses koopasse. Kui elektrienergiat tarvis, siis kuumutatakse õhku ning selle tulemusena gaas paisub ja hakkab läbi turbiinide liikuma.
Kasutatakse enamasti koos nö tavalise gaasiturbiiniga
Kokku surumiseks piikkoormuse välist baas-elektrienergiat
Soojendamiseks gaasiturbiini jääksoojus
Koos suruõhuga on gaasiturbiinil 3x suurem väljundvõimsus sama maagaasi koguse kohta
Eelised:
Suuremahuline energiasalvestussüsteem
Kiire koormusele reageerimine
Sobiv süsteem pidevateks ning lühiajalisteks seisakuteks/käivitamisteks
Puudused:
Tunduvalt odavam on kasutada looduslikke reservuaare –
Asukohaspetsiifiline
Summaarne efektiivsus 64-75%
6. Tuuleenergia (põhimõte, süsteemi kirjeldus, eelised-puudused)
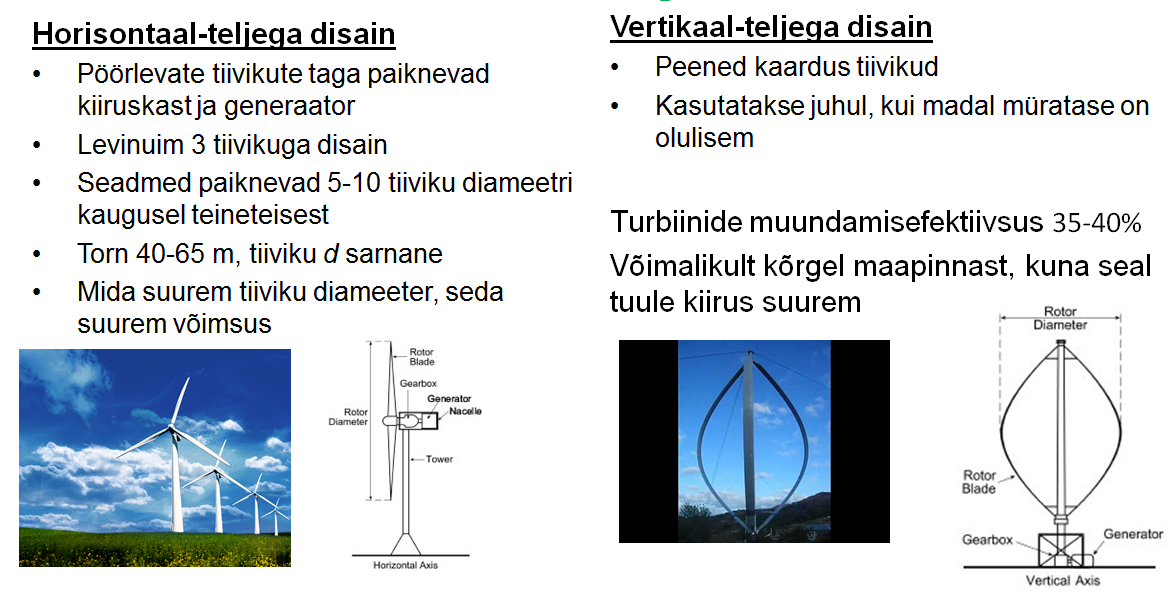
Põhimõte seisneb ikka selles, et rootor käib tuule mõjul ringi ning generaator muundab kineetilist energiat elektrienergiaks
Eelised:
Hästi väljakujunenud tehnoloogia
Väga suures mahus kättesaadav taastuvenergia liik
Elektrienergia allikas eraldatud piirkondades
Kasvuhoonegaaside jt keemiliste jäätmete vaba
Kiire ning moodul-ehitus
Madalad käitluskulud
Ohutu
Puudused:
Limiteeritud suure keskmise tuulekiirusega aladele
Kõikuva võimsusega
Tuulepargid võivad mõjutada rannikualade ökosüsteeme
Suhteliselt kallis tehnoloogia (eriti merepargid)
Samas 3-5 kuuga toob tagasi tootmiseks kulunud energiahulga
Mürasaaste, oht lindudele
Elanikkonna vastumeelsus visuaalse pildi rikkumise tõttu
7. Geotermaalenergia (põhimõte, süsteemi kirjeldus, eelised-puudused)
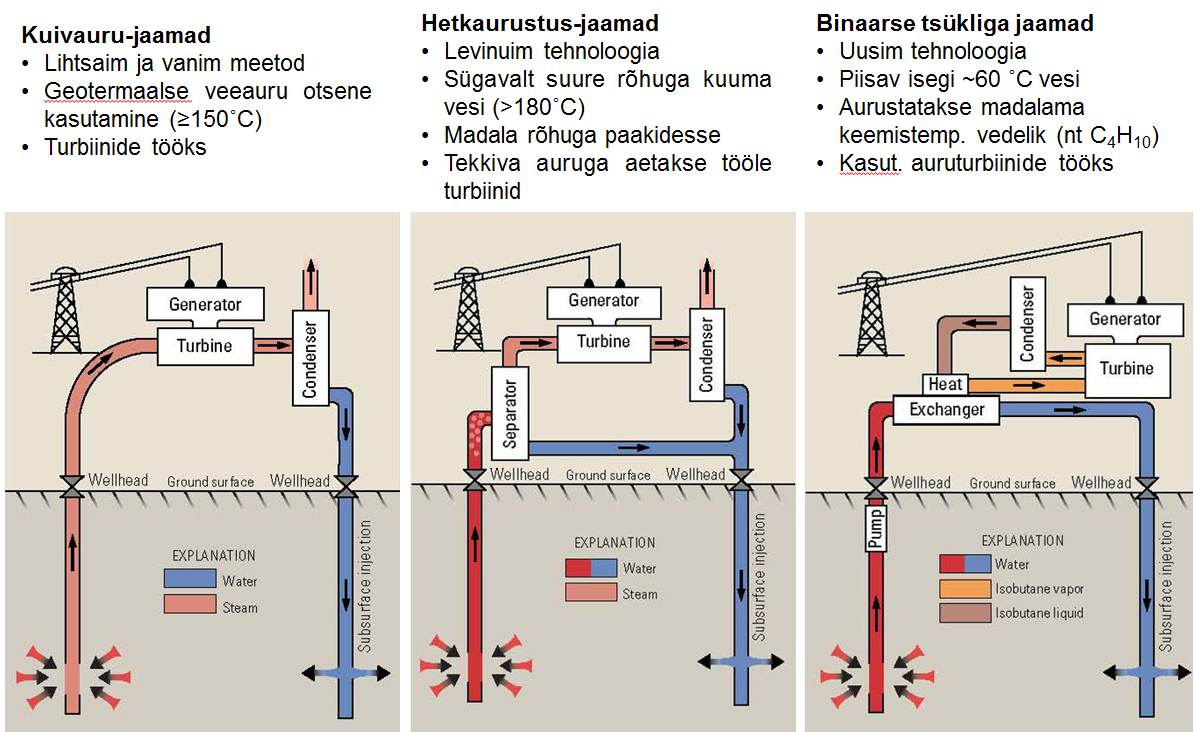
Kuivauru-jaam kasutab otse maa-seest tulevat auru turbiini ringi ajamiseks. Kui tahta vett auru asemel „väja pumbata“, siis peame kasutama ntks hetkaurustus-jaama. Hetkaurustus-jaamas tõmmatakse kuum (180 kraadi) vesi väga madala rõhuga paaki. See tekitab vee hetkelise aurustumise. See aur juhitakse jällegi turbiini, mis muundab kineetilist energiat elektriliseks. Kui tahame madalama temperatuuriga (60 + kraadi) vett kasutada, siis peab kasutama binaarse tsükliga jaama. Sellisel juhul maa-seest saadud kuum vesi aurustab paagis madalama keemistemperatuuriga vedeliku (isobutaan ntks). Isobutaani aurud liiguvad sealt edasi turbiini, kus muundatakse jällegi kineetilist energiat elektrienergiaks.
Eelised:
Tasuv energialiik
Usaldusväärne
Keskkonnasõbralik
Puudused:
Limiteeritud tektooniliste laamide äärealadele
Enamik piirkondades kasulik soojushulk liiga sügaval, et mõistliku vaeva ja kuludega selleni puurida
Loeng 14. Ülijuhtmähis-energiasalvestus. Päikeseelement ja teised päikeseenergia salvestamise viisid. Monokristallide kasvatamine
1. Ülijuhtmähis energia salvestamiseks (põhimõte, eelised-puudused)
Ülijuhtivus on füüsikaline nähtus, kus madalal temp.-l muutub aine eritakistus nulliks ja magnetväli tõrjutakse välja (Meissneri efekt). Ülijuhis säilib vool energiakadudeta.
Elektrienergia salvestatakse magnetväljas, mis on tekitatud alalisvoolu poolt ülijuhtmaterjali mähises
Mähis on krüogeenselt jahutatud materjali kriitilisest ülijuhtivustemperatuurist madalamale
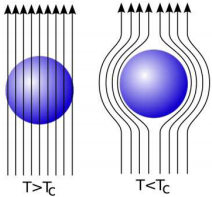
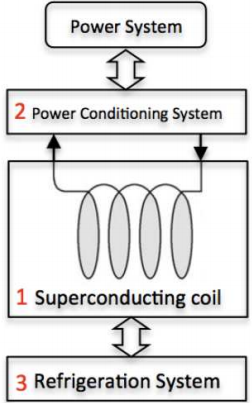 DC vool
DC vool
Süsteem koosneb 3 osast:
Mähis
Voolukontroll-süsteem
Jahutusseade
Erinevad ülijuhtmaterjalid:
Metallid ja süsinik (Pb, Hg, nanotorud, teemant)
Sulamid (peamiselt Nb-ga)
Kompleksoksiidid – keraamilised materjalid
Maksimaalne energia on määratud konkreetse ülijuht-materjali kriitilise voolutiheduse ning magnetvälja taluvusega, millest väljaspool ülijuhtivad omadused kaovad.
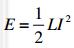
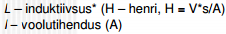
Eelised:
Efektiivsus 90-99%
Otsene elektrienergia salvestus – pole ühest energialiigist teise muundamise kadusid
Väike kadu AC/DC muundamisel
Suur võimsus ning kiire reageerimisaeg
Tühjenemise aeg <1 min, võimalik ka mõned ms-d
Pikk eluiga
Ülijuhtmaterjal ise võimaldaks pikemat eluiga, kuid külmutusning voolukontroll-süsteemid limiteerivad <100 000
Kiire lülitus laadimisest tühjenemise režiimi
Hooldusvaba
Puudused:
Energiahulk suhteliselt väike
Vajadus külmutada – energiakadu külmuti ja kompressorite tööst
Ohutus seoses:
Väga madala töötemperatuuriga
Suuremahuliste süsteemide korral ohutusprobleemid väga tugeva magnetvälja tõttu
Mähis tundlik temt muutustele
kallidmaterjalid
2. Energia päikesekiirguse koondamisest (põhimõte, eelised-puudused)
Päikesekiirguse koondamine (concentrated solar power)
Läätsede või peeglitega abil koondatakse suur hulk päikeseenergiat väiksele alale kokku
Saadava soojusenergia abil kuumutatakse vett, õli vms
Kasutatakse soojusenergiana – soe vesi
Muundatakse auru- või gaasiturbiini või sulasoolade abil elektriks, olenevalt saavutatavast temperatuurist
Koondatud päikeseenergiast saadava soojusenergia abil aetakse tööle „traditsiooniline“ elektritootmis-süsteem.
Erinevaid disaine on palju:
Paraboolsed taldrikud
„Päikesetornid“ (Solar power tower)
Paraboolsed vannid
Lineaarsed peeglid (Fresnel reflectors)



 Pildid õiges järjestuses alates paraboolsetest lineaarseteni
Pildid õiges järjestuses alates paraboolsetest lineaarseteni
Eelised:
Päikeseenergia on maailma suurim taastuva energia allikas
Elektrit saab toota mil iganes päike paistab
Töötamisel puudub saaste tahkete või vedelate jäätmete, nanoosakeste, mürgiste või kasvuhoonegaaside kujul
Puudused:
Päevane ja aastaajaline kättesaadavuse kõikumine
Maksimaalne kiiritus piiratud troopilistesse aladesse
Võrguühenduseta paneelidel vajalik salvestus
Tootmise keskkonnariskid (suures mahus tekkiva emissiooni ja jäätmete kontrolli probleemid)
3. Päikeseelemendid (põhimõte, rakendatavad materjalid, eelised-puudused)
Fotogalvaanilise elemendid (photovoltaics) – Otsene päikesekiirguse muundamine elektrivooluks.
Päikese-element muundab valgusfootonite energia (toimub elektronide tekitamine) fotogalvaanilise (photo voltaic – PV) efekti abil elektrienergiaks
Toodab vastavalt päikese kiirguse intensiivsusele muutuva voolu-tihedusega alalisvoolu
Inverteriga muundatakse saadav alalisvool vahelduvvooluks
Valgusfootonid on võimelised tekitama pooljuht-materjalides laengute lokaliseerumise ning selle mõjul pinge püstitumise – võimalik välise koormuse ühendamisel tekitada elektrivool.
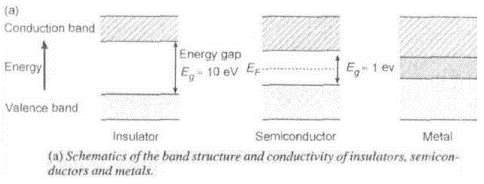
Materjalid:
Levinuim monokristalne, polükristalne ning amorfne Si
GaAs, CdTe, CuInSe2 ning mõned orgaanilised ühendid
Nt 2 pooljuhi tüüpi:
Si dopeerimisel 3-valentse lisandiga (B, Al) -> p-tüüpi auk-juhtivusega pooljuht
5-valentse lisandiga (P, As) dopeerides e– laengukandjatega n-tüüpi pooljuht
Nende pooljuhtide piirpinnal tekib laengukandjate vaene ala ning selle mõjul elektriväli.
Footonienergia abil tekitatakse laengute vaeses piirkonnas (depletion zone) uuesti elektronid ja vakantsid, mis tekkinud elektrivälja mõjul liiguvad.
Eelised:
Päikeseenergia on maailma suurim taastuva energia allikas
Elektrit saab toota mil iganes päike paistab
Töötamisel puudub saaste tahkete või vedelate jäätmete, nanoosakeste, mürgiste või kasvuhoonegaaside kujul
Päikeseelemendid:
Puuduvad liikuvad osad – vaikne töötamine
Usaldusväärsed ja hooldusvabad
Pikk eluiga (25+ aastat)
Modulaarsed
Laialdaselt leiduv ja odav peamine koostismaterjal (Si)
Puudused:
Päevane ja aastaajaline kättesaadavuse kõikumine
Maksimaalne kiiritus piiratud troopilistesse aladesse
Võrguühenduseta paneelidel vajalik salvestus
Si-elemente suhteliselt kallis toota
Automaatselt juhitavaid paneele kallis valmistada
Tootmise keskkonnariskid (suures mahus tekkiva emissiooni ja jäätmete kontrolli probleemid)
4. Monokristallide kasvatamisest üldiselt
Monokristalses tahkises on kogu faasi ulatuses kristallvõre katkematu – puuduvad polükristalsele materjalile omased terade piirpinnad (grain boundary),
„Struktuuri defektide“ puudumine
Monokristallidel on erakordne elektron-/ioonjuhtivus, mehaanilised ja optilised omadused
Võimalik päikesepaneelide, kütuseelementide, elektroonikaseadmete, gaasisensorite, jne. omadusi täiustada
Kallim vs. sama koostisega polükristalse materjali valmistamine
Struktuur kergesti rikutav lisandite ning sünteesitingimuste väikese varieeruvuse mõju
Kasvatamine toimub enamasti läbi faasi muutuse:
Vedel -> tahke
Gaasiline -> tahke
Sulafaas -> lahus -> tahke
Monokristalli süntees on aeglane pikaajaline kontrollitud tingimustel protsess (temperatuur, rõhk, vibratsioon, jne)
Liiga kiire protsessi korral:
Kristalli sees lõksus korrapäratud alad
Esineb kristallisatsioon monokristalli pinnalt erinevates suundades
Eri tüüpi kristallisatsioon:
Heterogeenne kristallisatsioon – vedelfaasi tahkumine toimub eksisteerivate tahkete osakeste pinnalt
Polükristalne struktuur
Näiteks tolmuosakestelt vees 0 ˚C
Ülijahutatud vedeliku kristallisatsioon – tahkete osakeste vaba vedelikku saab jahutada sulasmistemperatuurist madalamale
Spontaanne väikeste alade korrapärastumine
Järgneb kiire paljude suvaliselt orienteeritud kristallide teke
Idukristallist kasvatamine – monokristall kasvatatakse lisatud idukristalli pinnalt
Tingimusi kontrollitakse piiramaks kristallisatsiooni „idu“ lähedusse
Idukristalli puudumisel rakendatakse kristallide omadust kasvada kiiremini ühes kristallograafilises suunas
Bridgman-Stockbarger ja Czochralski meetodid
Levinumad meetodid:
Lahuse jahutamine ja väljasadestamine idukristallile
Sulafaasist jahutamine
Sulafaasist (T = const), sukeldades idukristall pinnale ja tõmmates eemale jahedamasse tsooni
Vedelfaasist erineva koostisega substraadil sadestades
Keemilisel reaktsioonil lahusest
Keemilisel reaktsioonil aurufaasist idukristalli pinna läheduses
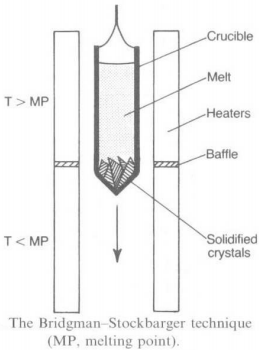 5. Bridgman-Stockbarger ning tsoonsulatus meetodid monokristallide kasvatamiseks
5. Bridgman-Stockbarger ning tsoonsulatus meetodid monokristallide kasvatamiseks
Bridgman-Stockbarger meetod (paremal olev joonis)
Oksiidide segu sulatatakse tiiglis (Pt-Rh)
Hoitakse >Tsul
Tiiglist madalamal järsk T langus
Tiigli alumine osa liigutatakse otsapidi külma alasse – algab kristalliseerumine
Ühes kindlas kristallograafilises suunas kasv kiirem
Ainult tiigli telje suunas kiiremini kasvavad kristallid kasvavad edasi tiigli liikumisel külma tsooni
Ülemises osas lõpuks kas üks või paar suurt monokristalli
Tsoonsulatus-meetod
Sulatatakse lokaalselt määratud stöhhiomeetrilise koostisega polükristalse materjali peenikest pulka
Sulatatakse väike ala korraga
Pulga otsa asetatakse idukristall
Sula tsooniga liigutakse ühest otsast teise
Monokristall kasvab piki toru telge (kõrge T-ga alas toimub reorganisatsioon
lisandid liiguvad koos sulatsooniga edasi, st võimalik puhastada lisanditest (võimalus tõsta monokristalli kvaliteeti))
Mitmekordne protsess
Röntgenanalüüsil on eristatavad suured monokristalsed alad
Toimub lisandite kandumine koos sulatsooniga pulga otsa
Segregeerumise koefitsient (lisand tahkes faasis/vedelas faasis) tavaliselt <1
Sulatatakse kas kuumutamisel või nt laserkiirega. Ülipuhta faasi jaoks lõigatakse vahepeal lisanditega küllastunud ots ära.
Horisontaalne tsoonsulatus
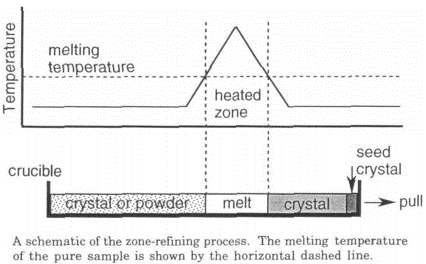
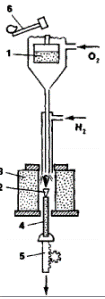 6. Verneuil leeksulatus ning Czochralski kristallitõmbamise meetodid monokristallide kasvatamiseks
6. Verneuil leeksulatus ning Czochralski kristallitõmbamise meetodid monokristallide kasvatamiseks
Verneuil leeksulatus meetod (joonis paremal)
Levinud meetod, kuid saadavate monokristallide kvaliteet pole parim
Oksiidide pulbrit suunatakse kontrollitud kiirusega mööda toru
Toru otsas sulatatakse pulber paukgaasi leegis
 Sulaoksiid tilgub idukristalliga alusele
Sulaoksiid tilgub idukristalliga alusele
Alust liigutatakse jahedamasse tsooni
Raske kontrollida kristalli kasvatamise keskkonda
Kristalli tõmbamine (Czochralski meetod)
Laialdaselt kasutatud Si, kompleksoksiidide ja paljude kongruentselt sulavate materjalide korral
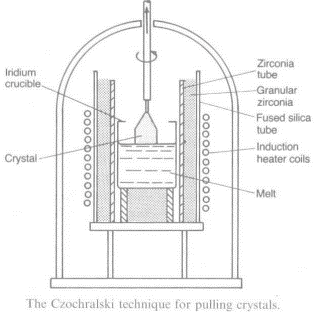 Segu hoitakse >Tsul
Segu hoitakse >Tsul
Pöörleva toru külge fikseeritud idukristall sukeldatakse vedela faasi pinnale
Idukristalli tõmmatakse aeglaselt eemale, kristall kasvab
Kristallihoidja toru sees vesijahutus
Monokristalli diameeter määratud eemaldumise kiirusega
„Vales suunas“ kasvava kristalli elimineerimine – suurendada ja uuesti vähendada kristalli diameetrit
~90% sulafaasist võimalik saada monokristallina
7. Vedelfaasi epitaksiline meetod õhukeste monokristalli kilede valmistamiseks
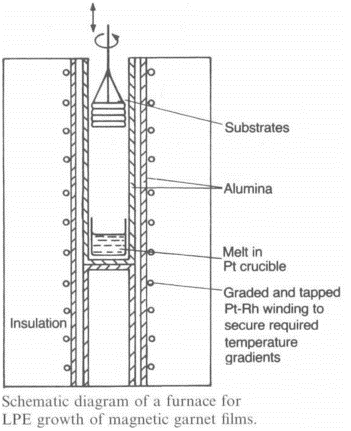 Vedelfaasi epitaksiline sadestamine (Liquid Phase Epitaxial Deposition)
Vedelfaasi epitaksiline sadestamine (Liquid Phase Epitaxial Deposition)
Õhukeste monokristalli kihtide sadestamise meetod (~10 µm)
Pöörleva pulga küljes ümarad substraadi plaadid
Sulafaasi jahutatakse paar kraadi üleküllastumise tekkimiseni
Pöörlevaid substraate hoitakse mõni s/min sulas faasis
Sulafaasist väljudes eemaldatakse liigne vedel faas kiirel keerlemisel
Laialdaselt kasutatud pooljuht ning elektro-optiliste seadmete detailide valmistamisel
Veel sarnaseid dokumente
Valitud peatükke elektrokeemiast (sarnasus: 28)Eksamiküsimused Aine “Vedelikkromatograafia ja massispektromeetria” jaoks (sarnasus: 25)
