Anorgaaniline keemia I vastused
Lisamise aeg:
2015-08-14 11:41:28Vaatamiste arv:
16355Tagasiside:
0 0Anorgaaniline keemia I
Õppeaasta 2011/2012 kevadsemester
KÜSIMUSED (II osa)
KOMPLEKSÜHENDID
Mille poolest erinevad kompleksühendid nn. lihtsatest ühenditest?
Nendes on osa sidemeid tekkinud doon-akts.meh. ja keskne element on moodustanud rohkem sidemeid kui on tema tavapärane oks.ast.
Millised osakesed saavad käituda kompleksimoodustajana, millised ligandidena?
Kompleksmoodustajana saab osaleda see millel on vabad elektronorbitaalid, ligandidena need millel on elektronpaar.
Kirjutage ühe komplekskatiooni, ühe kompleksaniooni ja ühe neutraalse kompleksi valem ning nimetus, määrake nendes kompleksimoodustaja koordinatsiooniarv ja sisesfääri laeng.
[Cu(NH3)4]SO4 tetraammiinvask(II)sulfaat koord.arv 4 sisesfääri laeng +2
Na3[Al(OH)6] naatrium heksahüdroksoaluminaat koordarv 6 sisesääri laeng -3
Fe(CO)5 pentakarbonüülraud koord.arv 5 sisesfääri laeng 0
Selgitage keemilise sideme iseloomu: a) kompleksimoodustaja ning ligandide vahel; b) kompleksi sise- ning välissfääri vahel.
Kompleksmoodustaja ja ligandide vahel on kovalentne. Sise-välis iooniline.
Kuidas liigitatakse kompleksühendeid sisesfääri laengu, ligandide tüübi ja kompleksühendi happe-aluse iseloomu järgi (näited)?
Ligandide iseloomu järgi: akvakompleksid ([Cr(H2O)6]3+), klorokompleksid (H2[CuCl2]), ammiinkompleksid ([Co(NH3)6]Cl3), hüdroksokompleksid Na3[Al(OH)6]
sisesfääri laengu järgi: kompleks katioonid ([Cu(NH3)4]2+), kompleks anioonid [Co(NO2)4(NH3)2]-, neutraalsed kompleksid [Fe(CO)5]. Happeline ja aluseline – välissfääris H või OH
Miks on komplekskatiooniga alused ja kompleksaniooniga happed tugevamad kui vastavate lihtioonidega happed ja alused (näited, põhjendused)?
Tava alustes ja hapetes on rohkem kovalentset sidet. Kompleksides on rohkem ioonilist.
Sisesfääris on ligandidega sidemed väga tugevad, seetõttu välisfääriga nõrk ning kerge loovutada ioone. H2[SiF6], [Cu(NH3)3]OH2
Millistele tuntumatele kompleksimoodustajatele on iseloomulikud hüdroksokompleksid, millistele ammiinkompleksid? Tooge näide ühe hüdroksokompleksi ja ühe ammiinkompleksi saamisvõimaluse kohta.
Hüdroksokompleksid tekivad amfoteersete metallidega: Zn, Al. Saamine metallisoolale leelise lisamisel. Ammiinkompleksid tekivad siirdemetallide Co, Ni, Cu. Alusele lisada NH3*H2O liias.
Tooge näiteid ühehambalistest (monodentaatsetest) ja mitmehambalistest (polüdentaatsetest) ligandidest ning kelaatidest.
Kui üks ligand saab anda mitme elektropaariga sidemeid. Nt: EDTA, en (etüleendiamiin). Kelaat on tsükliline kompleksühend. [Fe((COO)2)3] - trioksalato
Mis on kelaat-efekt? Põhjendage kelaatide ja nendega lähedase koostisega tavaliste komplekside püsivuse erinevust. Kelaadid on olulisemalt püsivamad entroopiaefekti tõttu. Näiteks tekib kelaat-efekt Cu(OH)2 + NH2CH2COOH abil, kus eraldub vesi ja tekib hapnikusild.
Tooge näiteid mitmetuumalistest kompleksidest. Millised ligandid saavad käituda sild-ligandidena mitmetuumalistes kompleksides? K2Cr2O7. Tuumasid seob sildligand, millel peab olema vähemalt 2 vaba elektronpaari. (nt näites O) Tüüpilised sildligandid veel OH, Cl
Mis on klastrid? Mille poolest nad erinevad teistest mitmetuumalistest kompleksidest? Tooge näiteid klasterühenditest. Klastrid on mitmetuumaline kompleks kus tuumade vahel on vahetu omavaheline side. [W2Cl9]3-
Millised tegurid mõjutavad kompleksimoodustaja koordinatsiooniarvu kompleksühendis (näited, põhjendused)? Kui palju on vabasid orbitaale, aatomi suurusest, laengust (mida suurem, seda kõrgem kordarv). Suurem laeng tõmbab elektrone paremini ligi. Kui ligandid neutraalsed siis koordinatsiooniarv suurem.
Millised on iseloomulikud koordinatsiooniarvud kompleksühendites? Millise kujuga kompleksid neile vastavad ja milline hübridisatsioon nendes esineb? 6 – oktaeeder (sp3d2), 4 – tetraeeder(sp3) , 5 – trigonaalne bipüramiid,
13. Millised on kompleksühendite isomeeria põhiliigid (selgitused, näited)? geomeetriline ehk cis-trans isomeeria – eri tüüpi ligandide erinev paigutus isomeerides
cis – sama tüüpi ligandid on lähestikku (samal pool tsentraalaatomit);
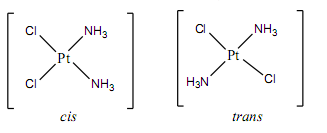 trans – sama tüüpi ligandid on vastasasendis (tsentraalaatomi vastasküljel).
trans – sama tüüpi ligandid on vastasasendis (tsentraalaatomi vastasküljel).
optiline ehk peegelisomeeria (kiraalsus) esineb keerulisemate komplekside (nt. kelaatide) korral
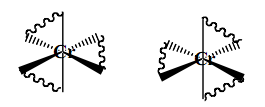 Ligandide vahekaugused on võrdsed, kuid isomeerid on teineteise peegelpildid. [Cr((NH2CH2)2)3]
Ligandide vahekaugused on võrdsed, kuid isomeerid on teineteise peegelpildid. [Cr((NH2CH2)2)3]
ionisatsiooni-isomeeria – eri tüüpi anioonsete ligandide erinev jaotus sise- ja välissfääri vahel: [Co(NH3)4Cl2]Br vs [Co(NH3)4ClBr]Cl
hüdraatne (solvaatne) isomeeria – eelmise erijuht, vee (lahusti) molekulide erinev jaotumine sise- ja välissfääri vahel. Hüdraatne isomeeria avaldub kristallveega komplekside korral (tahkes olekus). See, milline kompleks tekib, sõltub sünteesi tingimustest (ligandide ja vee kontsentratsioonide suhtest).
[Cr(H2O)6]Cl3 (violetne)
[Cr(H2O)5Cl]Cl2⋅H2O (heleroheline)
[Cr(H2O)4Cl2]Cl⋅2H2O (tumeroheline)
Millised on kompleksi MA2B2C2 võimalikud geomeetrilised ja optilised (peegel-) isomeerid (struktuurivalemid)?
Kuju |
A asend |
B asend |
C asend |
Cis |
cis |
trans |
|
Trans |
Trans |
trans |
|
Trans |
Cis |
cis |
|
Cis |
Trans |
cis |
|
Cis |
Cis |
cis |
Millised on komplekside [MCl(NH3)3en)Br ja [M(NO2)2en2)Cl võimalikud isomeerid (en – etüleendiamiin, kahehambaline ligand)?
Mis on lõhestumisparameeter? Millised tegurid ja kuidas mõjutavad lõhestumisparameetri suurust kompleksühendites (põhjendage)? Näitab kui suur on energeetiline lõhe soodsate ja mittesoodsate d-orbitaalide vahel. Oksüdatsiooniaste – ligandidega sideme tugevus kasvab, seega lõhestumisparameeter suureneb. mida parem elektronpaardoonor on ligand, seda suurem on lõhestumisparameeter. *Kui palju kulub energiat, et ergastada elektronid soodsamatelt ebasoodsamatele d-orbitaalidele. Kui lõhestumisparameeter on suur, siis ei kehti Hundi reegel.
Mis on kõrge- ja madalaspinnilised kompleksid, millistel tingimustel need tekivad (näited, selgitused)? Põhjendage nende püsivuse erinevust?
Kõrgespinnilised need mis on moodustunud sp3d2 orbitaalide, madalad need mis on moodustnud d2sp3. Esimene on moodustunud 4d orbitaalidega ja teine 3d orbitaalidega.
Kui lõhestumisparameeter on suurem kui elektroni paardumisenergia siis on madalaspinniline kompleks , see on energeetiliselt püsivam ja vastupidi.
Mis on ligandide spektrokeemiline rida? Millise omaduse järgi on ligandid selles reastatud? Lõhestumisparameetri suurenemise järjekorra. I- kõige vähem suurendab lõhestumisparameetrit ja CO kõige rohkem. CO kuni H20 on madalaspinniline.
Miks oksüdeeruvad koobalt(II) madalaspinnilised kompleksid kergesti vastavateks koobalt(III)-kompleksideks?
Kuna madalaspinnilised kompleksid on väga tugevad redutseerijad. Kuna 3d orbitaalil üksik elektron, mida soodsam ära anda.
Millise kujuga on kompleksid [Ni(CN)4]2− ja [Ni(Cl)4]2−, kui esimesel on ? > Ep, teisel ? < Ep (? – lõhestumisparameeter , Ep – elektronide paardumise energia)?
.
[Ni(CN)4]2− tasapinnaline ruut
[Ni(Cl)4]2−, tetraeeder
dε(t2g) telgede vahel, dγ(eg) telgedel, oktaeedrilisel ligandid telgedel, järelikult lõhestumine nii, et dγ täitub hiljem kui dε tetraeedrilise puhul vastupidi.
Tsüano on spektrokeemiliselt tugev ligand =>suur lõhestumisparameeter Cl- on spektrokeemiliselt nõrk ligand => lõhestumisparameeter väike
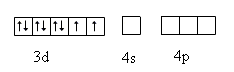 Seega tavaline Ni2+
Seega tavaline Ni2+
Nii tekkib sp3 hübridisatsioon ja kuju tetraeedriline
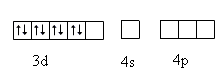 Tugeva ligandiväljaga Ni2+
Tugeva ligandiväljaga Ni2+
Hundi reegel ei kehti enam kui lõhestumisparameeter suur, seega kasutab ta dsp2 hübridisatsiooni ja sellele vastab planaarne ruut.
Miks on d-elementide kompleksid enamasti värvilised?
D-elementide delta (lõhestumisparameeter) energiakvant kuulub nähtava valguse alasse.
Mille järgi jaotatakse komplekse püsivateks ja ebapüsivateks, labiilseteks ja inertseteks (selgitused, näited)?
Inertsed on termodünaamiliselt ebastabiilselt kuid kineetiliselt püsivad. Labiilsed nii TD kui kineetiliselt ebastabiilselt. EBAPÜSIVUSKONSTANT. Ebapüsivus selle järgi kui püsiv on sisesfäär. Nt [Cu(NH3)4] + H2O = [Cu(NH3)3H2O] + NH3
Miks aktiivsete metallide (leelis- ja leelismuldmetallide) katioonid on väga nõrgad kompleksimoodustajad?
Kuna neil pole vabu d-orbitaale.
Mis on kaksiksoolad (selgitus, näited)?
Kompleksid milles anioonid on samad, aga katioonid on erinevad: 2KCl?CuCl2 →K2[CuCl4]
Spetsiifilised kaksiksoolad: Maarjad. Kaks katiooni erinevate laengutega(I ja III), sulfaadid ja 12 vett.
Kirjutage kompleksi [Zn(NH3)4]Cl2 püsivuskonstandi avaldised astmete kaupa ja summaarse ebapüsivuskonstandi avaldis. Milline on seos kompleksi püsivus- ja ebapüsivuskonstandi vahel?
Kuidas ja miks muutuvad (reeglina) kompleksi järjestikuste (astmete kaupa) püsivuskonstantide väärtused?
Püsivuskonstant muutub järjest suuremaks, kuna iga järgmist ligandi on raskem eemaldada.
Mis on trans-mõju seadus? Selgitage ligandide trans-mõju põhimõtet.
Mis on ligandide trans-mõju rida? Millise omaduse järgi on ligandid selles reastatud?
Transasendisse minemise järjekorras. Alguses tugevam transs-mõju.
Kuidas (milliseid lähteaineid kasutades) on võimalik sünteesida kompleksi [PtCl2(NH3)2] cis- ja trans-isomeere (põhjendused)? Pt(Cl4)-le NH3 lisades, saab cis-isomeeri.
REDOKSPROTSESSID
Mida iseloomustab elektroodipotentsiaali väärtus? Mis on standardpotentsiaal?
Mida positiivsem on standardpotentsiaal , seda tugevam on vastavas poolreaktsioonis elektroni liitmise tendents – tegemist on tugeva oksüdeerijaga.
Elektroodipotentsiaal (tähis sageli E ) on potentsiaal, mille omandab metallelektrood (või vesinikelektrood) vastava metalli katioone (või vesinikioone) sisaldava lahuse suhtes.
Redokspotentsiaali väärtus väljendab tööd või energiat mis vabaneb 1 elektroni üleviimisel vastavas protsessis.
Millised on seosed: a) redokspotentsiaali E ja reaktsiooni vabaenergia muutuse ΔG vahel: võrdeline seos;
b) reaktsiooni vabaenergia muutuse ΔGo ja tasakaalukonstandi vahel: logaritmiline seos.
c) reaktsiooni tasakaalukonstandi K ja standardredokspotentsiaali Eo vahel: ?
a)võrdeline seos(E~ -ΔG)
b)logaritmilne seos( nFE=RTlnK)
c)logaritmiline ja miinuseline ΔG=- RTlnK
Kuidas on redokspotentsiaalide põhjal võimalik otsustada, et: a) aine on tugev oksüdeerija või redutseerija,
b) aine on redoksreaktsioonide suhtes üsna püsiv,
c) ainele on iseloomulik autoredoksreaktsioon (disproportsioneerumisreaktsioon)?
a) Mida suurem positiivne E, seda tugevam oksüdeerija on oksüdeeritud vorm. Mida negatiivsem E seda tugevam redutseerija on redutseeritud vorm
b) kui latimeri diagrammil kui oksüdeerivat omadust näitav potentsiaal on madal ja redutseerivat omadust näitav potentsiaal on kõrge, siis on tegu püsiva ainega.
c) Kui ainele on iseloomulikud nii oksüdeerivad kui redutseerivad omadused. Latimeri diagrammil paremale jääv suurus on suur (hea oksüdeerija) ja kui vasakule jääv suurus on väike (hea redutseerija).
Mida väljendavad järgmised diagrammid: a) Latimeri diagramm, b) Frosti diagramm, c) Pourbaix’ diagramm, d) Ellinghami diagramm? Milliseid järeldusi on võimalik ainete redoksomaduste kohta teha nende diagrammide alusel?
Latimeri diagramm näitab ühest oa.’st teise oa’sse ülemineku redokspotentsiaali väärtusi.
Frosti diagramm iseloomustab kindla elemendi vabaenergia sõltuvust oksüdatsiooni astmest.
Pourbaix’ diagrammil on näidatud potentsiaali sõltuvus pHst.
Ellinghami diagramm näitab lihtainete osüdeerimise vabaenergia sõltuvust temperatuurist.
Miks on kaltsium metallide pingereas naatriumist vasakul (kuigi naatrium on keemiliselt aktiivsem metall ja tema ionisatsioonienergia on madalam) ja kõige vasakpoolsem metall on liitium (kuigi liitium on leelismetallidest kõige kõrgema ionisatsioonienergiaga)?
Kaltsiumi hüdraatumisenergia ületab naatriumi hüdraatumisenergia, kuna ta on suurema laenguga ja väiksem. Metallide pingerida on tehtud standardpotentsiaali põhjal. Standardpotentsiaalis on arvesse võetud ioonisatsiooni ning hüdraatumisenergiat.
Kuidas muutub p-metallide ja kuidas d-metallide oksüdatsiooniastmete püsivus rühmas ülevalt alla? Miks?
p-metallidel max o-a on võrdne rühma nr’ga. Rühmas ülevalt alla muutub püsivamaks rühma nr-2 – väliskihi s-elektronid on tugevamalt tuumaga seotud, läbitungimisefekt tugevneb.
d-metallidel ülevalt alla muutub stabiilseks kõrgem o-a. Tugevneb kov. sideme osatähtsus, tuleb lõhkuda nii metalliline kui ka kov. side, energia kompenseerimiseks on vaja saada võimalikult palju elektrone.
Miks 4. perioodi d-elementide 1. alaperes (Sc → Mn) elementide maksimaalne oksüdatsiooniaste küll piki rida järjest kasvab, kuid muutub järjest ebapüsivamaks ja miks 2. alaperes (Fe → Zn) maksimaalne oksüdatsiooniaste piki rida juba märgatavalt langeb (kuni oksüdatsiooniastmeni II)?
I alaperes o-a kasvab, sest elektrone tuleb juurde, mille äraandmine on energeetiliselt kasulik. Ebastabiilne on sellepärast, sest vahepeal on stabiilsed vaheolekud d5.
II alaperes langeb, sest d-orbitaalid on juba rohkemate elektronidega täidetud ning nende äraandmine ei ole enam energeetiliselt mõttekas.
Milline on järgmiste elementide maksimaalne ja milline on püsivaim oksüdatsiooniaste ühendites (põhjendage): Tl, Sn, Pb, Bi, Ti, V, Cr, W, Mn, Fe, Os, Co, Ni, Cu, Ag, Au?
Tl – 1,3 kuna s elektrone hoitakse paremini kinni, Sn max on 4, püsivam 2. Pb püsivam 2, max on 4. Bi max on 5, püsivam 3. Ti max on 4 ja püsivam samuti. V max 5, püsiv 5. Cr max on 6, püsiv 3. W max 6 , püsiv 6. Mn max 7, püsiv4. Fe max 8, püsivam 3. Os max 8, püsiv 8. Co püsiv 2,3 max 4. Ni max 4, püsivam 2. Cu max 4, püsiv 2. Ag max 3, püsivaim 1. Au max 5, püsiv 3.
Miks kroom praktiliselt ei moodusta ühendeid oksüdatsiooniastmes I ja ka vasel on püsivam oksüdatsiooniaste II, mitte I, kuigi nende aatomitel on eelviimase kihi d-alakiht saavutanud püsiva oleku ja väliskihis on vaid 1 elektron?
Energeetiliselt pole mõtet lõhkuda metallilist sidet et luua vaid üks side.
Millistele alltoodud ainetest on iseloomulik käituda: a) oksüdeerijana, b) redutseerijana, c) nii oksüdeerijana kui ka redutseerijana (olenevalt reaktsioonipartnerist)? Milline saadus seejuures tekib (enamasti)? Millistel juhtudel on reaktsiooni toimumiseks kindlasti vajalik kuumutamine (s.t vastav aine muutub aktiivseks oksüdeerijaks või redutseerijaks vaid kõrgel temperatuuril)?
a) H2, NaH, O2 redutseerijana OF6., H2O2, Cl2, HCl, KClO, I2 KIO3 , HI,
b) S, H2S, H2SO3, konts. H2SO4, Na2S2O8,
c) NH3, KNO2, KNO3, P4, PH3, KPO2H2, P4O10,
d) SnCl2, SnCl4, PbSO4, PbO2, KBiO3,
e) MnCl2, Mn(OH)2, MnO2, Cr(OH)2, CrCl3, K3[Cr(OH)6], K2Cr2O7, CrO3,
f) Fe, FeCl2, FeCl3, Ni(OH)2, NiOOH, CuCl, CuCl2, Ag, AgNO3 jne.
Hapnik on elektronegatiivsuselt teine element fluori järel? Millega seletada, et hapnik (lihtainena) on tavatingimustes suhteliselt nõrk oksüdeerija (näiteks kloor on oluliselt tugevam)? Hapniku aatomite vahel on tugev kaksikside
Gaasilise HCl saamiseks kasutatakse tahke NaCl ja konts. H2SO4 vahelist reaktsiooni (kuumutamisel). Miks pole HBr ja HI võimalik saada analoogilisel viisil (vastavalt NaBr ja NaI reageerimisel konts. H2SO4-ga)?
HBr ja HI reageerivad edasi k. väävelhappega ning tekivad vastavalt broom ja jood.
Tahke KMnO4 ja konts. HCl vahelist reaktsiooni kasutatakse laboris Cl2 saamiseks. Samas kasutatakse ka vastupidist võimalust – KMnO4 saaml kasutatakse lähteainena Cl2 (K2MnO4 oksüdeerimisel Cl2-ga). Kuidas seda näilist vastuolu selgitada (kummas suunas ja miks on kummalgi juhul nihutatud reaktsiooni tasakaal)?
Kuidas ja miks sõltub KClO3 tugevus oksüdeerijana lahuse pH väärtusest?
Kui pH happelisem siis vesinikioonid seovad paremini hapnikuaatomeid ,seega ühend parem oksüdeerija.
Millises keskkonnas (happelises, neutraalses või aluselises) on kergem Cr(III) ühendeid oksüdeerida Cr(VI) ühenditeks? Miks?
Happelises kuna, siis on redokspotentsiaal negatiivsem ja mida negatiivsem seda parem redutseerija on redutseeritud vorm ja seda paremini oksüdeerub oksüdeeritud vormiks.
Vesinikperoksiid H2O2 on tugevam oksüdeerija kui KMnO4. Millega seletada, et H2O2 käitub samas KMnO4 suhtes redutseerijana?
KMnO4 ei saa olla redutseerija aga H2O2 saab.
Kumb oksüdeerub kergemini, kas Fe(OH)2 või FeSO4? Miks?
Fe(OH)2 kuna molekuli standardpotentsiaal on suurem kui Fe2+
Kirjutage järgmiste redokspaaride osavõrrandid (poolreaktsioonide võrrandid) ja redokspotentsiaali E avaldised:
a) happelises keskkonnas: NO3 −/HNO2, ClO3 −/Cl−, Cr2O7 2−/2Cr3+;
b) neutraalses või aluselises keskkonnas: NO3 −/NO2 −, ClO3 −/Cl−; CrO4 2−/Cr(OH)6 3−.
Kirjutage reaktsioonide võrrandid, milles:
H2 käitub oksüdeerijana,
H2 käitub redutseerijana,
H2O käitub oksüdeerijana,
H2O käitub redutseerijana,
H2O2 käitub oksüdeerijana (vesilahuses),
H2O2 käitub redutseerijana (vesilahuses),
Cl2 käitub oksüdeerijana (vesilahuses),
Cl−-ioonid käituvad redutseerijana (vesilahuses),
I−-ioonid käituvad redutseerijana (vesilahuses),
KClO3 käitub oksüdeerijana (happelises keskkonnas),
S2−-ioonid käituvad redutseerijana (vesilahuses),
SO2 käitub redutseerijana (vesilahuses),
SO2 käitub oksüdeerijana (vesilahuses),
konts. H2SO4 käitub oksüdeerijana,
HNO3 käitub oksüdeerijana,
KNO2 käitub redutseerijana (vesilahuses),
KNO2 käitub oksüdeerijana (vesilahuses),
KMnO4 käitub oksüdeerijana (happelises lahuses),
KMnO4 käitub oksüdeerijana (neutraalses lahuses),
K2Cr2O7 käitub oksüdeerijana (happelises lahuses),
K2Cr2O7 käitub oksüdeerijana (neutraalses lahuses),
K2CrO4 käitub oksüdeerijana (aluselises lahuses),
Fe3+-katioonid (lahuses) käituvad oksüdeerijana (happelises keskkonnas),
Fe2+-katioonid (lahuses) käituvad redutseerijana (happelises keskkonnas),
Cu2+-katioonid (lahuses) käituvad oksüdeerijana.
Kumb metall korrodeerub, kui elektrolüüdilahuses on omavahel kontaktis:
a) Sn ja Zn, b) Zn ja Mg, c) Fe ja Cu? Miks?
kuna see metall on aktiivsem ning reageerib paremini. Annab elektrone paremini öra. Elektronpotentsiaal on negatiivsem.
Millised saadused tekivad elektroodidel alltoodud lahuste elektrolüüsil? Kirjutage vastavate elektroodireaktsioonide võrrandid.
CuSO4 (inertne anood);
CuSO4 (Cu anood);
CuCl2 (inertne anood);
H2SO4 (inertne anood);
KOH (inertne anood);
K2SO4 (neutraalne lahus, inertne anood);
NiSO4 (happeline lahus, inertne anood).
VI. LIHTAINED
Kuidas muutub (reeglina) metalliliste elementide sulamistemperatuur perioodilisustabeli A-rühmades ja B-rühmades ülevalt alla ja perioodides vasakult paremale? Miks?
B alla kasvab, kuna kovalentse sideme osakaal on oluliselt suurem. A rühmadel alla kahaneb, metalliline side nõrgeneb, aatomid muutuvad väiksemaks. Vasakult paremale A rühmas suureneb, kuna kovalentse sideme osakaal suureneb, aatomid on väiksemad., tõmbab elektrone rohkem ligi tuum. B metallidel keskele suureneb, kuna
Kuidas muutub lihtainete struktuur (tahkes olekus) järgmises ainete reas (põhjendage vastust): Ar → Cl2 → S (rombiline) → P (punane) → Si?
Argoonil on argooni aatomid ja nende vahel van der Waalsi jõud, Cl2 puhul on Cl2 molekulid ja nende vahel van der Waalsi jõud molekulaarvõre, mittepolaarne kovalente, gaasiline, kuna väike, S puhul aatomvõre., hästi tugev 1D aatomvõre ahelate vahel van der Waals; P aatomiliskihiline võre 2D aatomvõre kihtide vahel van der Waals, kaootiliselt, hästi tugev, ruumiline. Si puhul aatomvõre 3D,igat pidi keemiline side. Kovalentne mittepolaarne
Miks on süsiniku allotroobid väga kõrge sulamistemperatuuriga tahked ained, talle perioodilisustabeli 2. perioodis järgnevate mittemetalliliste elementide lihtained on aga tavatingimustes gaasilises olekus?
Annab hästi tugeva aatomvõre, Moodustab aatomvõre, võrktahkise, järgmised moodustavad kaheaatomilisi molekule, kordsed sidemed. C saab anda ruumilise, teised tasapinnalise
Miks on lämmastik ja hapnik tavatingimustes gaasid, fosfor ja väävel aga tahked ained?
Lämmastikul ja hapnikul madalam molaarmass, väikesed, avaldavad tugevaid tõukejõude ei ole otstarbekas moodustada suuremaid üksusi, fosfor ja väävel saavad kasutada ka d-orbitaale. Saavad kasutada hästi palju elektrone, n ja o ainult omavahel.
Kuidas muutub (reeglina) mittemetallide sulamistemperatuur rühmades ülevalt alla ja perioodides vasakult paremale? Miks?
Ülevalt alla sulamistemperatuur kasvab, ning vasakult paremale kahaneb kuna van der waalsi jõud kahanevad. Aatomid muutuvad väiksemaks, sidemed nõrgemaks vasakult paremaks.
Millisel järgmistest ainetest on kõige kõrgem ja millisel kõige madalam sulamistemperatuur? Miks?
S (rombiline) madalaim, P (punane), Si, C (teemant) kõrgeim;
Na, Cs madalaim, Ba, Ca, Be kõrgeim, Li;
Cu, Au, Mo, Hg madalam, Sc, Cr, W kõrgeim, Zn.
Võrrelge s-, p- ja d-metallide tüüpilisi füüsikalisi omadusi ja põhjendage erinevusi. P-metallised ülevalt alla pehmemateks, d-metallidel alla kõvemaks. S-metallid juhivad hästi elektrit ja on madalate sulamistemperatuuridega.
Kuidas ja miks muutub d-elementide erinevate oksüdatsiooniastmete püsivus rühmas (ülevalt alla) ja piki dekaadi (vasakult paremale)?
Ülevalt alla suurem oks-aste püsib. Vasakult paremale on keskel kõige suurem , siis jälle väheneb. elektronstruktuuri pärast. Kuna aatomid suuremad ja annavad elektrone paremini ära
Põhjendage 4. perioodi d-elementide püsivaima oksüdatsiooniastme muutust dekaadis. Miks on oksüdatsiooniaste III püsivaim skandiumi, kroomi ja raua korral, kuigi need elemendid ei asu perioodis väga lähestikku.
d0 , d5 ja d10 on väga stabiilsed.
Miks piki d-elementide dekaadi maksimaalses (rühma numbriga võrdses) oksüdatsiooniastmes ühendite püsivus väheneb ja oksüdeerivad omadused tugevnevad?
Tuumalaeng kasvab, efektiivne tuumalaeng kasvab. Oksüdeerivad omadused tugevnevad kuna aatom hoiab elektrone tugevamini kinni tugevama tuumalaengu tõttu.
Miks on volframi püsivaim oksüdatsiooniaste ühendites VI, sama rühma elemendil kroomil aga III? Kuna volframi aatom on suurem ja see loovutab elektron kergemini kui kroom.
Kirjutage lihtainetele iseloomulike reaktsioonide võrrandid (valides sobiva lihtaine, millega vastav reaktsioon kindlasti toimub):
a) Metallid
reageerimine hapniku jt. mittemetallidega;
reageerimine tavaliste hapete lahustega;
reageerimine konts. väävelhappega;
reageerimine lämmastikhappega (erineva kontsentratsiooniga);
reageerimine veega või veeauruga (kuumutamisel);
reageerimine leelise lahusega;
b) Mittemetallid
reageerimine hapniku, vesiniku jt. mittemetallidega;
reageerimine (aktiivsemate) metallidega;
reageerimine veega;
reageerimine leelise lahusega;
reageerimine konts. lämmastik- või väävelhappega (kuumutamisel).
BINAARSED ÜHENDID
1. Millised järgmistest binaarsetest ühenditest ja miks on a) happelised, b) aluselised,
amfoteersed: CO2, SO3, Fe2O3, CaO, SiO2, CrO, CuO, CO, NO2, SnO2, Cr2O3,
NO, CrO3, NH3, LiH, CH4, H2S, HF, KCl, NaF, CCl4, PCl5, K2S, Al2S3, CS2 jne?
Millised eelmises küsimuses esitatud binaarsetest ühenditest reageerivad veega? Kirjutage vastavate reaktsioonide võrrandid. Millised nendest reaktsioonidest kulgevad praktiliselt lõpuni?
Võrrelge ja põhjendage CrO, Cr2O3 ja CrO3 happe-aluse omaduste erinevust? Millistes keemilistes reaktsioonides see erinevus avaldub?
Kirjutage binaarsetele ühenditele iseloomulike reaktsioonide võrrandid:
a) Oksiidid
erinevat tüüpi oksiidide reageerimine veega, hapete või leeliste lahustega;
aluselise oksiidi reageerimine happelise oksiidiga.
b) Halogeniidid
erinevat tüüpi halogeniidide reageerimine veega, hapete või leeliste lahustega;
aluselise halogeniidi reageerimine happelise halogeniidiga;
c) Sulfiidid
erinevat tüüpi sulfiidide reageerimine veega, hapete või leeliste lahustega;
aluselise sulfiidi reageerimine happelise sulfiidiga;
d) Hüdriidid
erinevat tüüpi hüdriidide reageerimine veega, hapete või leeliste lahustega;
aluselise hüdriidi reageerimine happelise hüdriidiga;
amfoteerse hüdriidi reageerimine aluselise või happelise hüdriidiga;
hüdriidide reageerimine hapnikuga;
hüdriidide reageerimine happelise binaarse vesinikühendiga.
Kirjutage järgmiste ainete laboratoorsete saamisreaktsioonide võrrandid:
mittemetallid (H2, O2, Cl2, Br2, I2, S, N2 jt.);
metallid (Cu, Ag, Fe, Ni jt.);
binaarsed ühendid (HCl, HBr, HI, H2S, SO2, NH3, NO, NO2, PH3, CO2, C2H2, SiH4 jt.);
nõrgad, vees vähelahustuvad alused ja happed ( Cu(OH)2, Fe(OH)2, Fe(OH)3, H2 SiO3 jt.).
1
